Clear Sky Science · zh
从改造的肿瘤细胞构建的仿生囊泡作为术后个性化癌症免疫疫苗
将肿瘤残余转变为第二道防线
对于许多实体瘤患者,手术只是漫长斗争的第一回合。即便大部分肿瘤被切除,微小的癌细胞簇仍可能残留并在之后播散形成致命的转移。本研究探索了一种新颖方法:把患者自身的肿瘤细胞改造为个性化疫苗,旨在术后追踪并清除这些残余细胞,帮助免疫系统防止癌症复发。
为什么残留癌细胞难以根除
常规疗法难以应对手术切除后残留的细胞。这些散落的细胞常藏匿于远端器官,免受药物和免疫攻击。现有基于免疫的疫苗试图通过称为树突状细胞的专门免疫细胞训练机体识别肿瘤标志,但这些活细胞疫苗难以制造、难以有效转运到关键免疫器官,在临床上效果有限。一个核心挑战是每位患者的癌症携带独特的突变组合,因此一刀切的疫苗往往错过重要靶点。
让癌细胞更容易被发现的隐藏开关
研究人员首先搜寻免疫系统中天然存在、能增强细胞向免疫哨兵展示内部信息的开关蛋白。他们锁定了名为syntaxin 11的蛋白,这种蛋白在免疫细胞中通常含量高,但在许多肿瘤中偏低。通过在小鼠模型的侵袭性乳腺癌细胞中增强该蛋白,研究者发现这些癌细胞开始表现得更像专业的免疫哨兵:它们在表面显示出更高水平的分子“名牌”和助攻信号。实际上,肿瘤细胞被重新编程,以更多地向免疫系统暴露其独特特征,而不是掩藏它们。
构建微小的仿制免疫信使
以这些被重新编程的肿瘤细胞为原料,团队剥离了它们的外膜,用其包裹载有小分子免疫刺激药物的可生物降解纳米颗粒。结果是一群纳米级囊泡,每个囊泡携带着该肿瘤的完整标志物合集以及为杀伤性T细胞准备的“出动”信号。术后皮下注射到小鼠体内时,这些囊泡能高效转运到附近淋巴结——免疫细胞受训之地。在那里它们既能直接激活杀伤性T细胞,也能被天然免疫哨兵吞噬,从而进一步放大反应。实验显示,与更简单的纳米颗粒设计相比,经这些囊泡刺激的T细胞增殖更强,破坏癌细胞的能力也更佳。
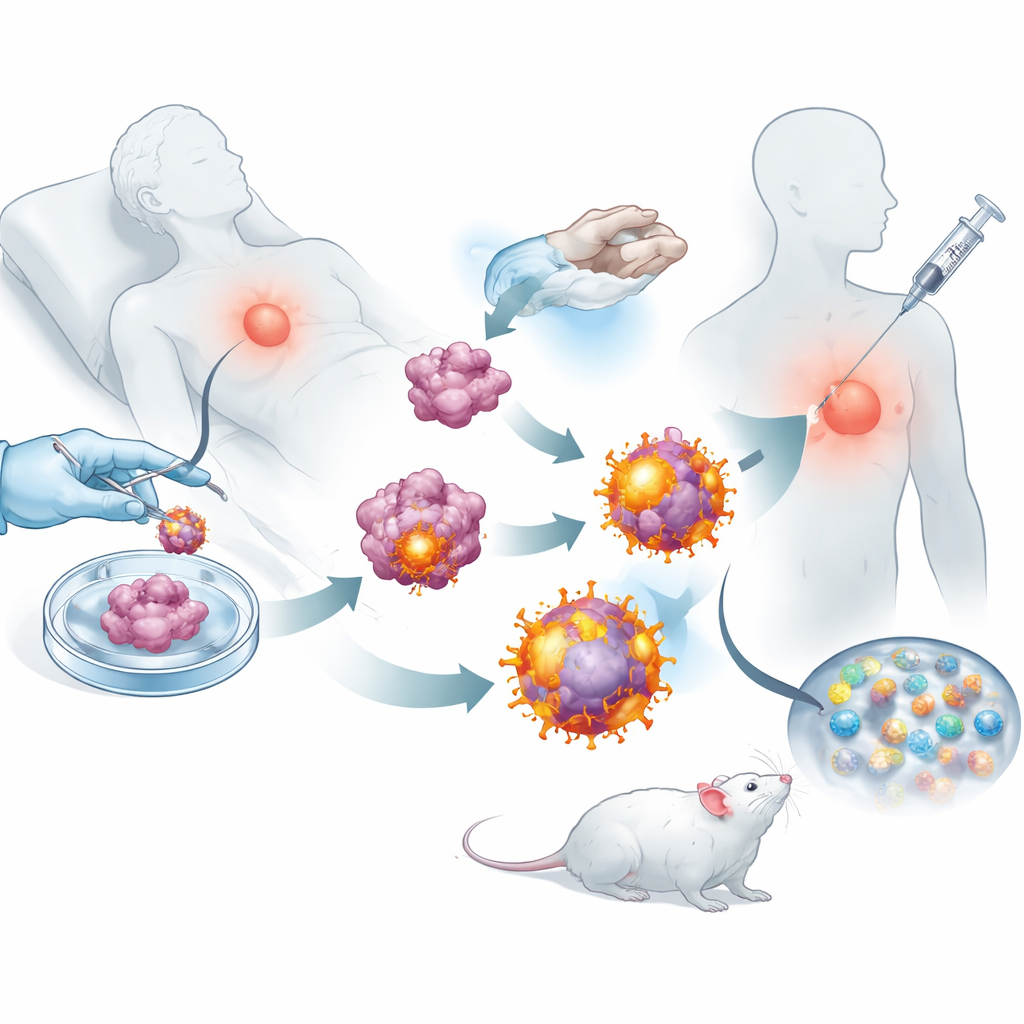
术后控制癌症的长效效果
研究者在多种乳腺癌和黑色素瘤小鼠模型中检验这种定制疫苗能否真正改变疾病进程。在多数乳腺肿瘤被外科切除的动物中,接受疫苗的鼠群复发肿瘤更小,肺转移也显著减少。处理组的淋巴结、脾脏和肿瘤中充斥着活跃的杀伤性T细胞和长期记忆细胞,表明免疫系统既被唤醒又被长期训练。当将该疫苗与获批的免疫检查点抑制抗体联合使用(该类抗体可防止肿瘤使T细胞失能)时,疫苗实现了持久的肿瘤控制,在许多小鼠中甚至达到了肿瘤完全消退和长期存活。
加速个性化治疗的实现
把这一概念转化为现实疗法的一大障碍是时间:基于基因的方法对肿瘤细胞重新编程往往耗时。为此,团队筛选天然化合物,发现了脱氧穿心莲内酯(deoxypodophyllotoxin),一种能快速提升关键信号蛋白及相同免疫刺激表面标志的小分子。利用这一捷径,他们在更短时间内构建出类似的囊泡包覆纳米颗粒,同时保留了唤起强烈肿瘤特异性免疫反应的能力。测试显示,用该小分子制备的疫苗与基因方法制备的疫苗同样有效,其益处依赖于识别正确的肿瘤类型,而非对癌细胞的广谱毒杀。
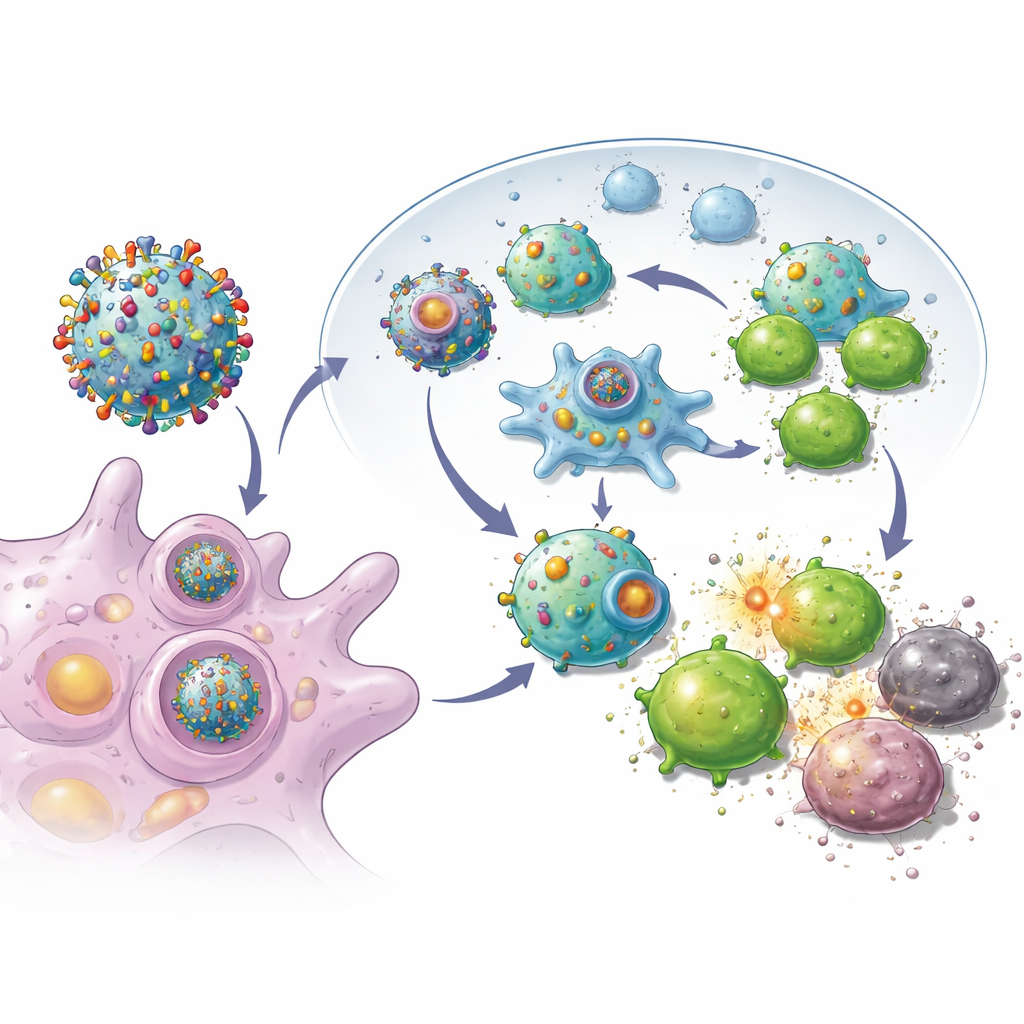
这对未来癌症护理可能意味着什么
对非专业读者来说,核心信息是:患者自身的肿瘤可以被改造成免疫系统的微型训练工具。通过将癌细胞转化为富含个性化信息的来源,并将这些信息封装到稳固的纳米级载体上,这种方法旨在清扫手术留下的残余细胞并阻止新病灶生长。尽管在将此类疫苗常规化应用于人类之前仍需完成许多步骤——包括在人类肿瘤中证明安全性与有效性并建立可靠的生产流程——这项工作勾勒出一条路径,朝着高度个体化的术后治疗前进,动员机体的防御来完成外科所开启的工作。
引用: Yu, P., Jin, Z., Meng, L. et al. Biomimetic vesicles engineered from modified tumour cells act as personalized vaccines for post-surgical cancer immunotherapy. Nat. Nanotechnol. 21, 443–454 (2026). https://doi.org/10.1038/s41565-025-02113-w
关键词: 癌症疫苗, 免疫疗法, 纳米医学, 术后治疗, 个性化肿瘤学