Clear Sky Science · zh
皮肤雄激素通过群体感应调节金黄色葡萄球菌的致病性
为什么皮肤上的激素很重要
男性比女性更容易出现更严重的皮肤感染,但其原因长期不清楚。这项研究表明,直接存在于皮肤表面的激素,尤其是男性激素睾酮,能够把一种常见细菌的行为从沉默的邻居转换为危险的入侵者。理解我们自身激素与微生物之间这种隐秘的对话,不仅解释了长期存在的性别感染风险差异,也指向了一种意想不到的方法,可以在不依赖传统药物的情况下使抗生素耐药菌失去攻击力。
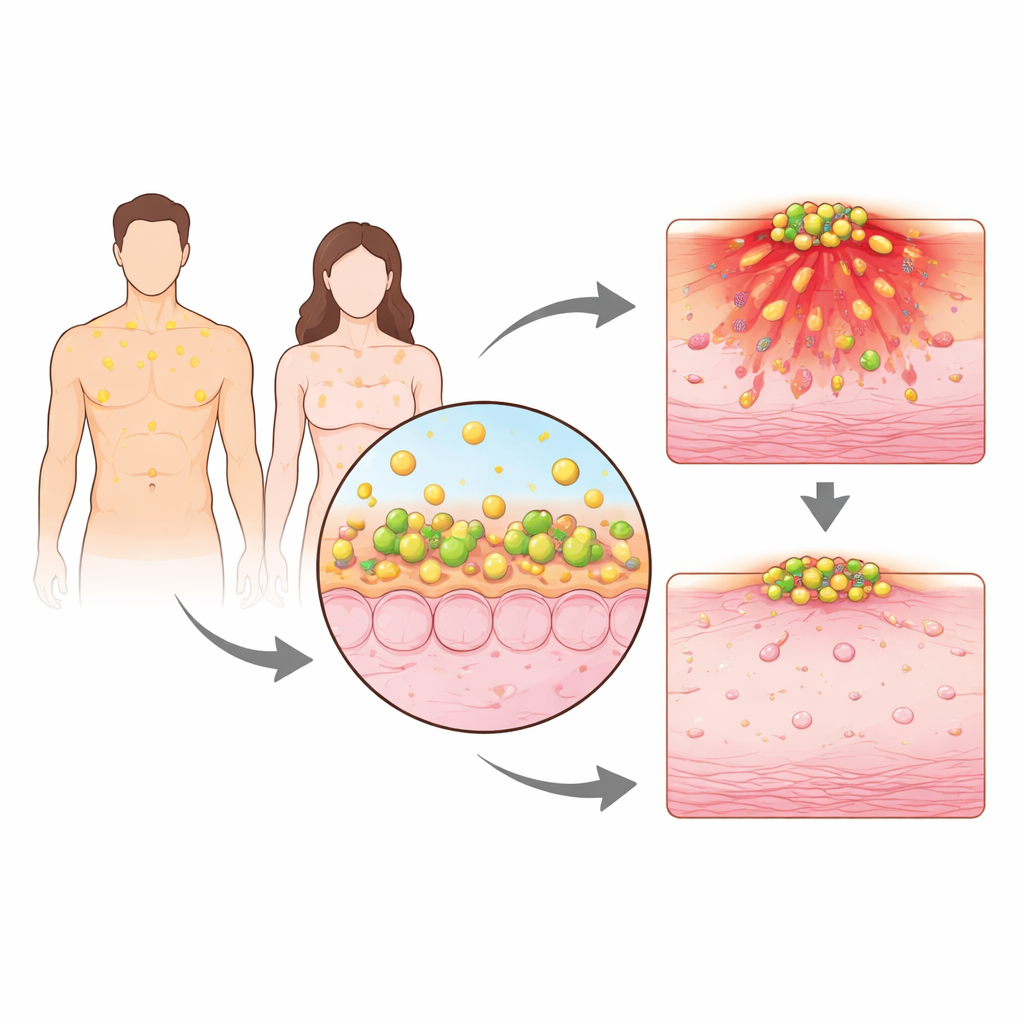
日常包围皮肤的激素
我们的皮肤不仅保护我们免受外界侵害,还能合成并释放自身的一系列激素。研究人员使用能吸收皮脂的小型粘贴膜,测量了健康男女面部多日间的睾酮水平。两性在皮肤表面都产生稳定的纳摩尔量睾酮,但男性始终较高。在小鼠中,雄性在皮肤分泌物中也显示出更高的睾酮及其密切相关的双氢睾酮水平。这些更高的雄激素水平与当动物暴露于金黄色葡萄球菌时更严重的感染相伴随——金黄色葡萄球菌是人体皮肤与软组织感染的重要病原体。
降低皮肤激素可保护免受感染
为检验皮肤自身产生的激素是否确有影响,研究团队构建了皮肤细胞缺失一种用于局部生成睾酮关键酶的小鼠模型,而血液中的激素水平保持不变。这些“雄激素缺陷”小鼠皮肤结构和屏障功能正常,但分泌到皮肤表面的睾酮、孕酮和双氢睾酮明显减少。用耐甲氧西林金黄色葡萄球菌(MRSA)感染时,这些小鼠表现出较弱的细菌信号、较轻的红肿与肿胀、较少的组织损伤以及更好保留的屏障功能。值得注意的是,当在雌性雄激素缺陷小鼠的皮肤上涂抹少量睾酮时,其感染变得更严重并开始类似雄性小鼠的情况。这表明,是皮肤表面的雄激素,而非全身激素状态,帮助决定了金黄色葡萄球菌疾病的发生环境。
细菌如何窃听我们的激素
金黄色葡萄球菌使用一种称为群体感应的通讯系统来决定何时产生损伤宿主细胞的毒素。该系统的核心是一对感受器 AgrC 和 AgrA,通常响应小的细菌肽。当研究人员将不同株的金黄色葡萄球菌暴露于微量睾酮或双氢睾酮时,细菌上调了通常在群体感应过程中开启的基因,包括编码强效毒素的基因。这一现象在多种临床菌株中都出现,包括 MRSA 以及来自异位性皮炎患者的分离株。睾酮增强了细菌对人类红细胞、皮肤细胞和中性粒细胞的杀伤力,但并未促进细菌本身的生长。在皮肤雄激素低的小鼠体内,携带群体感应报告基因的菌株显示出明显更弱的激活,证实皮肤激素在活组织中驱动了细菌的“群体决策”。
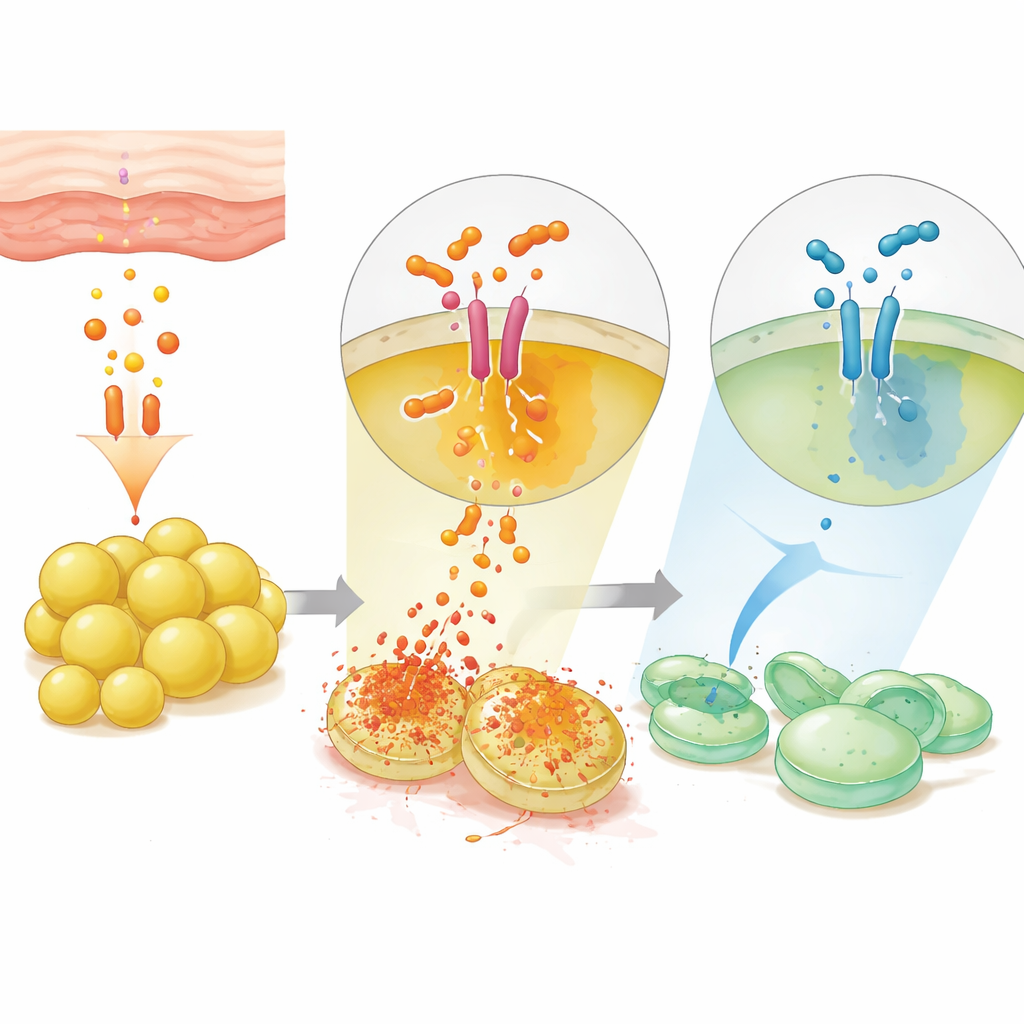
直接的分子握手与内建的关断开关
令人惊讶的是,即便在无法自身合成信号肽的突变菌株中,睾酮仍能激活群体感应,这意味着该激素可以替代通常的细菌触发物。然而,这需要细菌表面的完整 AgrC 感受器及其配对的 AgrA;当任一被破坏时,睾酮便不再促进毒素基因表达或引发细胞损伤。计算模拟表明,睾酮嵌入 AgrC 上一个疏水口袋,这个位置不同于常见的肽结合位点,物理上将受体推向其活化构象。研究团队随后反转思路,测试了睾酮的镜像异构体——对映体睾酮(ent‑T)。尽管化学结构相近,ent‑T 阻断了群体感应,减少毒素产生并保护人类细胞免受细菌损伤。涂抹于受感染的小鼠皮肤后,ent‑T 在雌雄两性中都抑制了群体感应活性,作为毒力的分子刹车起作用。
对未来治疗的意义
简而言之,该研究揭示金黄色葡萄球菌可以“嗅到”我们皮肤上的睾酮,并利用这一信号来决定何时发动攻击。男性较高的皮肤雄激素水平有助于解释他们为何更易出现严重的金黄色葡萄球菌感染。同样重要的是,这项工作提出了一种新的治疗思路:与其直接杀灭细菌,不如通过阻断其激素感受器来降低其攻击性。像 ent‑T 这样的化合物,或旨在降低皮肤表面雄激素的策略,可能削弱 MRSA 及相关菌株,使感染更易控制、损害更小,同时避开一些推动抗生素耐药性的压力。
引用: John, M.S., Chinnappan, M., Sturges, C.I. et al. Skin androgens regulate Staphylococcus aureus pathogenicity via quorum sensing. Nat Microbiol 11, 704–717 (2026). https://doi.org/10.1038/s41564-026-02261-2
关键词: 皮肤激素, 金黄色葡萄球菌, 群体感应, MRSA 感染, 睾酮信号