Clear Sky Science · zh
单价类拟天然产物通过其天然的E3 KLHDC3超速降解IDO1
关闭有利于癌症的酶
我们的免疫系统不断巡查癌细胞,但肿瘤常通过劫持机体自身的化学机制进行反击。这个拉锯战中的关键角色之一是称为IDO1的酶,它帮助肿瘤削弱免疫细胞。本研究描述了一类新型小分子,它们不仅仅阻断IDO1的活性——还说服细胞将该酶彻底清除。通过利用细胞的天然清理机制,这些化合物可能以旧药无法实现的方式恢复对肿瘤的免疫攻击。
肿瘤如何利用一个代谢看门人
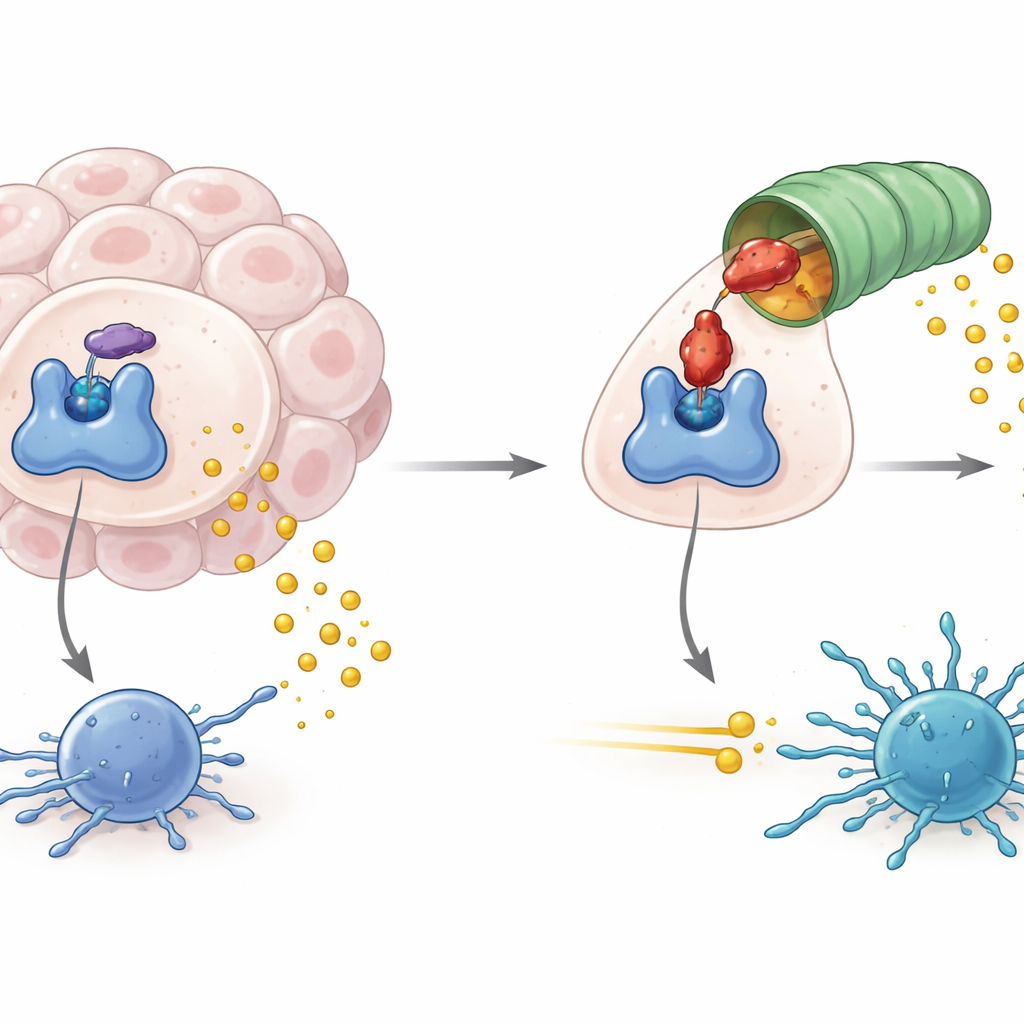
IDO1位于将氨基酸色氨酸分解为产物犬尿喉(kynurenine)这一代谢通路的入口处。当IDO1丰度高且活性强时,色氨酸水平下降而犬尿喉上升,营造出一种抑制免疫细胞(包括抗肿瘤T细胞)活性的化学环境。高水平的IDO1活性不仅与抗肿瘤免疫力减弱相关,还与病毒驱动的淋巴瘤和某些形式的神经退行性疾病有关。因此,药物开发者一直专注于阻断IDO1的酶学活性,期望切断这种免疫抑制信号,从而增强现有的癌症免疫疗法的疗效。
为何简单的酶抑制剂未达预期
尽管在动物研究中取得了令人鼓舞的结果,但传统IDO1抑制剂的临床试验令人失望。一种新出现的解释是,IDO1不仅仅是一个简单的催化剂。即使其化学活性被阻断,该蛋白本身仍能作为一个信号枢纽,继续促进肿瘤生长和扩散。某些抑制剂甚至会稳定IDO1,增加细胞中该蛋白的含量。换言之,仅仅关闭催化功能可能无法触及其促肿瘤的非酶学作用——甚至可能在某些情况下加强这些作用。
设计触发自毁的化合物
作者筛选了一个大型的“拟天然”分子库——这些合成化合物由受天然产物启发的片段重新组合而成。他们发现了一类名为iDegs的分子,源自一种类植物的构件(−)-没药酚((−)-myrtanol)。这些化合物结合在IDO1用于含铁辅因子血红素(haem)的常位点内。通过置换血红素,iDegs既削弱了IDO1产生犬尿喉的能力,又关键性地重塑了蛋白尾部的一部分。高分辨率的晶体结构显示,当iDegs占据血红素位点时,它们使一个C端螺旋松动并部分无序,而该螺旋在正常情况下处于紧凑、受保护的构象中。
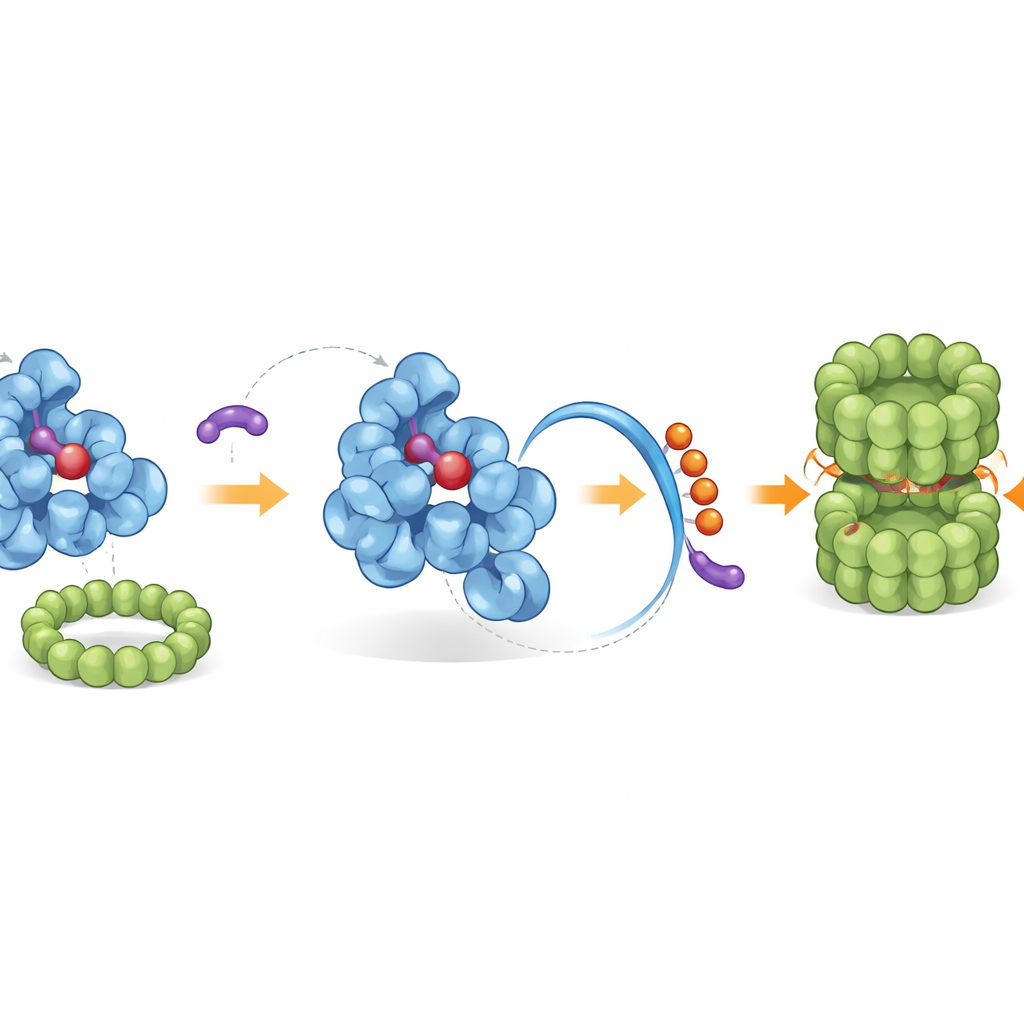
招募细胞的本土清理队伍
被重构的尾部暴露出一个内建的“末端标签”,这是细胞废物处理机制能够识别的。通过遗传筛选和生化重构,研究人员鉴定出一个特定的连接酶复合体,称为CRL2–KLHDC3,它天然地在IDO1暴露的尾部附加小的泛素“旗标”,将其标记为由蛋白酶体——细胞的分子粉碎机——降解。在正常条件下,只有无血红素形式的IDO1能有效被这样标记,而结合血红素的IDO1受到保护。iDegs通过仅结合无血红素形式来倾斜这一平衡,从而放大了自然的降解途径。该系列中效力强的分子不仅阻断犬尿喉产生,还显著增加IDO1上的泛素标记并在多种癌细胞类型中急剧降低其蛋白水平。
改变IDO1的命运——以及免疫反应
这种双重作用的行为具有重要的功能性后果。在卵巢癌细胞的迁移实验中,一种临床研究过的会稳定酶的IDO1抑制剂实际上加速了细胞运动,这与IDO1的非酶学促肿瘤作用一致。相比之下,一种iDeg化合物减缓了迁移,符合同时抑制酶学活性并使蛋白被消除的结果。因此,该研究揭示了一种操纵IDO1的新方法:不是用笨重的设计分子强行将其拖向不相关的连接酶,而是“超充能”细胞中已存在的天然降解通路。
这对未来癌症疗法意味着什么
对非专业读者而言,关键信息在于抑制酶的质量——而不仅仅是数量——很重要。这些新小分子像精密开关:它们将IDO1锁定到一种细胞易于识别并摧毁的脆弱构象,从而同时切断其代谢和信号学上对肿瘤存活的贡献。由于iDegs体积紧凑、具备类药物特性并依赖细胞自身的连接酶来去除IDO1,它们可能比早期的“蛋白降解”药物提供一种更为微妙且适用范围更广的方法。如果类似策略能应用于其他问题蛋白,这项工作预示着新一代疗法的可能——这些疗法促使病变细胞拆解自身的分子武器。
引用: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
关键词: IDO1, 癌症免疫治疗, 靶向蛋白降解, 泛素连接酶, 小分子降解剂