Clear Sky Science · zh
赖氨酸11位泛素化驱动cGAS–STING与Toll样受体3和4的I型/III型干扰素诱导
我们的细胞如何发出警报
当病毒或有害分子入侵机体时,细胞必须在数分钟内决定是否发起强有力的抗病毒警报信号——干扰素。这些信号可以使我们免受严重感染,但若误触发也会导致破坏性的自身免疫性疾病。本研究揭示了细胞内一个之前未被发现的分子“总控板”,它帮助决定何时开启干扰素反应、何时抑制。理解这一“总控板”为改进疫苗、抗病毒疗法以及针对干扰素驱动疾病的治疗提供了线索。
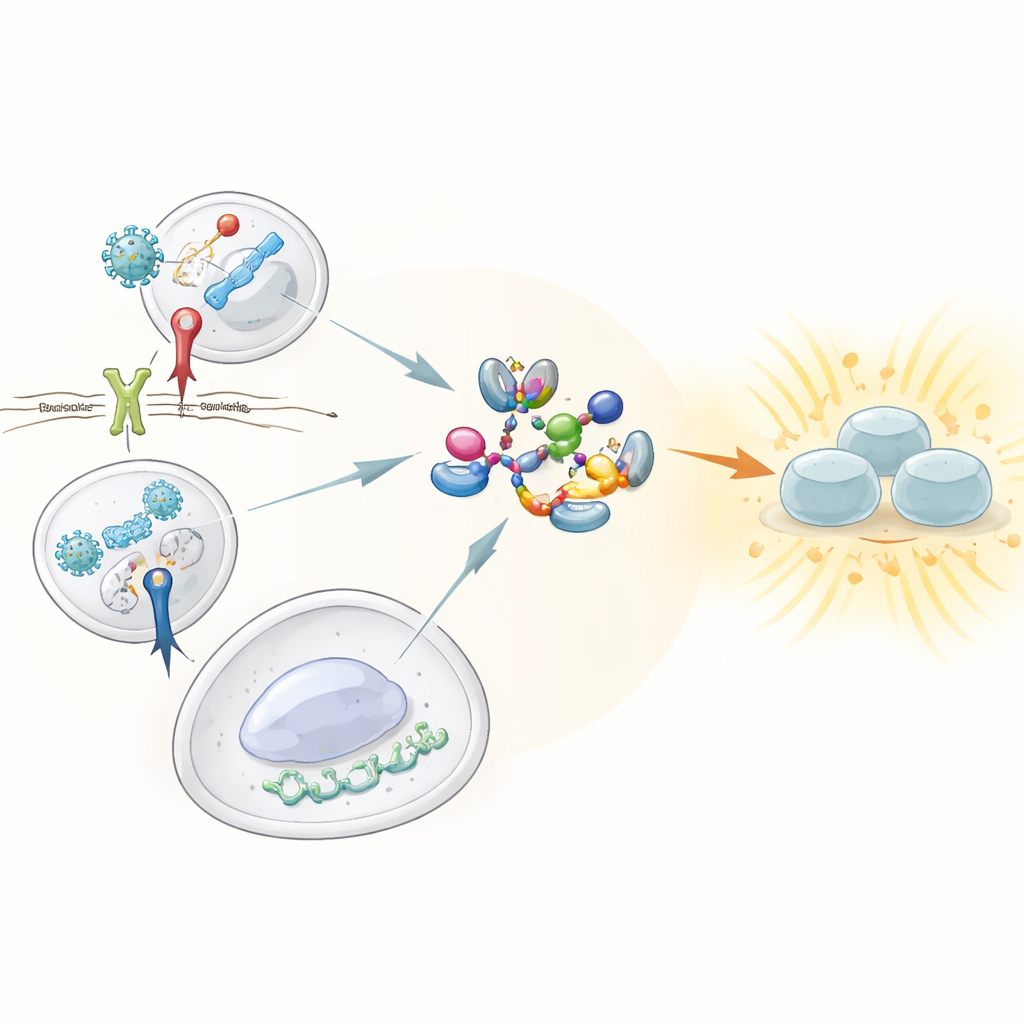
感知危险的守卫者
我们的先天免疫系统依赖被称为模式识别受体的哨兵,巡查病毒和细菌的特征性分子。在这些受体中,有三者在触发强烈干扰素反应方面尤为重要:识别双链病毒RNA的Toll样受体3(TLR3);感知细菌细胞壁成分的Toll样受体4(TLR4);以及能识别细胞内异常DNA的cGAS–STING通路。这三者都必须激活一个中心酶TBK1,TBK1进而激活转录因子IRF3,驱动I型和III型干扰素的产生。此前这些传感器如何汇聚到TBK1并将其翻转为活性状态尚不清楚。
一个隐秘的分子连接器
研究人员发现一种名为ANKIB1的蛋白充当了这些传感器与TBK1之间的关键连接器。ANKIB1是一种将小分子标签——泛素链——连接到其他蛋白上的酶。重要的是,它构建的是一种特定类型的链,基于称为“K11”的连接位点,这种连接位点此前更多与细胞分裂相关,而非免疫。在缺乏ANKIB1的人类细胞中,刺激TLR3或激活STING不再能正常诱导TBK1和IRF3的活化,干扰素基因几乎不被激活。恢复ANKIB1后反应得以恢复,表明该酶对于驱动这一路径的抗病毒警报既是必需的又是充分的。
构建用于中继蛋白的对接平台
更细致的观察揭示了ANKIB1如何发挥作用。当TLR3或STING感知到危险时,它们组装成多蛋白平台,称为信号体。ANKIB1通过其识别泛素的结构域被招募至这些平台。到位后,它在若干关键成分上修饰K11连接的泛素链——包括适配子蛋白TRIF与STING自身以及其他信号分子。这些链并非简单地标记蛋白以便降解;相反,它们像分子“魔术贴”一样。另一种蛋白Optineurin(OPTN)被专门吸引到这些经修饰的位点。作为中继适配子,OPTN随后将TBK1带入复合体,使其得以被激活并将信号传递给IRF3与干扰素基因。移除OPTN会导致TBK1激活崩溃,进一步强调了ANKIB1介导的K11标记与OPTN结合构成了一个单一且必需的轴线。
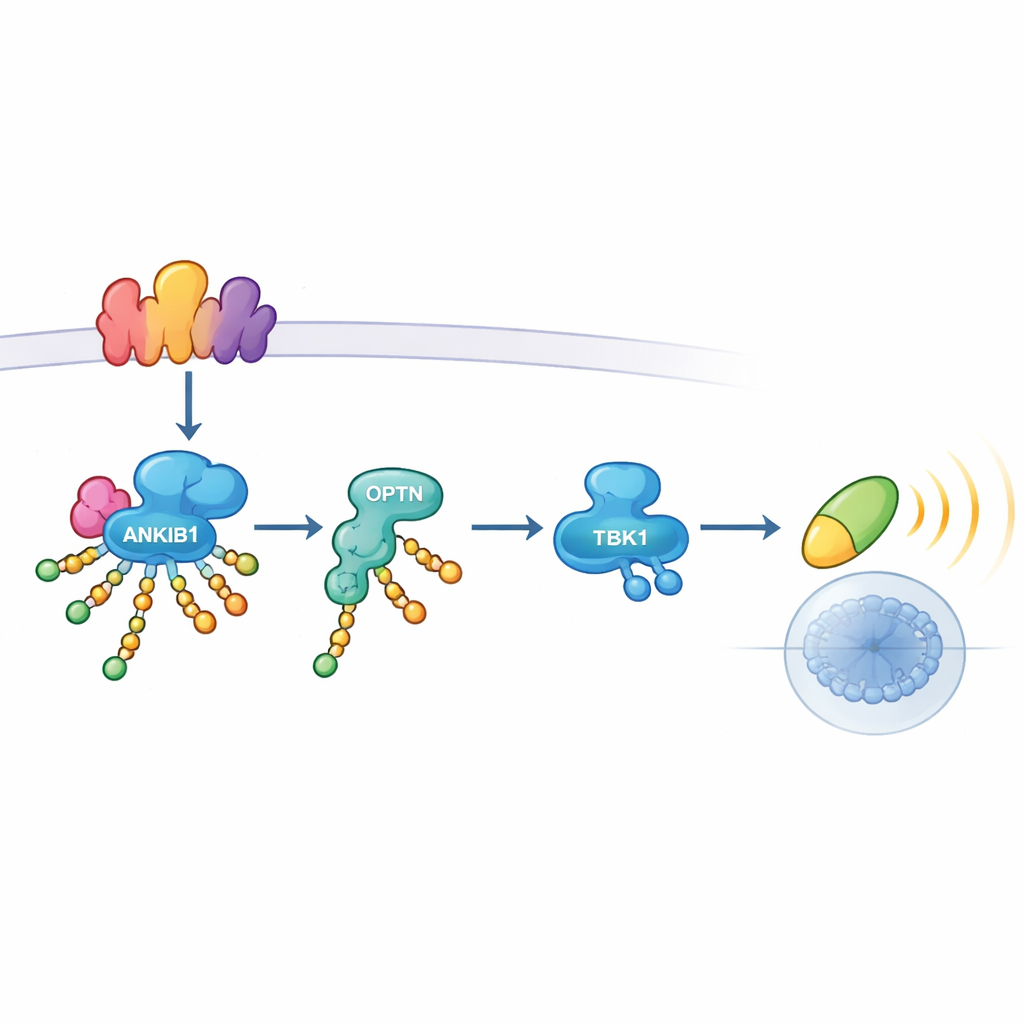
该通路何时重要——何时不重要
研究团队接着询问该机制是否普遍存在于所有抗病毒传感器中。他们发现ANKIB1对于通过TLR3、TLR4的TRIF依赖臂以及cGAS–STING通路诱导干扰素是至关重要的,这些通路都使用OPTN作为与TBK1连接的主要适配子。相反,另一种识别病毒RNA的传感器RIG-I依赖不同的一组适配子,不需要ANKIB1或OPTN来激活TBK1。小鼠实验与细胞研究结果一致:缺失Ankib1的动物在激活TLR3或STING后产生的干扰素显著减少,能避免致死性的干扰素驱动炎症综合征,但对依赖cGAS–STING驱动干扰素来控制的单纯疱疹病毒1型(HSV-1)等DNA病毒则更易感。对于主要由RIG-I检测的流感病毒,反应则大体保持完整。
平衡保护与伤害
综上所述,这些结果表明ANKIB1生成的K11连接泛素链是先天抗病毒信号传导主要分支中的一种核心“通用货币”。通过为OPTN创建对接位点,ANKIB1帮助组装精确的分子中继,将由TLR3、TLR4(通过TRIF)和cGAS–STING感知到的危险转化为强烈的干扰素产生。该轴具有双刃剑特性:它对某些病毒的防御至关重要,但在过度激活时也助长干扰素驱动的炎症性疾病。由于ANKIB1的催化活性和特定结构域对其功能是必需的,它们成为未来药物设计中有吸引力的靶点,既可用于抑制自身免疫病中有害的干扰素反应,也可用于增强抗病毒免疫在不足时的能力。
引用: Betrancourt, A., Cinko, M.T., Varanda, A.B. et al. Lysine-11 ubiquitination drives type-I/III interferon induction by cGAS–STING and Toll-like receptors 3 and 4. Nat Cell Biol 28, 608–621 (2026). https://doi.org/10.1038/s41556-026-01886-z
关键词: 先天免疫, 干扰素信号传导, 泛素化, cGAS–STING通路, 病毒感染