Clear Sky Science · zh
使用深度学习的时间解析功能基因组学揭示自噬的全局层级控制
细胞如何自我回收——以及如何知道何时停止
我们的细胞通过一种称为自噬的过程回收自身部件以度过匮乏期——字面意思是“自我吞噬”。回收太少会导致受损组分堆积;回收过多则会让细胞相互吞噬。这项研究提出了一个看似简单但对衰老和疾病影响深远的问题:活细胞如何在营养起伏时机上正确地开启和关闭自噬?
追踪数千个细胞经历盛宴到饥荒的周期
为了解决这个问题,研究者以酵母为模型,观察了近六千种不同突变株在饥饿与恢复过程中表现。每个酵母株携带标记自噬相关结构的荧光标记,借助高性能显微镜在去除并随后恢复营养的过程中每小时拍摄图像。研究团队没有人工分类这些图像,而是训练深度学习算法仅基于图像特征(而非人为判断)识别细胞是否处于自噬状态。这产生了几乎覆盖整个酵母基因组的精确自噬活动时间曲线,展示了每个突变株对营养变化反应的速度和强度。 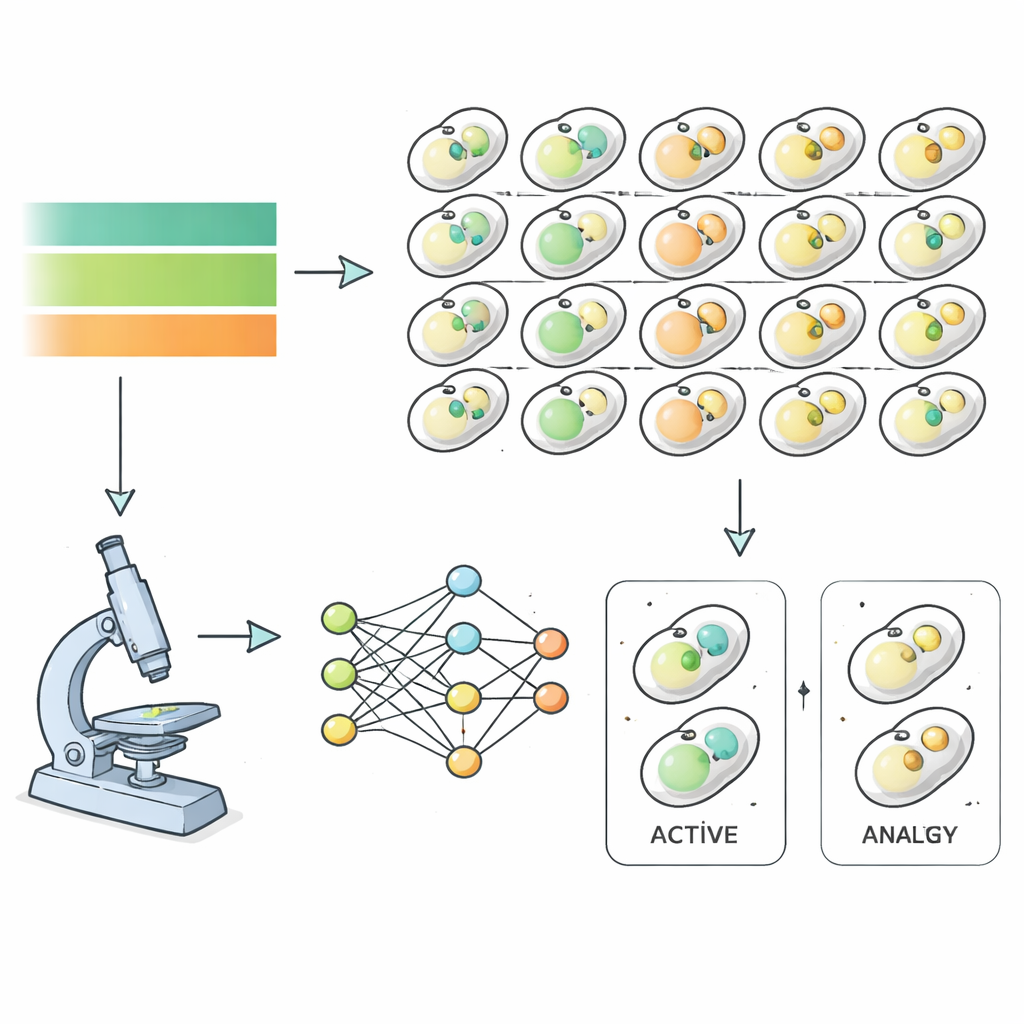
细胞处理回收失误的六种截然不同方式
通过对这些时间曲线进行数学拟合,作者为每个突变株提取了详细的“动力学指纹”——自噬开启的速度、持续的时间以及关闭的陡峭程度。对这些特征进行分组后,发现了六类广泛的行为模式。有些突变株是“超敏感”的,在饥饿和营养恢复时都反应非常快;另一些是“低敏感”的,反应迟缓。一组表现为“高活性”,在基线条件下回收异常升高,而另几组在启动适当反应方面存在不同程度的失败。重要的是,已知的核心自噬基因落在最严重的类别中,这验证了该方法捕捉到的是生物学信号而非测量噪声。
绘制自噬调控的层级结构
自噬并非孤立发生,而是嵌入在细胞更广泛的调控网络中。团队将其动态谱投射到酵母的大型基因与蛋白相互作用图上。丧失导致严重自噬缺陷的基因倾向于位于这些网络中已知自噬“核心机器”附近,而影响较轻的突变株则更远,表明它们通过更间接的途径发挥作用。通过检查每类行为中富集的细胞过程,研究者发现饥饿触发的激活主要由处理RNA、蛋白质合成和能量代谢的通路塑造,而在营养恢复后关闭自噬更依赖膜运输和融合步骤,这些步骤负责清除回收囊泡。
深入研究囊泡如何形成与清除
自噬通过两个主要阶段进行:构建载货囊泡,然后将其与细胞的回收隔室融合以便分解。为解析这些阶段,研究者挖掘了神经网络内部的“潜在空间”——网络用来区分图像的压缩表征。通过将该内部表征投影到二维地图上,他们可以看到细胞群体从无囊泡的区域移动,经过含有许多自由囊泡的区域,最终到达囊泡被清除的区域。借助与被锁定在不同阶段的参考突变株的统计比较,他们为每个基因量化了其主要影响是囊泡形成、囊泡清除还是两者兼有。这一分析表明,囊泡形成的控制对随时间变化的氮水平高度敏感,而清除机制则更稳定,常常成为总体回收通量的主要限制因素。 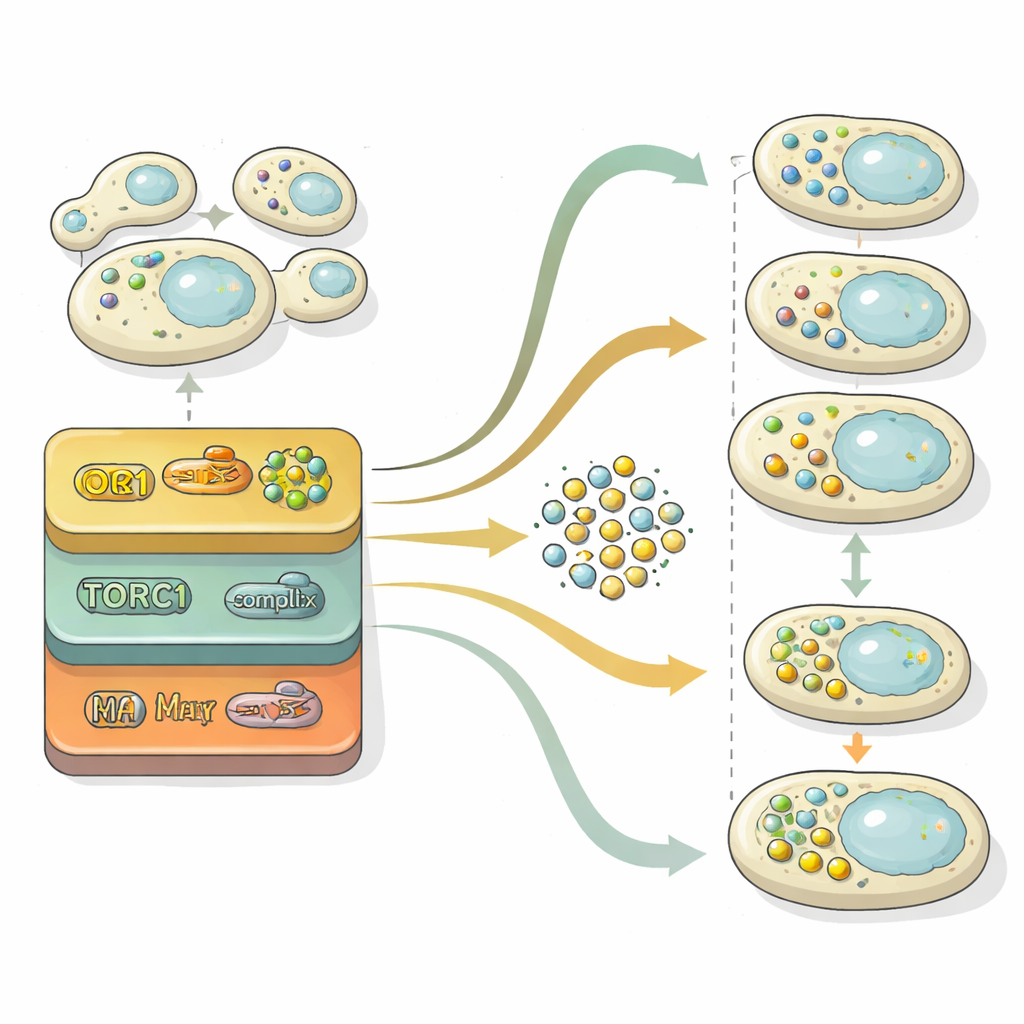
回收上的隐性制动器:逆行通路
其中一项最引人注目的发现涉及所谓的逆行(RTG)通路,它将线粒体的信号传递到细胞核。缺失RTG组分的酵母即使在营养充足时也产生过多自噬泡,并且在营养恢复后难以清除它们。后续的详细实验显示,该通路控制关键自噬基因的表达,特别是主启动子ATG1的表达,这在很大程度上独立于众所周知并被雷帕霉素等药物靶向的营养感受器TORC1。实际上,RTG信号充当一个时变的制动器,在富营养条件下防止自噬失控,并在条件改善时帮助终止反应。
这对健康与治疗意味着什么
总体而言,这项工作提供了一张基因组范围、时间解析的图谱,展示了细胞如何在变化的营养条件下调节自噬。研究揭示激活与关闭并非镜像过程:影响回收启动的基因远多于影响其关闭的基因,长期平衡在很大程度上依赖于囊泡清除和诸如RTG通路的转录性制动器。对普通读者而言,关键结论是细胞的自我吞噬受多层次、分层的控制,我们现在能以高精度绘制这些层次。这类系统级的视角可能最终指导更为细致的治疗策略,在特定阶段调节自噬——增强有益的回收,同时避免长期、失控的自我消化所带来的有害后果。
引用: Chica, N., Andersen, A.N., Orellana-Muñoz, S. et al. Time-resolved functional genomics using deep learning reveals global hierarchical control of autophagy. Nat Cell Biol 28, 465–479 (2026). https://doi.org/10.1038/s41556-025-01837-0
关键词: 自噬, 深度学习, 酵母遗传学, 营养感知, 细胞回收