Clear Sky Science · zh
治疗性免疫接种后在猿类与人类免疫缺陷病毒感染中的功能性抗体特征
这项研究为何重要
对于感染 HIV 的人来说,现有药物可以将病毒控制住,但很少能让患者停药。这项研究探讨治疗性疫苗是否能训练免疫系统——特别是抗体——自行帮助控制病毒,使我们更接近长期缓解或在无需终身服药的情况下实现功能性治愈。
对 HIV 疫苗的新视角
研究人员测试了最初为预防感染而设计的 HIV “马赛克”疫苗,并将其重新用于已经感染且通过常规药物将病毒抑制的人和猴子。这些疫苗利用无害的载体病毒(Ad26 和 MVA)传递精心设计的 HIV 蛋白,以覆盖多种病毒株。团队关注的不仅是疫苗是否提高了抗体水平,还着眼于这些抗体在结合到 HIV 感染细胞后到底能做什么。
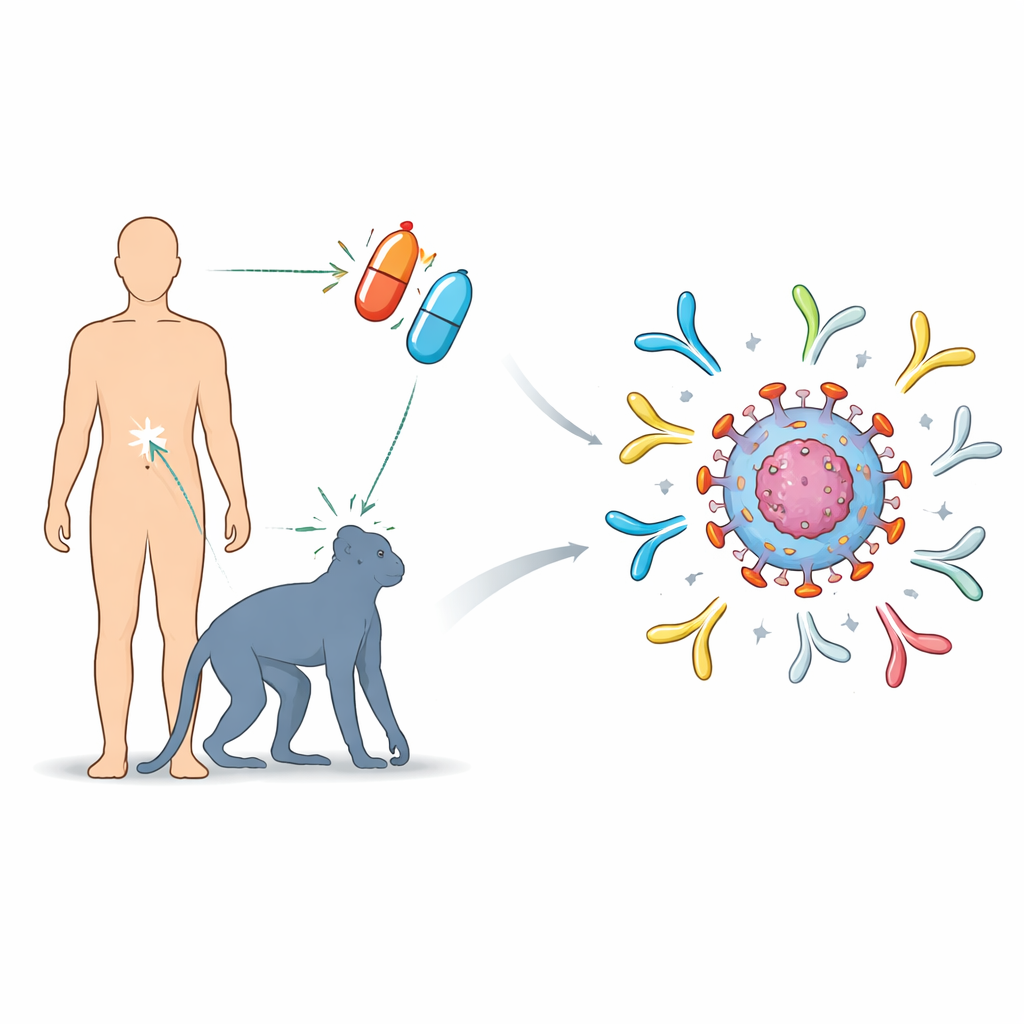
不仅仅是阻断的抗体
人们通常把抗体看作简单的阻断者,附着在病毒上阻止其进入细胞。但抗体的“尾部”区域还能召集免疫系统的其他力量。在接种疫苗并感染杂交猿猴-人类免疫缺陷病毒的恒河猴中,针对 HIV 外衣蛋白的抗体水平在接种后显著上升。这些抗体更好地与免疫细胞上的特殊受体结合,并触发一系列有益反应:标记靶点以便清除、吸引吞噬病毒颗粒的清道夫细胞,以及激活能杀死被感染细胞的自然杀伤细胞。
短暂的强效,持久的影响
猴子中最强的抗体反应出现在加强免疫后,随后在数月内逐渐减弱。即便如此,接种疫苗的动物仍比未接种对照保持更高水平的功能性抗体活性。当随后暂停药物治疗时,这些抗体特征并不能可靠预测病毒何时首次强烈反弹。然而,那些抗体表现出更强功能性特征的动物在初次反弹后往往达到较低的长期病毒水平,表明此类反应可在病毒回归后帮助更好地限制病毒。
将疫苗与工程化抗体配合使用
部分猴子还接受了 PGT121——一种实验室制备的广谱中和抗体。既接受疫苗又接受 PGT121 的动物在停止常规药物后最有可能保持对病毒的强有力控制。在 PGT121 存在期间所做的测量显示,更好的抗体尾部受体参与度与病毒重新出现前延迟时间更长相关。这一模式提示,将治疗性疫苗与强效的工程化抗体结合使用,可能在某些方式上缩小或削弱病毒储库,从而在这些额外抗体消失后仍带来长期收益。
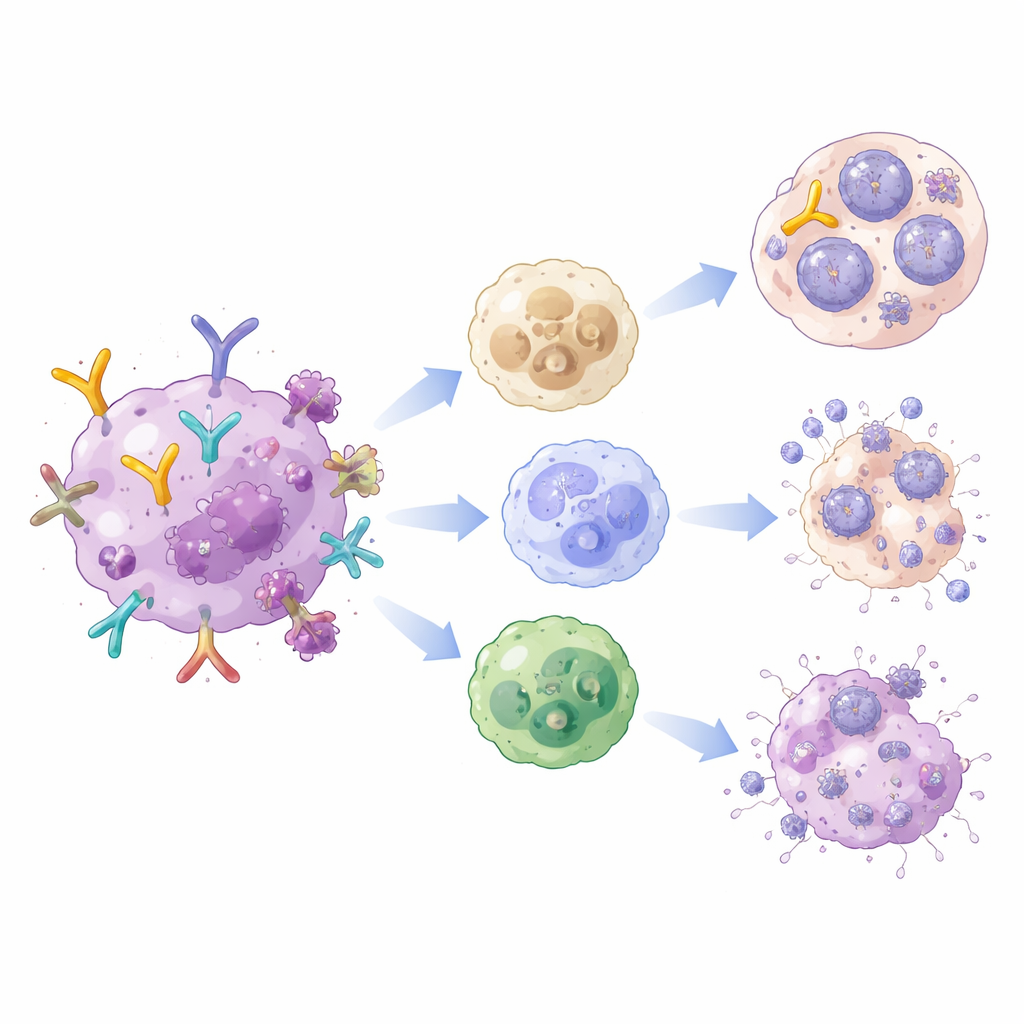
这对 HIV 感染者意味着什么
研究团队在病毒已被治疗抑制的人群中进行了平行试验。在这里,将 Ad26 免疫与额外 HIV 蛋白加强剂配对的疫苗方案,最明显地增强了功能性抗体,而单独的 Ad26 与 MVA 则效果较为温和。由于人类研究未中断治疗,无法显示这些反应是否能转化为更好的病毒控制。不过,在猴子和人类的结果中,信息是一致的:合适的治疗性疫苗能唤醒不仅能识别 HIV、还能招募机体细胞攻击被感染靶点的抗体。利用这些多功能抗体反应——尤其是与其他免疫手段结合——可能成为未来策略的重要组成部分,旨在用更少依赖每日抗逆转录病毒药物的方式实现持久的 HIV 控制。
引用: Ilan, S., Bartsch, Y., Jung, W. et al. Functional antibody signatures following therapeutic immunization in Simian and Human immunodeficiency virus infection. npj Vaccines 11, 62 (2026). https://doi.org/10.1038/s41541-026-01390-3
关键词: HIV 治疗性疫苗, 功能性抗体, Fc 效应功能, 病毒反弹控制, 广谱中和抗体