Clear Sky Science · zh
对疫苗反应的精细表型分析揭示中和抗体差异的转录组决定因素
为什么某些疫苗对特定人群更有效
当我们为新冠疫苗接种卷起袖子时,可能会假设每个人的免疫系统反应相同。实际上,人们在建立保护性抗体的速度和强度上存在很大差异。这项研究随访了接受灭活SARS-CoV-2疫苗的成人,显示疫苗反应呈现不同的模式,每种模式由在基因和血细胞中早期出现的不同免疫信号驱动。理解这些模式有朝一日可能帮助定制接种时间表,以便每个人都能获得所需的保护。
同一疫苗接种后的三条保护路径
研究人员追踪了73名接受两剂灭活新冠疫苗的健康成人。他们在接种前、第二针后一周以及大约一个月后测量了能够阻断病毒的中和抗体。研究没有简单地将人分为“高反应者”和“低反应者”,而是采用数据驱动方法按抗体随时间变化的轨迹对人群进行分组。出现了三种清晰的模式:“低-延迟”组,其抗体上升缓慢且幅度有限;“快速-稳定”组,其抗体迅速升高随后趋于稳定;以及“持续上升”组,其抗体持续上升至最高水平。这些模式无法用年龄、性别或体重解释,且仅部分与受种者所用灭活疫苗品牌有关。
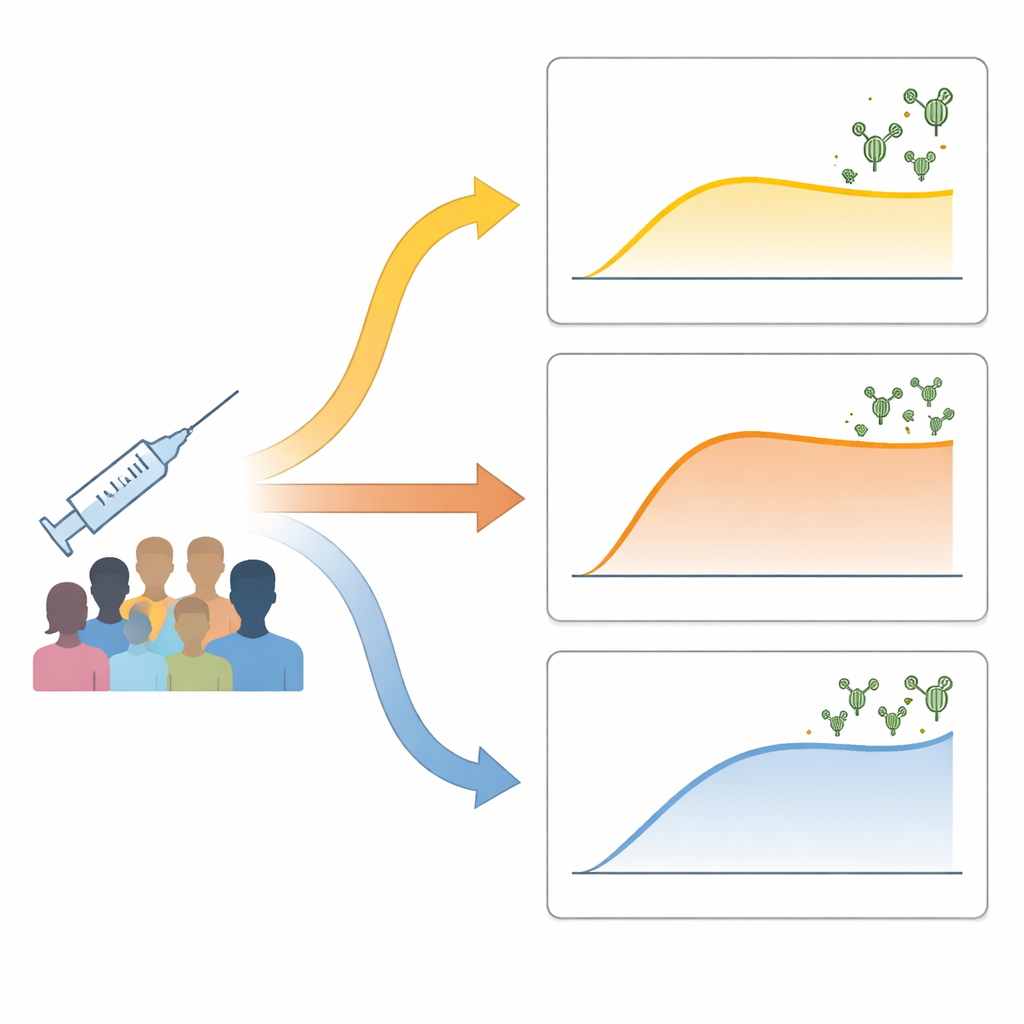
早期免疫活动如何塑造结局
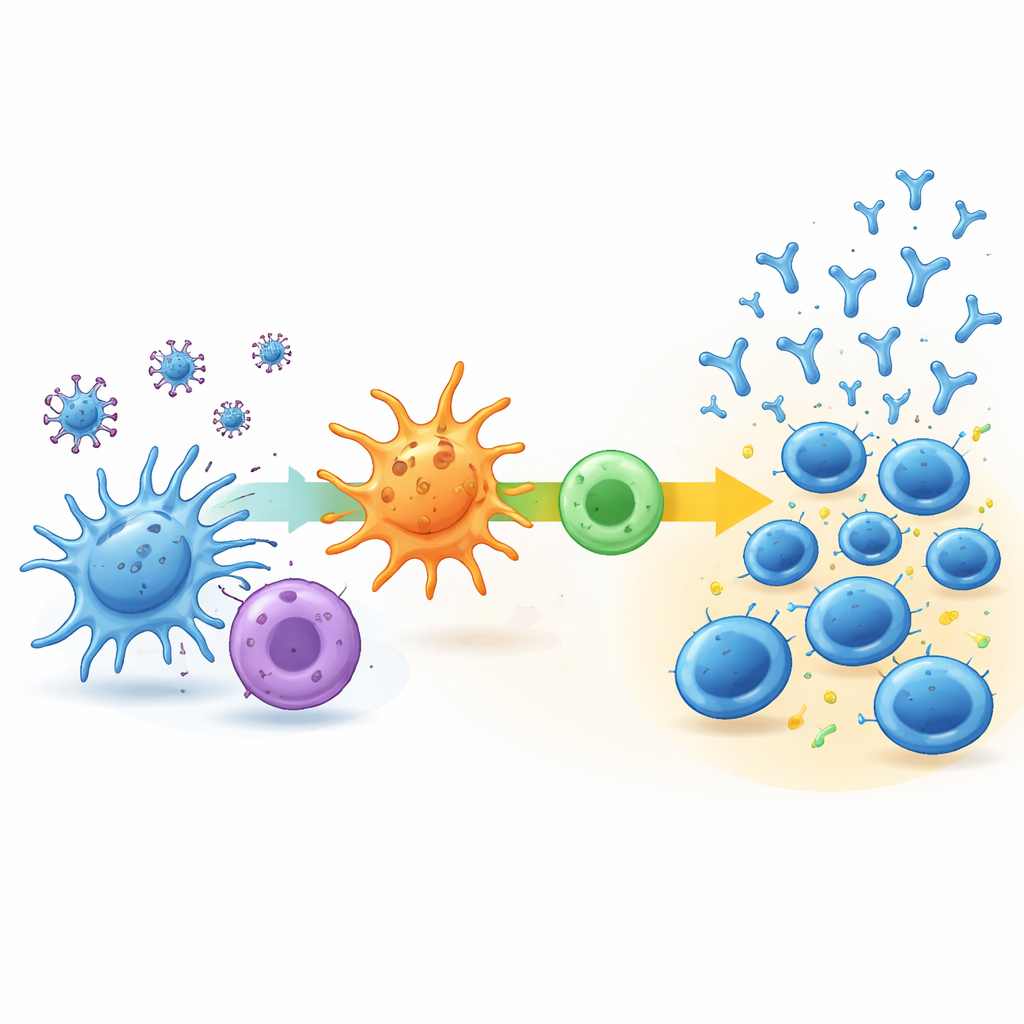
为探明驱动这些不同路径的因素,团队分析了在第二针前及其后一周血中免疫细胞的基因活性。在低-延迟组,变化很小:关键免疫通路几乎未被激活,血液中免疫细胞类型的组成大体保持不变。相比之下,快速-稳定组和持续上升组显示出明显的早期免疫激活信号。在反应最强的人群中,有一系列协调的通路活动,这些通路负责处理病毒片段、将其呈递给其他免疫细胞,并支持一种已知可促进抗体产生的辅助T细胞反应。这些受试者也倾向于拥有更多的未成熟B细胞和准备响应的辅助T细胞,随后表现出较强的病毒特异性T细胞活性。
RNA与B细胞中的隐含调控层
除了简单的基因开启或关闭变化外,科学家还研究了嵌入RNA中的更微妙的调控层——RNA是DNA与蛋白质之间的中间分子。在反应最强的组中,参与向免疫系统呈递病毒片段的免疫基因表现出不同的“剪接”模式和RNA末端更短的尾部区域。这些特征被认为有助于细胞更容易生成某些蛋白并维持强信号传导。团队还从相同的血样重建了B细胞受体库——抗体产生细胞上的独特“天线”。虽然总体多样性在各组间相似,但每种反应模式使用了略有不同的受体组合和构型,且最强反应者偏好以前与针对冠状病毒刺突蛋白的强效抗体相关的受体类型。
在接种前识别可能的低反应者
由于低-延迟组在标准接种方案后可能保护不足,研究人员探讨是否能在接种前将其识别出来。他们关注了一小组在基线时在最弱与最强反应者间存在适度差异的基因。利用机器学习方法,他们基于接种前仅测量的八个基因的活性建立了一个模型。该模型在他们的数据集中能够高准确度地区分低-延迟反应者,其中两种参与基础细胞信号传导和炎症的基因贡献了大部分预测能力。尽管这项工作需要在更大、更多样化的人群中验证,但它表明未来可能通过一次简单的血液检测来指导更个性化的疫苗方案。
对未来疫苗的意义
总体而言,这项研究表明,人们并非仅仅产生“强”或“弱”的抗体反应;他们沿着由早期、难以察觉的免疫事件塑造的不同时间轨迹发展。受保护最好的个体会启动协调的基因和细胞网络,帮助他们快速识别疫苗并构建持久的抗体,而低反应者则表现出较弱的早期反应。通过描绘这些内部差异并构建预测谁会反应不佳的工具,这项工作为个性化疫苗接种奠定了基础——例如为有风险的人群提供更早的加强针或替代配方——以便疫苗带来的益处能更均衡地分配。
引用: Wu, Q., Hu, H., Qin, L. et al. Refined phenotyping of vaccine responses reveals transcriptomic determinants of neutralizing antibody heterogeneity. npj Vaccines 11, 61 (2026). https://doi.org/10.1038/s41541-026-01386-z
关键词: 疫苗反应, 中和抗体, 新冠疫苗接种, 免疫异质性, 个性化疫苗