Clear Sky Science · zh
通过抑制 miR-126 克服血管小环境介导的急性髓性白血病对酪氨酸激酶抑制剂的耐药性
这对癌症患者为何重要
急性髓性白血病(AML)是最具侵袭性的血液恶性肿瘤之一,尽管有现代靶向药物,许多患者仍会复发。本研究提出了一个看似简单但影响深远的问题:问题是否不仅在于癌细胞本身,还在于它们在骨髓内所处的“邻里”环境?通过构建一个以实验数据为基础的详细计算模型,作者探讨了微小血管如何屏蔽白血病干细胞免受药物作用——以及阻断一种小型 RNA 信号如何可能瓦解这种防护。
骨髓中隐藏的安全屋
AML 起源于骨髓,恶性原始细胞挤占正常的造血。隐藏在这片细胞群中的是一小部分能自我更新并在治疗后存活的白血病干细胞,它们会播下复发的种子。这些干细胞并非自由漂浮;它们依附于围绕小动脉和毛细血管的专门“口袋”,统称为血管小环境。本研究聚焦于携带 FLT3‑ITD 突变的患者,其白血病细胞以酪氨酸激酶抑制剂(TKI)作为治疗。尽管这些药物能显著降低肿瘤负荷,许多患者仍然复发,这提示一些细胞被隐藏或受到保护。
双面作用的治疗效应
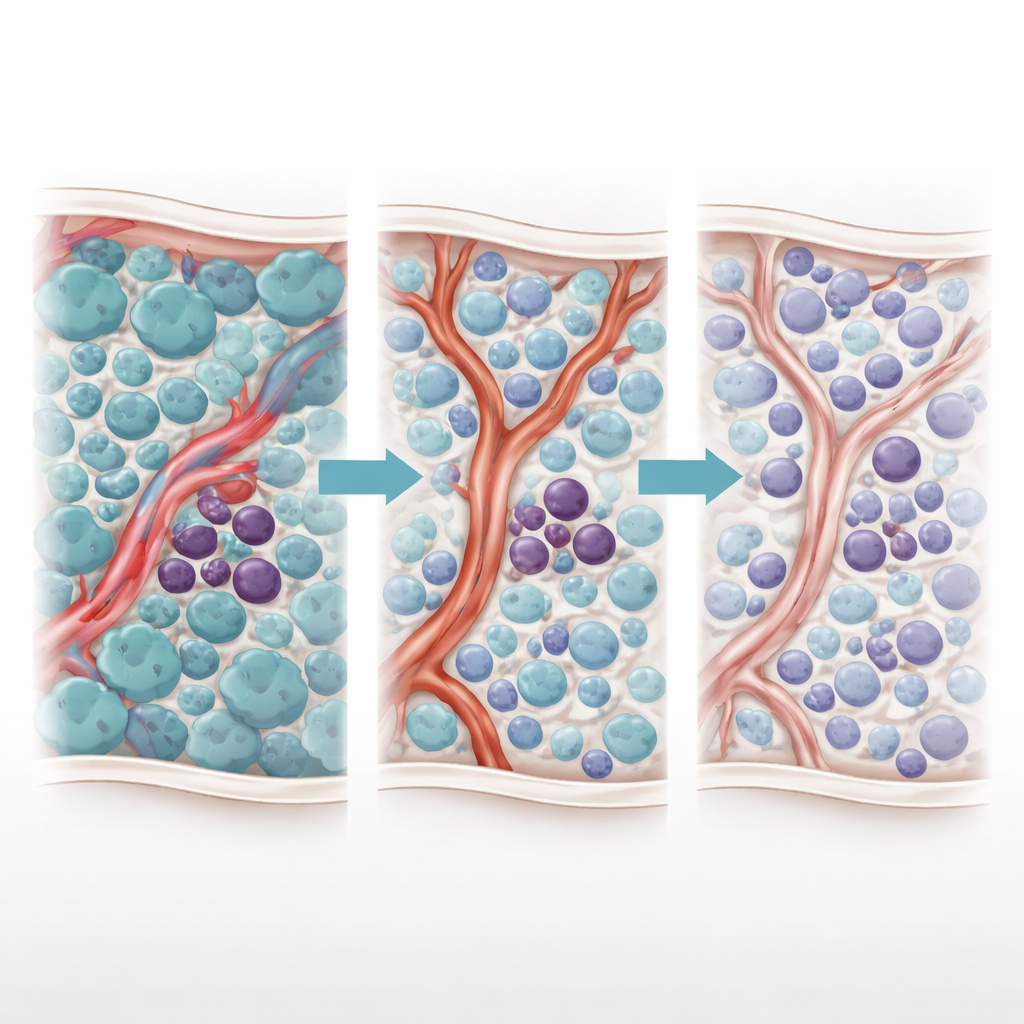
作者此前发现了一个令人费解的“双面现象”——对 TKI 治疗的两面反应。当 TKI 杀死快速分裂的原始细胞时,一种炎性分子 TNF‑α 的水平下降。出乎意料的是,这种下降使附近的血管内皮细胞提高了对一种称为 miR‑126 的小调控 RNA 的产生。该 miR‑126 从内皮细胞传递到白血病干细胞,使其转入静默、非分裂状态,从而高度耐药。换言之,清除大多数癌细胞的治疗会重塑骨髓,使最危险的细胞得以藏匿。
构建虚拟骨髓
为了解剖这一动态过程,团队建立了一个基于个体代理的 AML 骨髓计算模型。每一个关键角色——原始细胞、白血病干细胞和衬里血管的内皮细胞——都作为遵循生物学规则的“代理”单独表示。扩散分子如 TNF‑α、miR‑126、TKI(AC220)以及一种名为 miRisten 的 miR‑126 抑制药在模拟组织中传播。该模型用小鼠成像数据进行校准,映射真实的血管格局,包括富含或缺乏 miR‑126 产生血管的区域。在模拟中,标准 TKI 治疗可靠地重现了双面效应:原始细胞减少,TNF‑α 下降,血管来源的 miR‑126 激增,干细胞撤入保护性小环境,疾病随后反弹。
通过精准时机关闭护盾
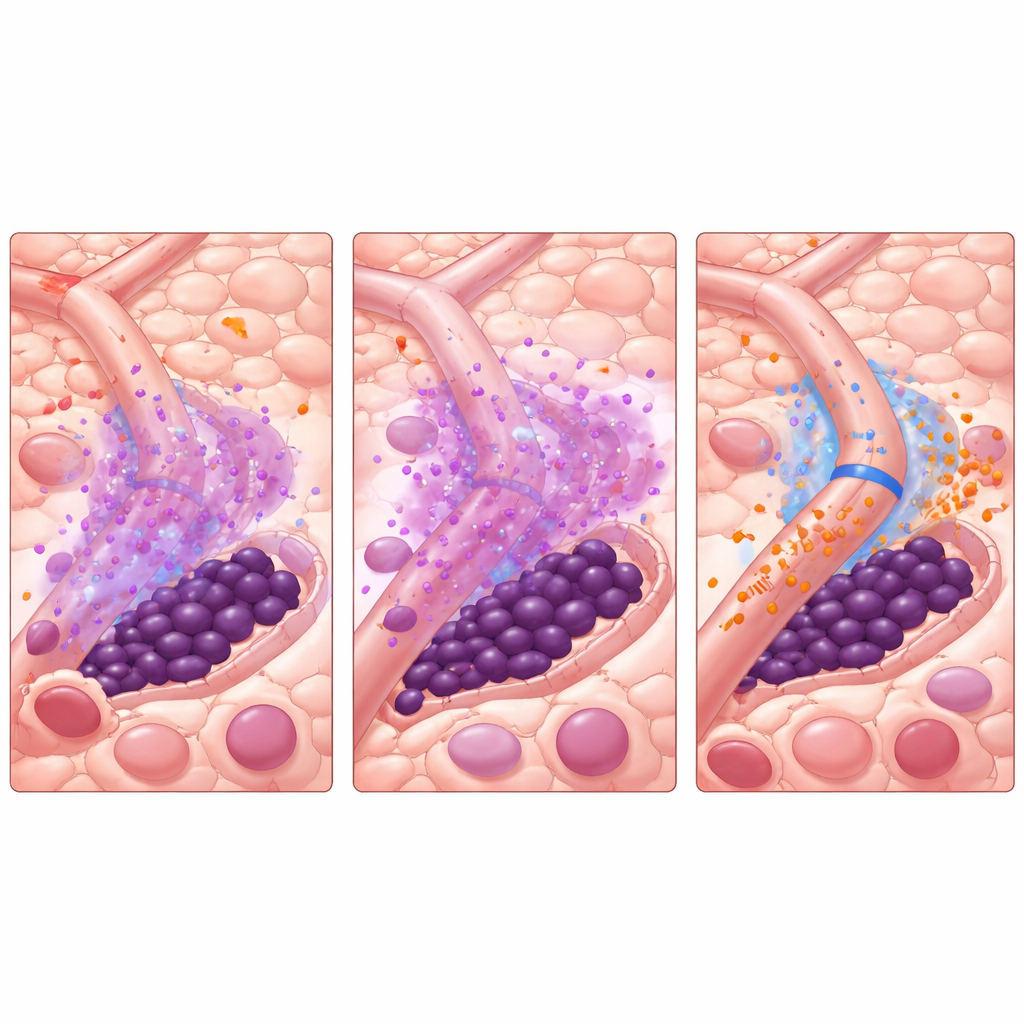
借助这个虚拟系统,研究者测试了打破恶性循环的方法。与 TKI 同时加入 miRisten 虽然有帮助,但在模型中很少能治愈疾病。一种更具策略性的做法更为有效:短期“预处理”单独使用 miRisten 以抑制血管 miR‑126,然后再给予单用 TKI 或继续联合治疗。在多种模拟血管布局中,即便在开始 AC220 之前仅进行几天的 miRisten 预处理,也能显著减少或消除复发,同时限制总体药物暴露。模型还显示,白血病干细胞与血管的距离强烈影响其命运——紧贴血管的细胞获得的保护最多,除非阻断了 miR‑126。
这对未来治疗可能意味着什么
简言之,这项研究表明,一些白血病干细胞的存活并非因为 TKI 无效,而是因为骨髓内的小血管在治疗期间短暂转为“保护者”模式。通过在给予 TKI 之前短暂关闭单一信号 miR‑126,可能有望剥除这一护盾,迫使干细胞现身并使其可被现有药物清除。虽然此工作基于与实验数据挂钩的计算模拟,尚未进入临床试验,但它提出了一个具体策略:在标准治疗之前及期间安排针对微环境的药物。如果得到验证,这一方法不仅可能改善携带 FLT3 突变的 AML 患者的预后,也可能启发在其他血液或实体肿瘤中采用类似战术——这些肿瘤同样依赖周围环境来躲避治疗。
引用: Froid, M., Branciamore, S., Chen, Z. et al. Overcoming vascular niche–mediated TKI resistance in acute myeloid leukemia through miR-126 inhibition. npj Syst Biol Appl 12, 38 (2026). https://doi.org/10.1038/s41540-026-00675-6
关键词: 急性髓性白血病, 白血病干细胞, 骨髓微环境, 酪氨酸激酶抑制剂耐药, miR-126 抑制