Clear Sky Science · zh
深度学习模型识别阿尔茨海默病进程中的大脑变化
为什么追踪大脑随时间的变化很重要
阿尔茨海默病会逐步剥夺人们的记忆和思维能力,但大脑内的损伤在日常症状明显出现之前就会积累多年。医生通常依赖单次脑扫描或一次检测结果来判断某人是否患有阿尔茨海默病,尽管该疾病是随时间展开的。这项研究提出了一个简单但后果重大的问题:如果我们在数年间追踪受试者的脑部影像,并让先进的计算模型从这些变化中学习,能否不仅更准确地检测阿尔茨海默病,还能看出哪些脑区最先和最严重地受累?
追踪大脑的演变,而不仅仅是抓取快照
研究者使用了结构性 MRI 扫描,它能显示详细的大脑解剖结构,样本来自 280 多名老年人,包括阿尔茨海默病患者和认知正常的同龄人。关键在于,每个人都有大约相隔一年的三次扫描,使团队能够在两年内追踪脑组织如何变化。研究不是将每次扫描视为独立的图像,而是构建了一个将所有时间点一起输入的深度学习模型。该模型被设计为关注灰质(富含神经元细胞体的大脑组织)、白质和脑脊液,并学习这些组织中模式随疾病进展而如何变化。
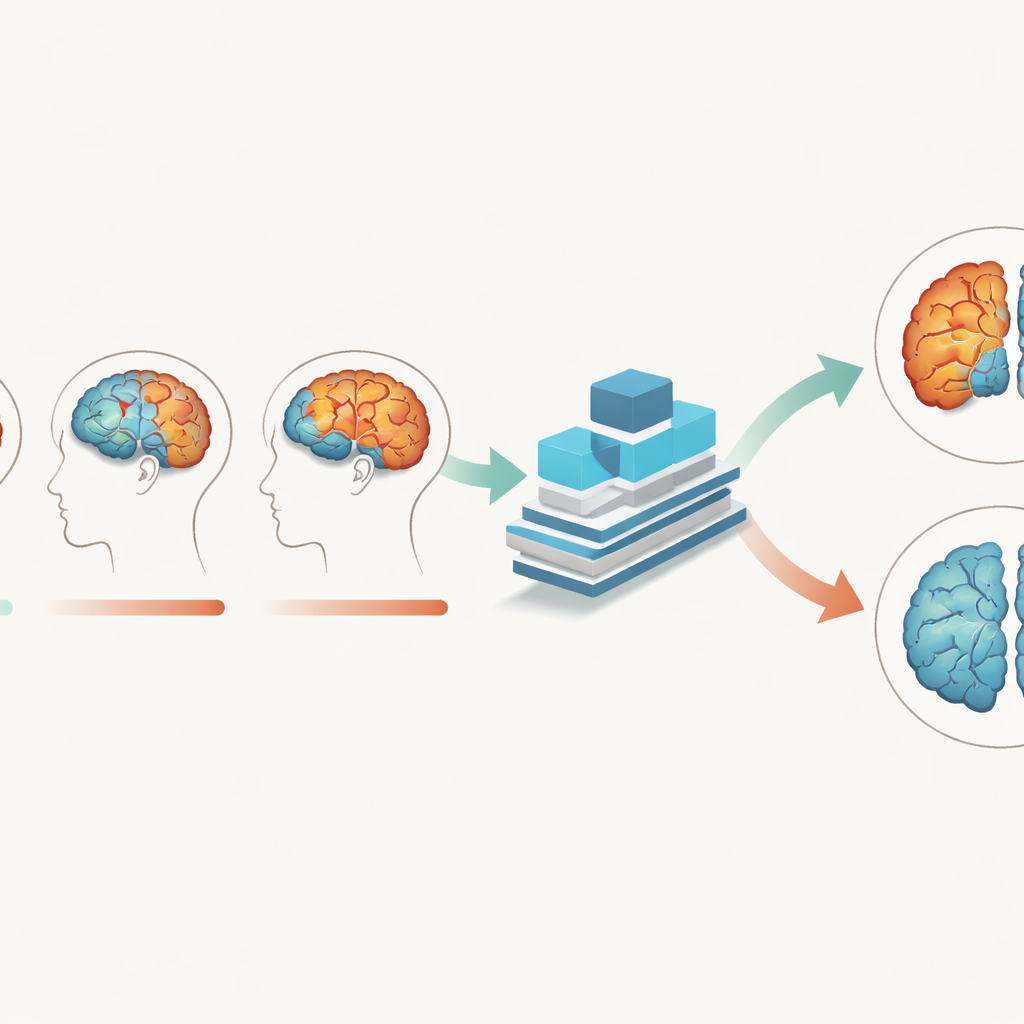
针对大脑节律调校的深度学习模型
为了捕捉这些微妙变化,团队创建了多分支融合通道注意力网络(Multi-Branch Fusion Channel Attention Network),这是一种处理 MRI 体积数据而非二维图像的 3D 卷积神经网络。不同分支分别处理不同组织或不同时间点的数据,然后融合它们的信息,同时“注意力”机制帮助模型在三维空间中聚焦最有信息量的区域。该网络主要在灰质数据上训练,学会以约 93% 的准确率并在一个数据集上达到完全特异性区分阿尔茨海默病大脑与正常老化大脑,优于若干现有的 AI 方法。它在一个独立的澳大利亚数据集上也表现良好,表明模型并非简单记住单一研究的特征,而是捕捉到更广泛的疾病信号。
看清哪些脑区左右局面
单有高准确率对医学来说还不够;临床医生需要理解驱动模型决策的因素。因此研究者采用了一种可解释性技术 SHAP,为 MRI 中的每个三维微小像素(即体素)分配重要性分数。将这些体素按解剖区域分组后,展现出疾病的动态图景。早期,杏仁核——一个与情绪和记忆相关的区域——在将患者与健康同龄人区分开时显得尤为重要。随着时间推移,海马、海马旁回,尤其是颞叶后部的影响力上升,而杏仁核的相对作用减弱。到两年时点,患者与对照组之间的差异更加明显并呈聚集状,尤其在大脑左侧。
与症状和临床评分相符的模式
为了验证模型关注的区域是否与生物学一致,团队进行了传统的大脑体积分析和统计检验。他们发现这些突出区域的灰质在阿尔茨海默病患者中萎缩得比正常老化者更快,而且这些区域较低的体积与常用认知测试(如简短智能状态检查量表 MMSE 和临床痴呆评分 CDR)较差的分数密切相关。损伤从内侧颞叶结构向外扩展到后部语言和联合区的路径,与阿尔茨海默病的经典病理分期方案相呼应。同样出现了左侧偏向,这与大脑在语言和某些记忆功能上的左侧优势一致。基于体素的形态学分析显示,早期变化分散且较小,随着疾病进展,在后颞叶和额叶区域变得更大且更集中。
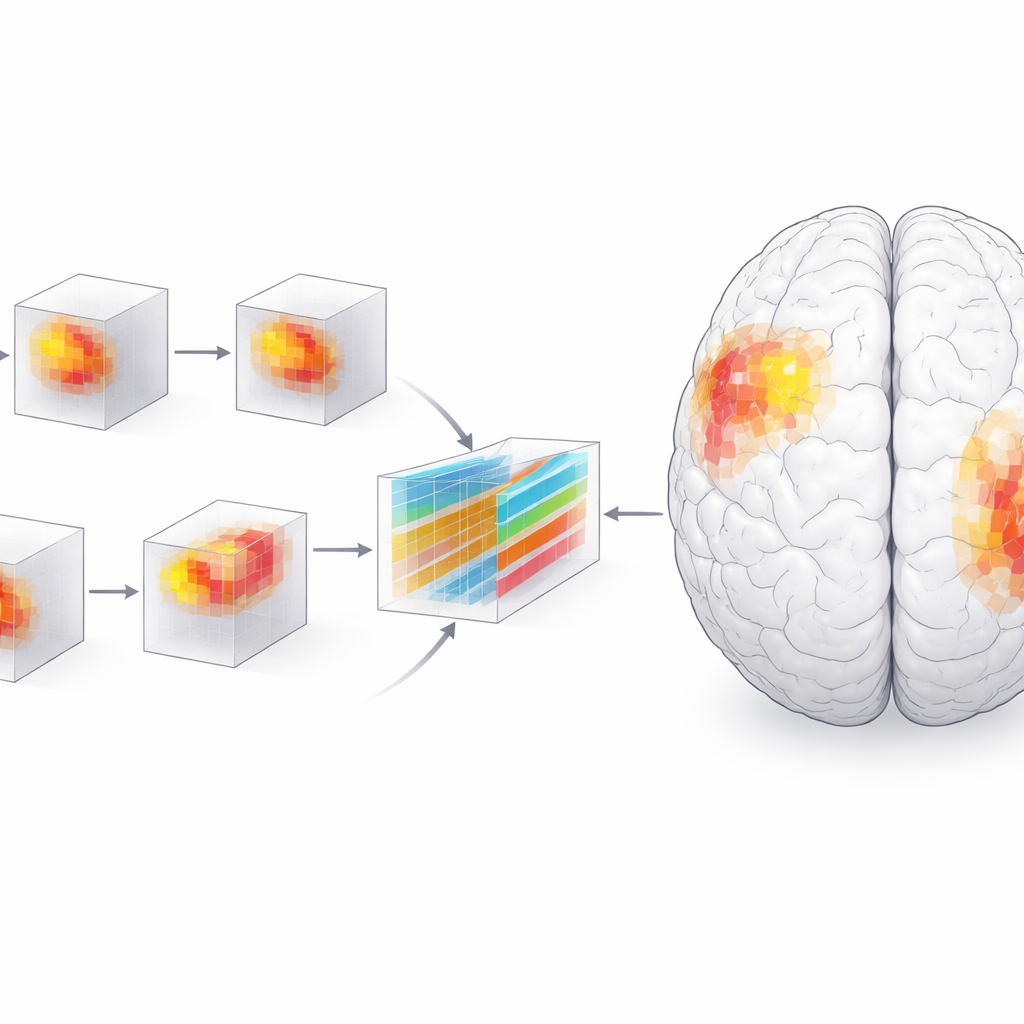
这对患者和医生意味着什么
对非专业读者来说,关键结论是阿尔茨海默病并非在大脑中表现为简单的开关式变化;它沿着有序但加速的路径发展,随时间留下明显的痕迹。通过教会深度学习模型不仅识别大脑哪里不同,而且识别这些差异在数年内如何增长,本研究提供了一种在更早期、更准确地识别阿尔茨海默病的方法。研究还定位出一小组与认知衰退密切相关的脑区——包括杏仁核、海马、海马旁回和后部颞皮质——其体积和结构的变化尤为关键。尽管仍需更多工作,尤其是结合更多成像手段和更大样本的数据集,但这种方法使我们更接近将时间分辨的脑扫描和可解释的人工智能作为早期诊断、监测并最终指导针对阿尔茨海默病干预的实用工具。
引用: Sun, J., Han, JD.J. & Chen, W. Deep learning models identify brain changes during the progression of Alzheimer’s disease. npj Syst Biol Appl 12, 42 (2026). https://doi.org/10.1038/s41540-026-00666-7
关键词: 阿尔茨海默病, 大脑 MRI, 深度学习, 纵向影像学, 神经退行性变