Clear Sky Science · zh
严重大鼠复喂综合征模型的建立及相关低磷血症的数学建模
为何再次进食可能危险
当长期严重营养不良的人最终开始进食或接受静脉营养时,医生必须小心行事。突然大量的热量输入可能引发“复喂综合征”,一种会扰乱体内电解质并损害心脏、肌肉和肺的并发症。磷是其中的关键角色——它是每个细胞获得能量所必需的矿物质。该研究使用大鼠和计算机建模来揭示为何复喂期间血中磷浓度会剧烈下降,以及我们如何更好地预防这种危险的下跌。
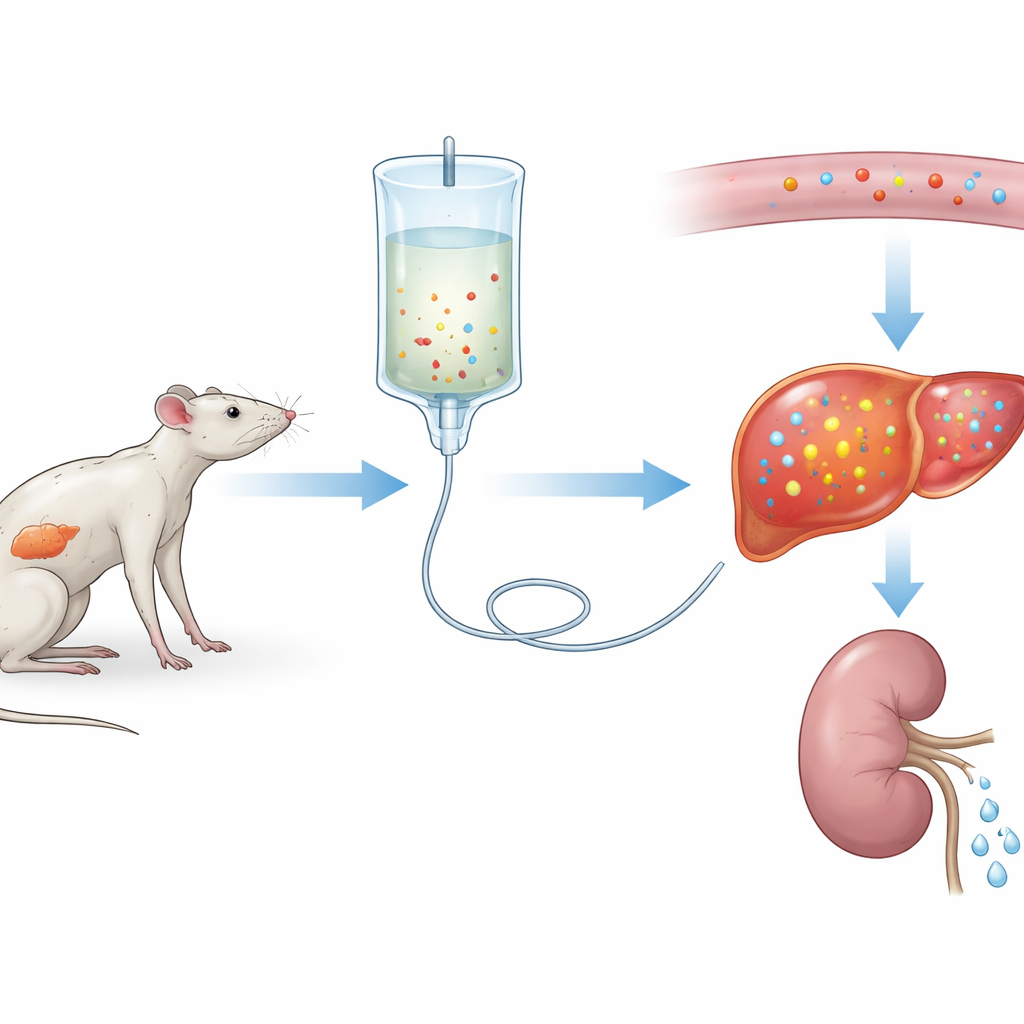
仔细审视复喂问题
研究人员首先在大鼠中建立了严重的复喂综合征模型。三周内,一组大鼠进食正常饮食,而另一组摄入极少蛋白质,以模拟长期营养不良。随后两组均接受相同的静脉营养持续三天。低蛋白组的大鼠出现了血磷陡降——约 75% 的下降——同时伴随其他电解质的变化和器官损伤迹象,尤其是肝脏和肌肉。这些变化类似于患者中的严重复喂综合征,表明研究团队构建了一个可信的实验模型。
复喂期间磷发生了什么
为了解磷在体内随时间的流动,科学家对同一只大鼠反复采血和采尿。他们发现,开始喂养后正常和蛋白质缺乏的动物血磷均下降,但在营养不良组下降更深且持续时间更长。令人意外的是,肾脏在复喂后立即减少了尿中磷的流失,因此并非磷被排出体外。相反,磷正被从血液拉入组织,特别是肝脏——其储备在数周不良饮食中已被耗尽。计算机计算证实,营养不良大鼠细胞内起始磷含量远低于正常大鼠,营养到来后细胞积极地大量吸收磷。
胰岛素并非全部答案
因为复喂会升高血糖和激素胰岛素,临床上长期将磷进入细胞归咎于胰岛素。研究团队通过抑制胰岛素分泌的激素生长抑素来检验这一观点。正如预期,血糖升高,但血磷的骤降几乎没有改善。与此同时,自由氨基酸——蛋白质的构件——水平上升。在另一项独立实验中,科学家从输液中去除了氨基酸。此时,磷水平保持得更稳定,严重下降被阻止,尽管胰岛素水平相似。这些结果表明是一个联合效应:胰岛素与氨基酸共同作用,而非仅胰岛素,促使细胞在复喂时大量摄取磷。
肝脏与肾脏中的隐藏控制网络
进一步挖掘时,研究人员检查了参与营养感知的肝脏蛋白,重点关注被称为 mTOR 的通路,该通路对胰岛素和氨基酸有反应。在低蛋白大鼠中,复喂强烈激活了该通路,并增加了一种名为 Pit2 的磷转运蛋白的水平,这有助于肝细胞摄取磷。这一模式与他们数学模型的预测相符,该模型将该网络打包为一个他们称之为“simTOR”的单一控制信号。模型还需要一个独立的反馈因子来解释肾脏如何调整尿中磷的丢失。来自骨源激素 FGF-23 的测量很好地符合这一角色:其水平在开始喂养时骤降,限制了磷的排泄,随后在正常与营养不良大鼠间出现分化,这种分化与模拟的反馈信号相吻合。
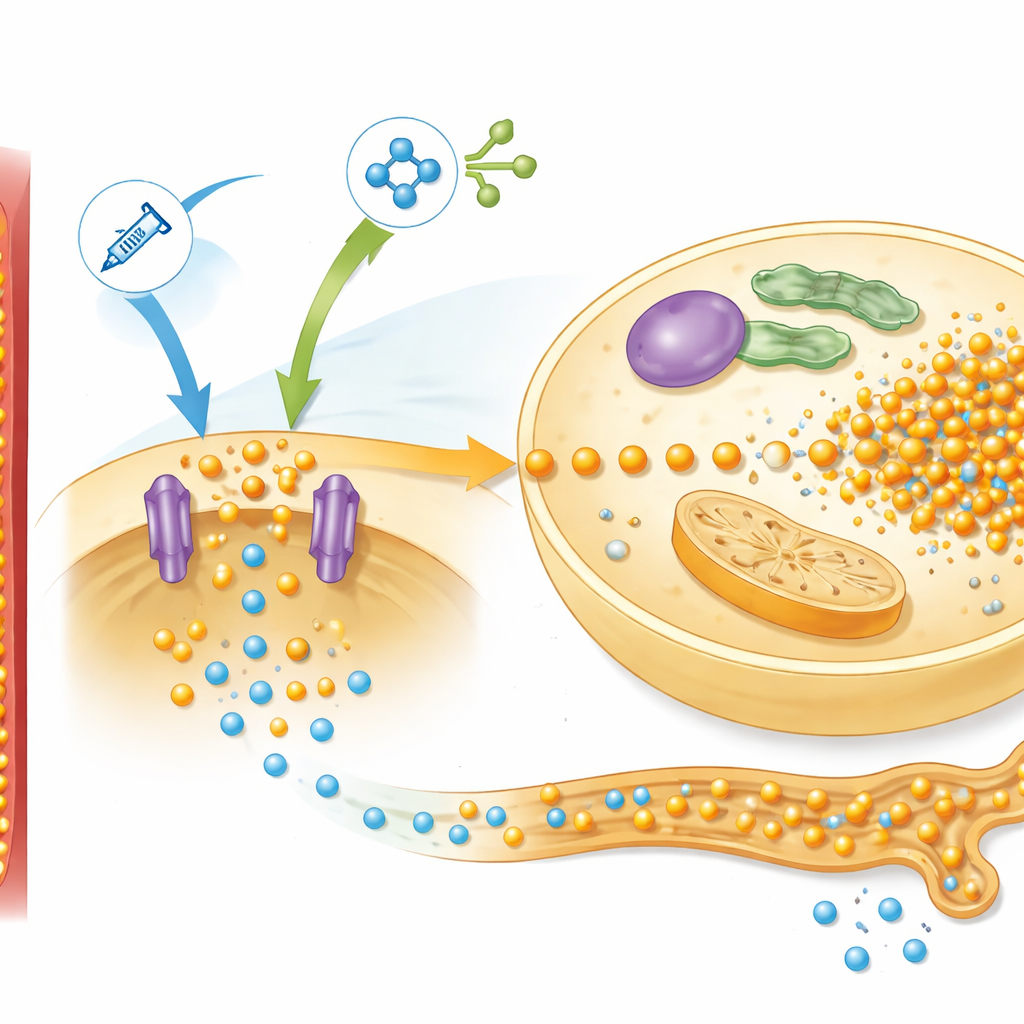
用数学检验预防策略
通过调节计算机模型中的不同参数,作者能够提出难以或具有风险直接在患者中测试的“如果……会怎样”的问题。分析凸显了影响磷下降深度及恢复速度的三大因素:细胞内初始磷含量、mTOR 驱动的摄取系统强度以及营养中磷的摄入速率。模拟表明,在复喂时直接添加大量磷酸盐难以安全平衡。然而,在复喂前补充额外磷——让器官悄然重建其细胞内储备——可以减轻随后血磷的剧烈下跌。减少氨基酸负荷,特别是那些强烈激活 mTOR 和胰岛素的氨基酸,在动物实验中也显示出保护作用。
对患者的意义
对于处于复喂综合征风险的人群——例如长期进食障碍或严重虚弱者——这项工作表明危险不仅来自血糖的短时升高。饥饿的器官在复喂时进入时细胞内的磷储备已耗尽,然后在胰岛素与氨基酸的共同推动下迅速从血液中吸收矿物质,而肾脏在短时间内则减少磷的排出。其结果是循环系统中出现急剧的、短暂的缺乏,可损害重要组织。这里建立的大鼠模型和数学框架指向更有针对性的预防措施:谨慎且及早使用磷补充、对富含氨基酸的营养进行仔细控制,以及关注调节肾脏排磷的激素。综合这些方法,可能帮助临床医生更安全地喂养易受损的患者。
引用: Kato, H., Yamaoka, I. & Kubota, H. Development of a severe rat refeeding syndrome model and mathematical modeling of the associated hypophosphatemia. npj Syst Biol Appl 12, 34 (2026). https://doi.org/10.1038/s41540-026-00658-7
关键词: 复喂综合征, 低磷血症, 磷代谢, mTOR 信号通路, 肠外营养