Clear Sky Science · zh
空间FBA揭示肾脏肿瘤中异质的沃伯格生态位及结直肠癌中的乳酸消耗
为何肿瘤代谢的空间分布重要
即便在同一肿瘤内,癌细胞的行为也并非一致。有些靠近血管,有些位于供养不足的深层区域,而这些位置会影响它们如何获取和利用燃料。本研究提出了一种新方法,从先进的空间基因表达数据中读取隐藏的“代谢地图”。通过这种方法,作者发现了肿瘤处理关键分子乳酸的意外模式,挑战了肿瘤只将乳酸作为废物排出的传统看法。
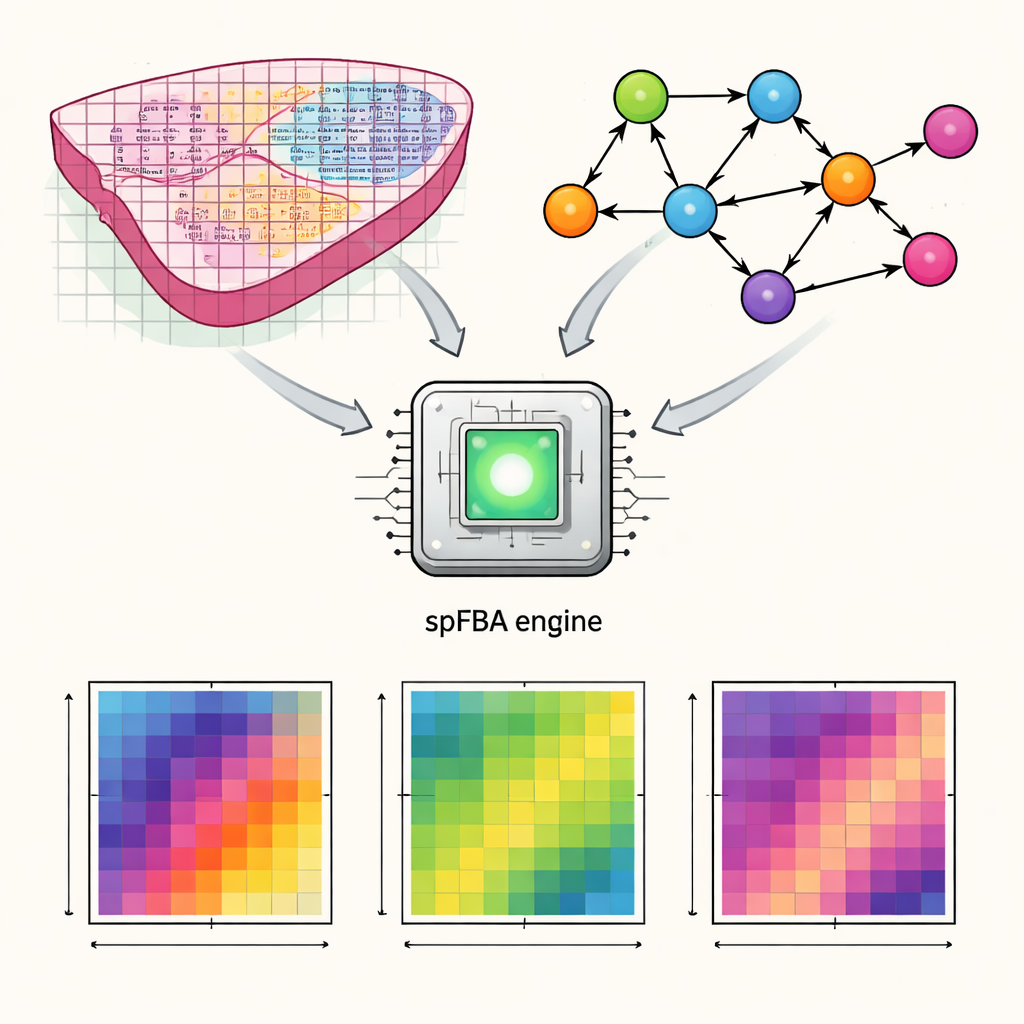
把基因图谱转化为代谢活性
作者开发了一个名为空间通量平衡分析(spFBA)的计算框架。空间转录组技术在组织薄片的成千上万个微小点位上测量哪些基因在活跃。spFBA将这些空间基因活性图与详尽的人体代谢模型相结合,代谢模型描述了葡萄糖、氧气和氨基酸等营养物质在细胞内如何被转化。spFBA并不假定组织的每个区域具有相同的代谢目标,而是将每个点位独立处理,在化学和质量守恒定律下探索该处可能的反应模式。输出是一组“通量富集评分”,指示在每个位置不同代谢反应可能的流向与强度。
在肾脏肿瘤上验证方法
为检验spFBA是否产生生物学上合理的结果,团队首先研究了透明细胞肾细胞癌,这是一种以高度依赖糖酵解和乳酸释放(即沃伯格效应)著称的肾癌。使用来自十个肾脏肿瘤样本的公开空间数据,他们检查了预测的代谢模式是否与组织已知结构相符。结果显示,按推断通量分组的点位与显微镜下的组织学结构以及仅基于基因表达的聚类高度一致。重要的是,spFBA重现了肿瘤与正常肾组织之间预期的代谢对比:肿瘤区域表现出更高的葡萄糖使用、增强的生物质生成(细胞生长的替代指标)以及强烈的乳酸分泌。同时,氧气的利用仍然显著,表明同一肿瘤的不同部位可根据局部血供在发酵与呼吸之间混合使用。
结直肠癌呈现不同的乳酸图景
研究者随后将相同流程应用于来自一例原发结直肠癌及其配对肝转移的高分辨率空间数据集,以及另一个使用不同技术生成的公开结直肠数据集。结果截然不同。多数结直肠癌区域——无论是原发肿瘤还是肝转移——被预测为从周围环境摄取乳酸,而非将其作为废物排出。邻近支持组织中的间质细胞倾向于释放少量乳酸,而肿瘤细胞则表现为强烈的乳酸消耗者。通过追踪反应级别的通量模式,作者展示这些转移细胞并非简单在粒线体内按常规能量代谢回路燃烧乳酸;相反,它们将乳酸转化为进入脂类及其他合成通路的构建块,用于细胞生长,这是一种“拟逆向沃伯格效应”,即乳酸被用作生物合成的原料。
代谢生态位与肿瘤-间质边界
由于spFBA保留了空间布局,它可以精确定位特定代谢交换发生的位置。在肾脏肿瘤中,该方法揭示了并存的代谢“邻域”:氧供较好、血液充足的界面区域癌细胞既进行呼吸又进行发酵,而更深、血管稀少的核心则更依赖发酵。在结直肠肝转移中,spFBA突出显示肿瘤与间质交界处的鲜明对比,谷氨酸和乳酸的处理方向发生改变,提示侵袭前沿存在强烈的交换。在所有数据集中,预测的与生长相关的通量与基于基因的独立增殖测量相关,支持模型的生物学现实性。关键在于,同一算法在肾癌中预测乳酸分泌而在结直肠癌中预测乳酸摄取,表明观测到的差异源自数据本身,而非模型的内在偏差。
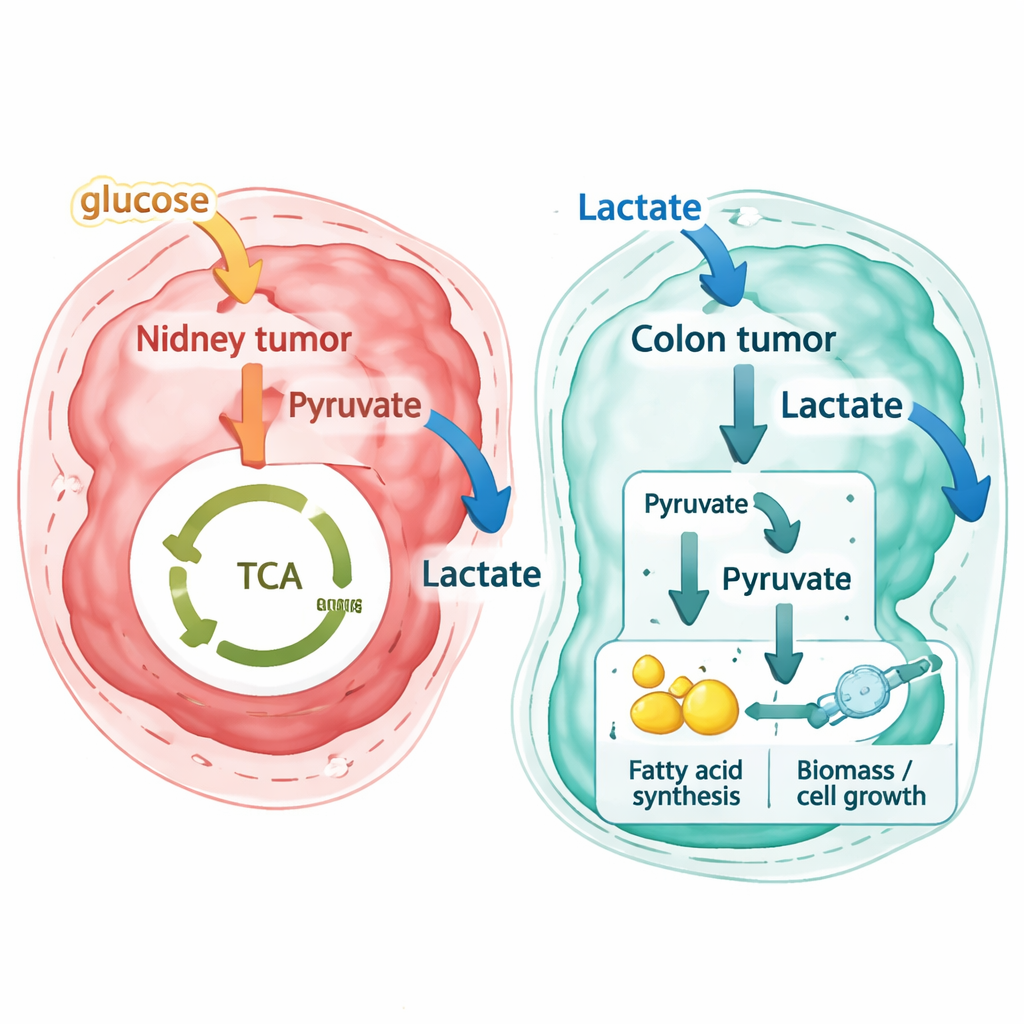
这对理解和治疗癌症意味着什么
给非专业读者的要点是:癌症代谢不仅异常,而且高度具有空间特异性。同一肿瘤内部可以存在多种代谢生态位,而不同器官中外观相似的肿瘤可能以相反的方式使用相同分子。这项工作表明,通过将空间基因表达与详细的代谢模型叠加,研究者可以推断肿瘤在哪些位置可能对特定营养物质(如乳酸)有较强需求。在结直肠癌中,发现肿瘤细胞大量消耗乳酸并将其引入与生长相关的合成过程,提出了关于饮食、肠道微生物以及肝脏自身代谢如何影响疾病进展的新问题,并且提示阻断乳酸利用是否能使这些肿瘤对治疗更脆弱的值得进一步探索。
引用: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
关键词: 癌症代谢, 空间转录组学, 乳酸, 沃伯格效应, 结直肠癌