Clear Sky Science · zh
动力学网络分析揭示pMHC界面上突出的长程残基耦合,解释增强的免疫原性
微小的病毒片段如何引导我们的免疫防线
我们的杀伤性T细胞在体内巡逻,寻找感染或癌变的迹象。它们通过扫描暴露在细胞表面的微小蛋白片段(称为肽),这些肽由称为MHC I类的分子呈递。本文探讨了一个细微却重要的问题:为什么单个肽中一个小小的变化能让T细胞的反应大幅增强——或完全丧失?答案不仅关乎静态结构,还涉及整个分子组装随时间运动和弯曲的方式。
锁、钥匙与可动部件
理解这项工作有助于把肽–MHC(pMHC)复合体想象成一把锁,而T细胞受体(TCR)是钥匙。肽位于MHC分子的一个沟槽中,二者共同形成TCR探测的表面。先前研究表明,肽的精确序列和特定的MHC变体都会显著影响T细胞是否被激活。科学家们也设计了“改变肽配体”,通过小的改动来调节免疫反应,包括用于癌症免疫疗法。不过,尽管我们对这些复合体的静态形状了解较多,却对肽上一处的运动如何影响TCR实际结合的远端界面知之甚少。
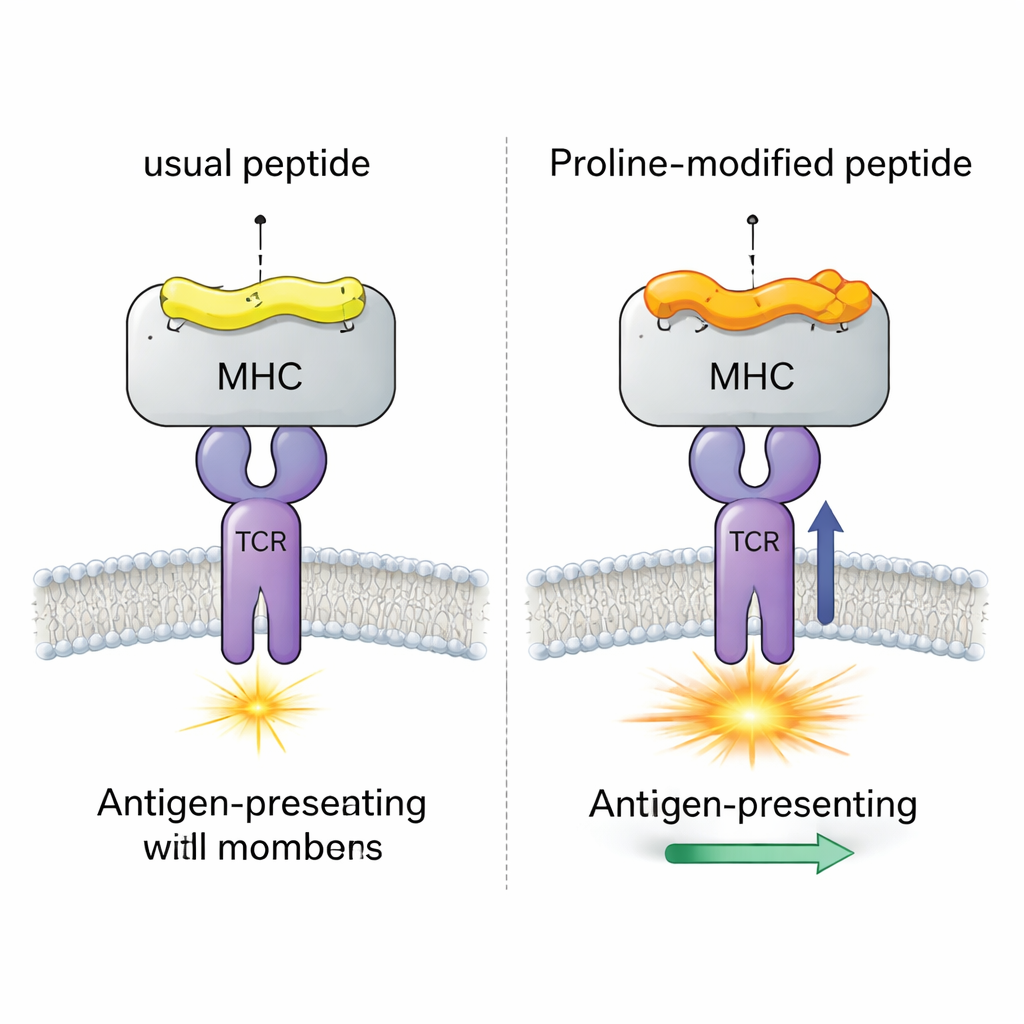
四种几乎相同肽的病毒实验证例
研究团队聚焦于一个研究充分的小鼠病毒(LCMV)体系,涉及肽gp33,该肽通常会触发强烈的CD8+ T细胞反应。他们比较了与同一MHC分子(H-2Db)结合的四种密切相关的肽变体。其一为原始病毒肽;另一种带有使T细胞几乎无法识别的免疫逃逸突变;还有两种是“脯氨酸改造”疫苗候选物,其中肽靠近N端的一个氨基酸被替换为脯氨酸。早期实验证明,这种脯氨酸替换提高了肽–MHC复合体的稳定性并增强了模型TCR(称为P14)的反应,但其具体机制尚不清楚。
观察分子的抖动:模拟与晶体学相结合
为揭示真实发生的过程,作者将高分辨率晶体结构与对每个pMHC复合体进行的长时间、逐原子计算机模拟相结合。他们检查了每个氨基酸残基随时间的波动程度,以及当肽的第三位被转换为脯氨酸时这些波动如何变化。通过对大量配对模拟中运动模式的相关性分析,他们构建了一个“动力学地图”,显示了哪些残基会共同运动,即使它们在空间上相距甚远。随后他们将该地图转化为网络,其中每个残基为节点,边表示统计学上关联的运动,并使用类似社交网络分析的图论工具对该网络进行分析。
免疫锁内的长程通讯
核心发现是,将肽的第三位改为脯氨酸不仅仅是局部变得更僵硬。它改变了沿着构成肽结合沟槽一侧的MHC螺旋传递运动的方式。这反过来影响了另一个肽残基(第六位)的行为,该残基位于TCR接触面正下方,对识别至关重要。在“有效”的脯氨酸改造版本中,该残基采样更广泛的构象范围,包含对TCR结合有利的构象。在不含脯氨酸的免疫逃逸变体中,该残基更受限制,很少采用有利于TCR的取向。网络分析显示,这种影响通过MHC沟槽中具体的氨基酸传递,形成一条动态耦合残基链,将脯氨酸变化的位置与TCR接触区连接起来。
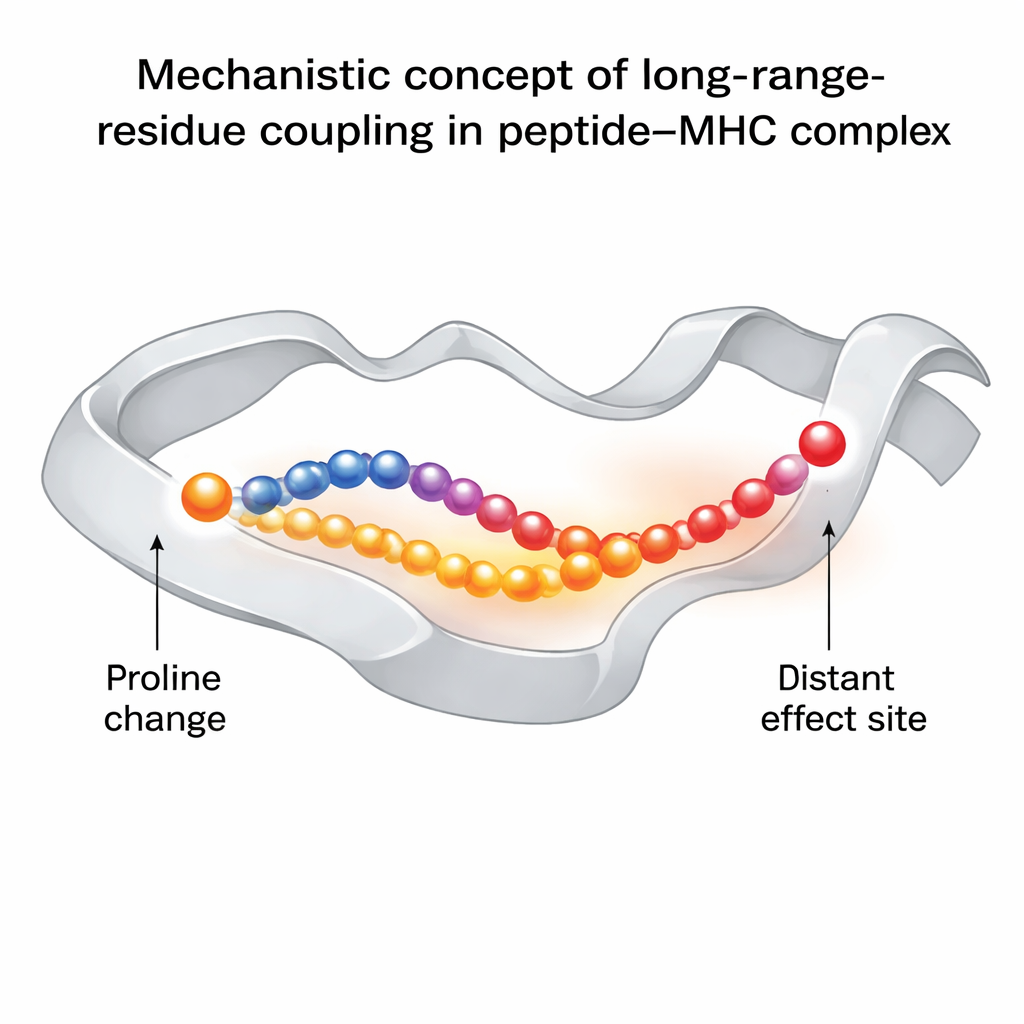
这对疫苗和免疫治疗的意义
这些结果表明,免疫原性——肽激活T细胞的强度——不仅关乎某一瞬间形状的匹配,还关乎复合体随时间呼吸和弯曲的方式。一个位点的细微变化可以通过分子网络产生涟漪,使关键接触残基更可能呈现出与TCR兼容的构象。作者提出的计算工作流程提供了一种系统检测此类长程耦合的方法,可为疫苗和癌症治疗中改变肽的设计提供指导。简而言之,他们展示了通过仔细选择修饰肽的位置,可以将整把“锁”调整到更容易被免疫系统“钥匙”打开的动态状态。
引用: Resink, T., Sala, B.M., Sun, R. et al. Dynamical network analysis reveals long-range residue couplings at the pMHC interface underlying enhanced immunogenicity. npj Syst Biol Appl 12, 15 (2026). https://doi.org/10.1038/s41540-026-00653-y
关键词: T细胞识别, 肽 MHC, 蛋白质动力学, 改变肽配体, 免疫原性