Clear Sky Science · zh
利用计算模型模拟前肠内胚层向肺上皮祖细胞分化
将干细胞转变为构建肺组织的细胞
科学家正在研究如何诱导患者自身的干细胞成为可替代的肺组织,这在将来有望修复慢性阻塞性肺病、纤维化或严重感染等疾病造成的损伤。本文探讨研究人员如何利用计算建模来绘制并微调这一路径中的关键步骤:将一种中间细胞类型——前肠内胚层,转化为早期肺上皮祖细胞——这些是可以最终形成气道和肺泡的起始细胞。
为何肺的起始细胞重要
人类诱导多能干细胞(iPSC)可以从成人组织重编程得到,然后被引导分化为多种器官细胞。要构建肺组织,这些细胞首先要经过若干发育节点。其中之一是前肠内胚层——胚胎期通常会发育为呼吸和消化系统部分的细胞层。在适当的化学信号作用下,这些细胞可以成为携带早期肺标记的肺上皮祖细胞,随后成熟为专门的气道或肺泡细胞。由于未来的细胞疗法将需要数十亿甚至更多这样的细胞,研究人员需要可靠的方法来提高产量并将方案适配不同患者的细胞系,而不是在实验室中进行无休止的试错。
构建细胞分化的虚拟模型
该团队扩展了先前的数学框架,构建了他们所知的第一个用于描述前肠内胚层向肺祖细胞这一特定转变的人群水平模型。他们考虑了两种表示细胞的方法:一种简单版本仅跟踪存活细胞的总数,另一种更详细的版本则分别追踪前肠细胞和肺祖细胞。在两种情形下,模型还跟踪培养基中的葡萄糖和乳酸,代表营养物和代谢废物。利用系统生物学的工具,研究者构建了多个候选方程来描述细胞如何增殖、死亡和分化,然后使用可辨识性测试剔除了那些即便在理想数据下也无法确定参数的模型。
用模型设计更聪明的实验
研究者没有仅仅拟合现有数据,而是让模型来指导如何开展新的实验。他们使用模拟数据评估需要多频繁测量细胞数量和营养水平才能精确估计模型参数,在统计精度与频繁取样带来的成本和劳动之间权衡。由此产生了一个切实可行的计划:每天测量葡萄糖和乳酸,并每一到两天进行一次细胞计数,在四种条件下比较——这些条件改变了第10天的传代强度以及是否每天更新培养基。随后他们开展了这些实验,既测量总细胞数,又通过流式细胞术测定仍为前肠细胞或已成为肺祖细胞的比例。
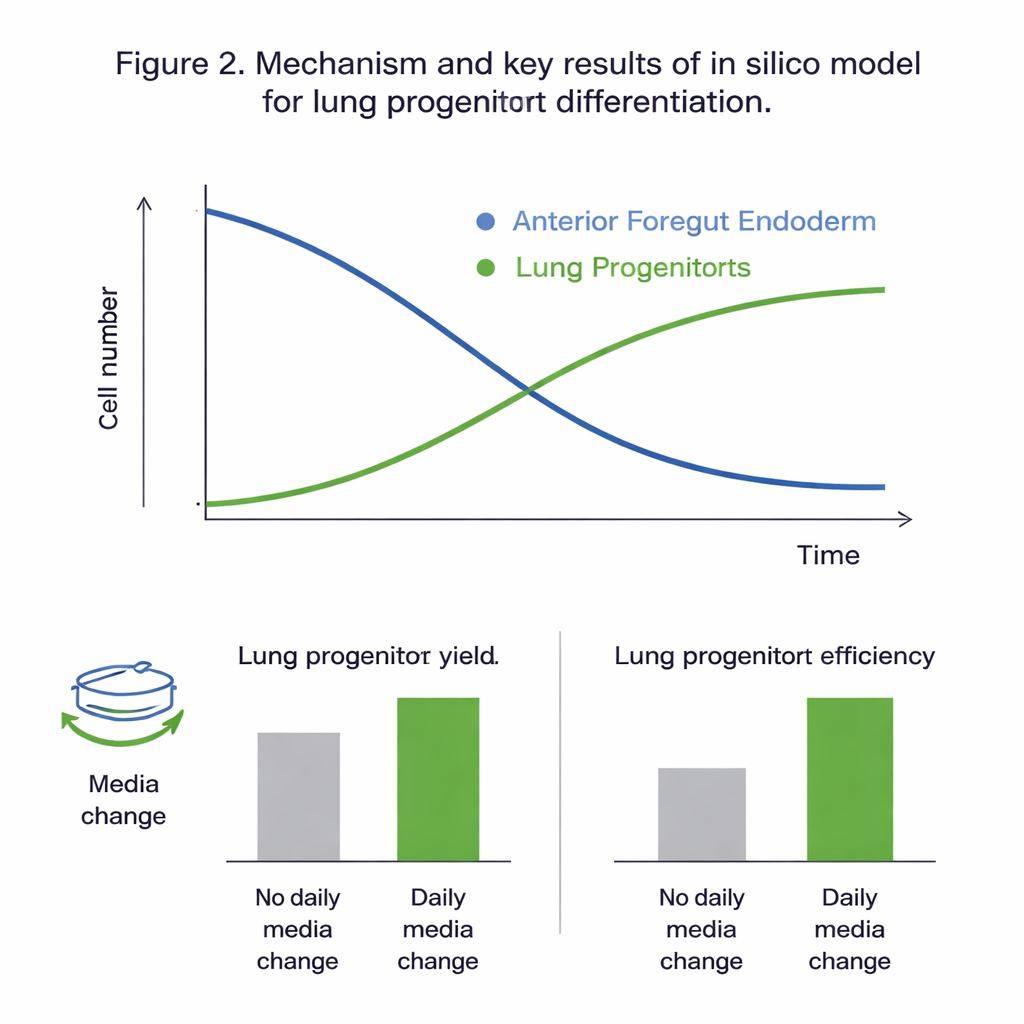
虚拟实验揭示的内容
将所有候选模型拟合到实验数据表明,能够分别追踪前肠细胞和肺祖细胞的两群体模型可以被可靠校准并最好地捕捉到观察到的行为。统计检验显示,在所研究的时间窗口(方案的第11至第15天),动力学主要由前肠细胞的增殖和分化驱动,而肺祖细胞本身的增殖贡献较小。全局灵敏度分析强化了这一结论,突出显示前肠细胞的生长、死亡和分化速率——以及葡萄糖的影响——是控制结果的主要杠杆。经校准的模型能以与实验自然变异相当的误差再现未见过的数据,表明其足够精确,可用于在计算机中探索“如果……会怎样”的情形。
优化换液与传代策略
有了可靠的虚拟系统,团队测试了两个实际操作选择对结果的影响:第10天培养的稀释程度(传代比例)以及是否每天更换培养基。模拟预测每日换液几乎可使肺祖细胞数量和每个起始细胞的产出翻倍,主要是通过防止营养耗尽与废物及不稳定信号分子的积累。实验结果与这些预测高度一致。模型还表明,使用更高的传代比例——第10天将细胞铺得更稀——能将“每个输入细胞的产出”提高约四分之一,尽管这会减少绝对细胞数。在两种情况下,这些改变对培养物中最终肺祖细胞的百分比影响不大,主要是改变了可以高效生产的细胞总量。
这对未来肺部疗法意味着什么
对非专业读者而言,关键信息是作者构建了一种类似飞行模拟器的工具,用于干细胞培养过程中一个关键步骤。通过将精心设计的实验与严谨的数学建模相结合,他们展示了诸如换液频率和接种密度等简单的操作选择如何显著影响可产生的构建肺细胞数量而不改变细胞质量。此类计算机模拟可帮助简化未来的培养方案、减少实验猜测,并最终支持更可靠、可扩展的肺祖细胞生产,用于研究、疾病模型构建及未来的再生治疗。
引用: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
关键词: 肺祖细胞, 诱导多能干细胞, 计算机模拟, 细胞分化, 再生医学