Clear Sky Science · zh
拷贝数改变与癌症免疫转录组景观的关联
为什么我们的基因对癌症免疫疗法重要
癌症免疫疗法通过帮助免疫系统识别并攻击肿瘤发挥作用,但只有少数患者能获得持久疗效。本研究提出了一个基础但具有重大临床意义的问题:肿瘤细胞内部的基因混乱——尤其是称为拷贝数改变的大范围DNA增失——如何塑造针对癌症的免疫反应,我们能否从基因活性模式中读取这些影响?
从全景视角审视癌症数据
为了解答这一问题,研究者汇集了庞大的数据集,总计294,159份来自肿瘤及其他组织的基因活性谱。这些谱来自多个主要公共数据库,记录了数千个样本中哪些基因被开启或关闭,涵盖多种癌症类型和实验条件。研究团队没有逐个基因地检视,而是使用一种数学方法将每个谱分解为若干潜在“成分”——那些倾向于同时上调或下调的重复基因模式,每一成分代表一种生物学过程,如免疫反应或DNA改变的效应。
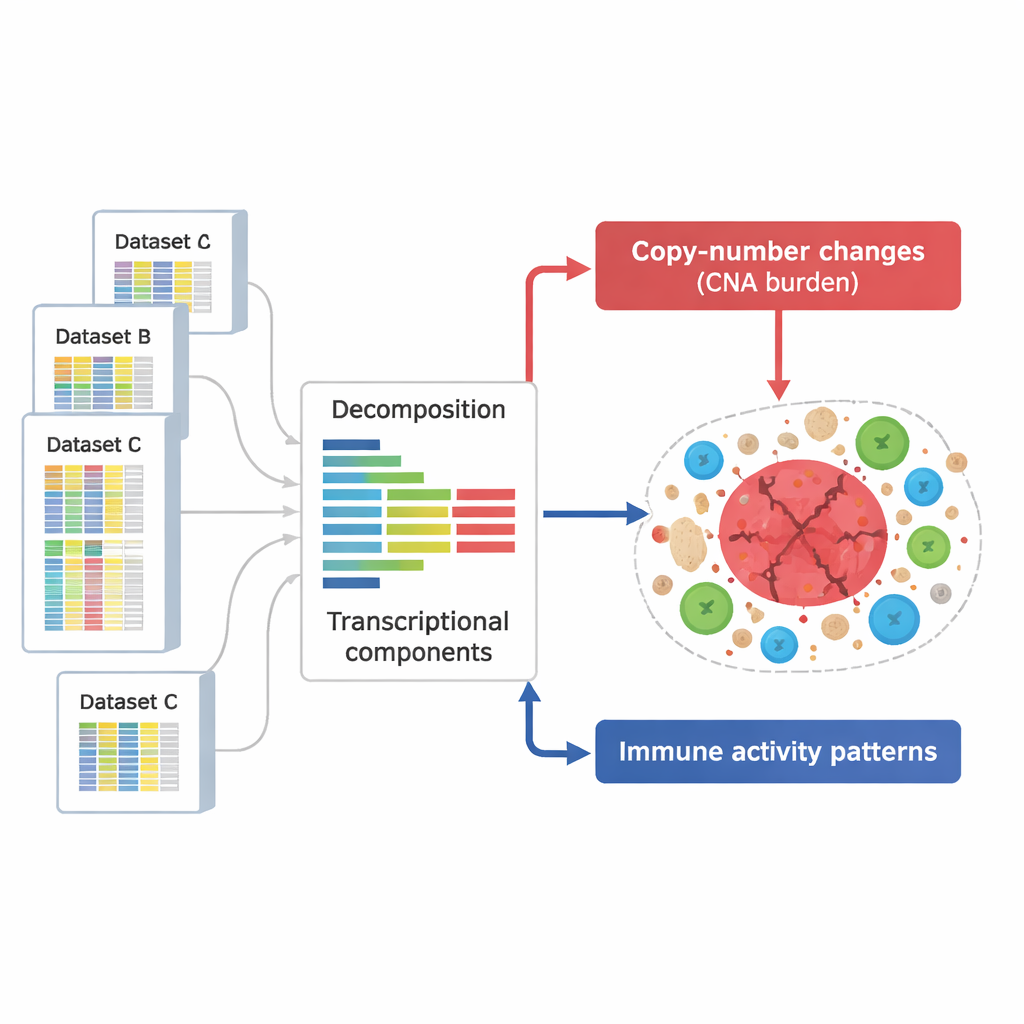
把DNA损伤信号与免疫信号分开
从这些成分中,科学家定义了两类关键组。一类捕捉了拷贝数改变的效应——在癌细胞中反复被增多或缺失的染色体片段。这些模式覆盖了几乎整个基因组,表明大多数受此类改变影响的区域都会在基因活性上留下可检测的印记。另一类成分则富集了参与免疫功能的基因,例如T细胞活化、自然杀伤细胞活性和抗原呈递。总体上,他们识别出657个与DNA相关的成分和283个与免疫相关的成分,其中许多在独立数据集和不同技术中可重复观察到,表明它们代表了肿瘤生物学的稳健、普遍特征。
将模式与治疗反应联系起来
团队随后探讨这些免疫相关模式能否帮助预测谁会对免疫检查点抑制剂(一类主要的癌症免疫药物)产生反应。利用来自13项临床研究、共1,167名患者(涉及7种癌症类型)的数据,他们训练了计算模型,仅基于治疗前肿瘤样本中免疫成分的活性来区分应答者与非应答者。有些模型在完全独立的患者组上仍表现强劲;例如,在一组乳腺癌队列上训练的模型能够准确预测另一独立乳腺癌队列的反应,并在若干其他癌种中显示有用的预测能力。一小部分免疫模式对这些预测贡献最大,包括与干扰素反应、自然杀伤细胞和T细胞活化相关的模式。
基因混乱如何重塑肿瘤免疫
在此框架下,研究者系统地将总体拷贝数改变负荷——衡量肿瘤DNA被增失的广泛程度——与多个癌种中每个免疫模式的活性相关联。大多数免疫模式呈负相关:具有高DNA改变负荷的肿瘤往往在与有益免疫功能相关的成分(如抗原呈递和关键免疫细胞浸润)上表现较低。然而,少数模式则朝相反方向变化。高改变负荷的肿瘤常伴随免疫抑制性细胞类型的信号增强,包括调节性T细胞和某些巨噬细胞,以及一些可促进肿瘤生长而非破坏肿瘤的炎性细胞。对肿瘤切片的空间分析证实,DNA变化严重的区域常与有益免疫模式活动低下重合,并与“免疫排斥”区相符——这些区域中免疫细胞被限制在肿瘤边缘。
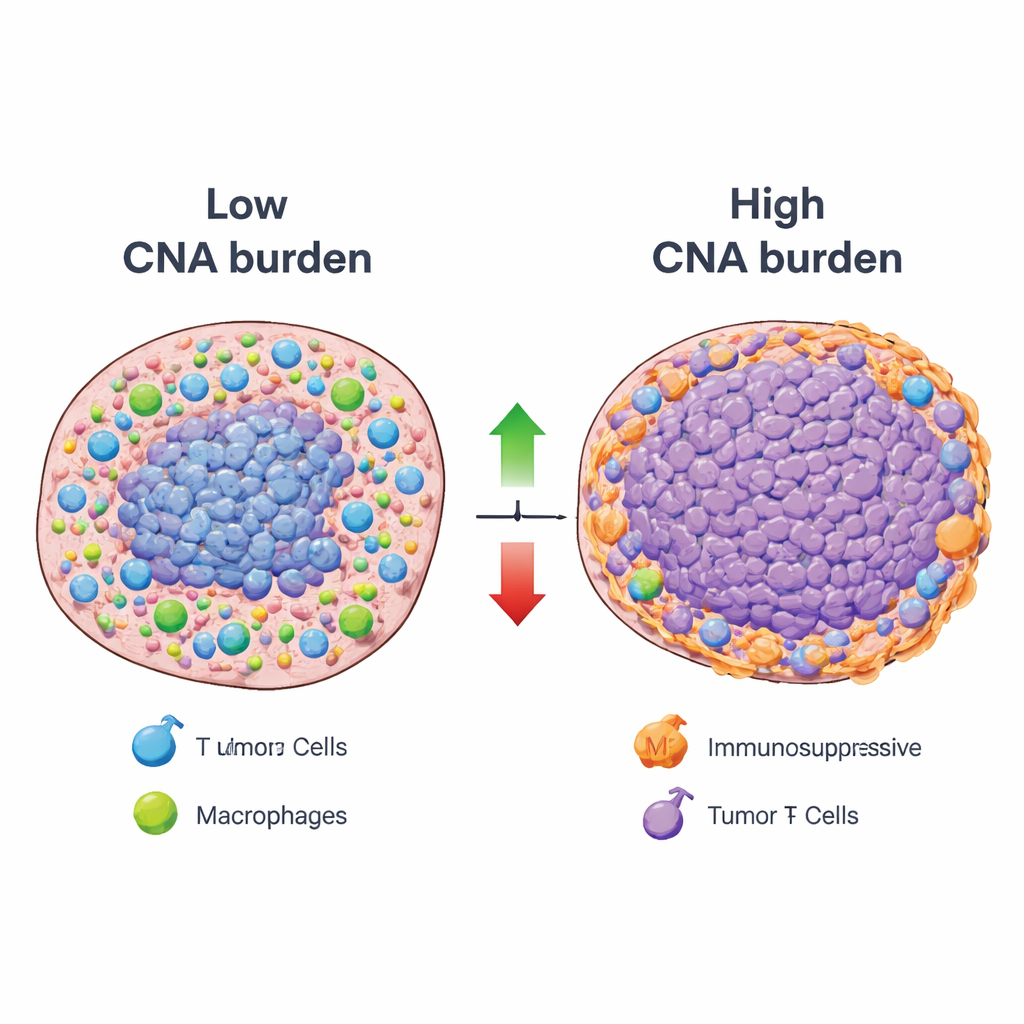
这对未来癌症治疗意味着什么
简而言之,研究表明,被大规模DNA增失困扰的肿瘤既抑制有益的免疫反应,又促成抑制性或促肿瘤的免疫环境。然而,它们并非免疫学上的沉默群体;相反,它们展示出特定且重复出现的免疫状态,这些状态可能对靶向疗法敏感,例如阻断IL-17或IL-23信号的药物,或重新编程某些巨噬细胞的策略。通过在各类癌症中绘制这些DNA—免疫关系并公开该资源,该工作为解释为何某些基因不稳定的肿瘤抵抗当前免疫疗法提供了详尽指南,并提出了可帮助免疫系统克服这种抵抗的新型组合治疗策略。
引用: Loipfinger, S., Bhattacharya, A., Urzúa-Traslaviña, C.G. et al. Association of copy number alterations with the immune transcriptomic landscape in cancer. npj Syst Biol Appl 12, 28 (2026). https://doi.org/10.1038/s41540-026-00649-8
关键词: 癌症免疫疗法, 拷贝数改变, 肿瘤微环境, 免疫检查点抑制剂, 转录组学