Clear Sky Science · zh
多糖与结肠粘液屏障:生物物理相互作用与功能影响的综述
为何肠道那层光滑内膜至关重要
在你的大肠深处存在一层黏滑、肉眼不可见的防护膜:一层粘液,将数万亿微生物与自身细胞隔开。本文综述探讨了来自食物、海藻、真菌和医疗产品的复杂糖类——多糖,如何与该粘液屏障相互作用。理解饮食与粘液之间的这种对话,有助于解释为何某些纤维对肠道健康有益、为何一些治疗能保护结肠免受结肠炎等肠病侵扰,以及更智能的药物递送系统如何将药物精准地输送到最需要的位置。
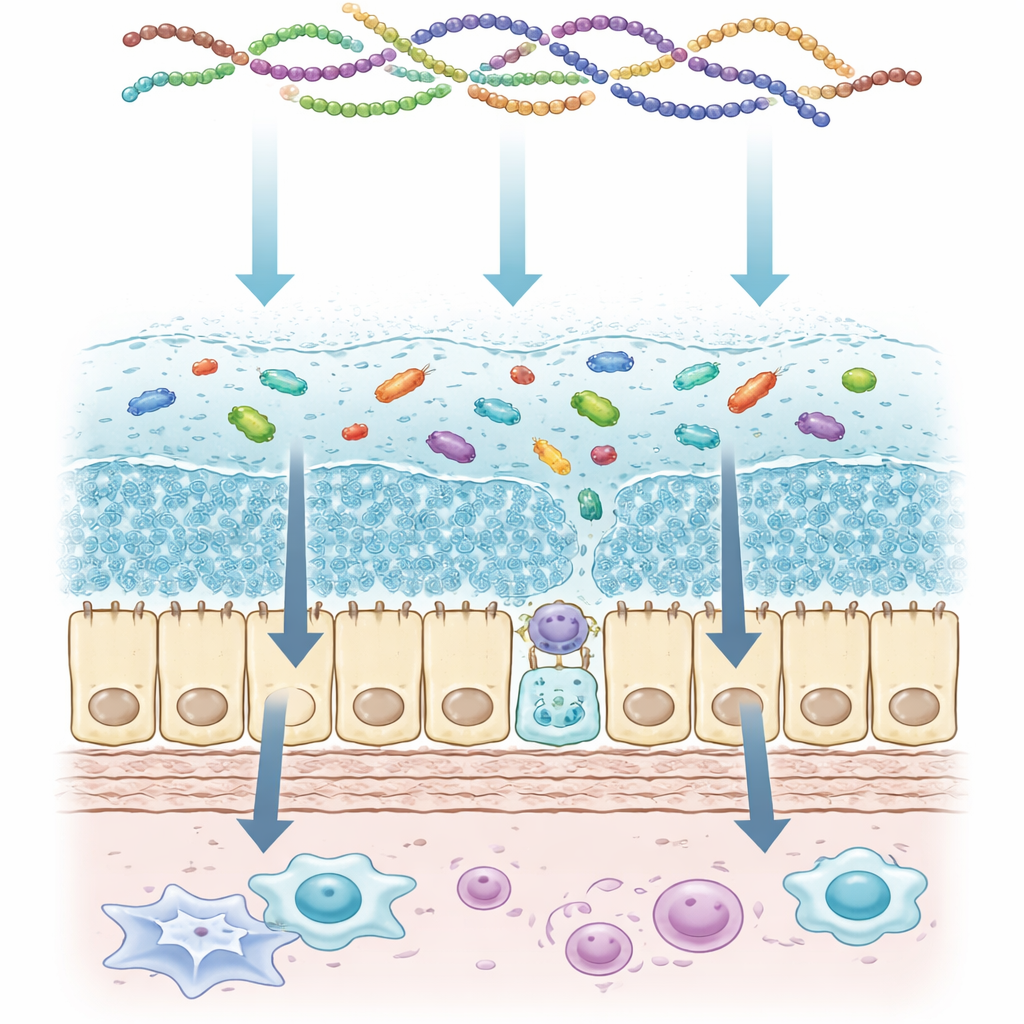
结肠的双层安全毯
作者首先将结肠粘液的结构描述为一座两层建筑。最靠近肠壁的是一层致密的内层,几乎无细菌并像一道紧密的屏障。外层则较为疏松,是益生微生物的受控栖息地。称为杯状细胞的专门细胞不断产生并分泌大型粘液分子,这些分子到达肠表面后迅速展开并凝胶。这些成胶分子带有大量糖分支,赋予粘液黏稠度、持水能力和负电荷。当该结构因炎症、感染或基因缺陷而破坏时,细菌更靠近肠壁,免疫报警被触发,慢性肠道疾病可能随之出现。
不同糖类,不同的黏附方式
多糖本身是由简单糖构成的长链,但它们在粘液中的行为取决于诸如大小、分支和电荷等细节。中性链如抗性淀粉和菊粉主要通过氢键和物理缠绕与粘液网状结构交织。来自果胶、褐藻酸盐和海藻胶等的带负电荷的链,依据局部离子环境以及两者电荷的精细分布,可能与粘液弱相互作用或相互排斥。带正电的链,尤其是来源于甲壳类和真菌的壳聚糖,会强烈吸附粘液并形成紧密复合物。综述指出,这些相互作用并非由单一力主导,而是由静电吸引、氢键、疏水接触以及微妙的范德华力共同决定多糖穿透凝胶的深度及其黏附强度。
芯片、培养皿与组织切片上的模型肠壁
为理清这些复杂相互作用,研究者依赖一整套实验模型。可在平面细胞培养中加入分泌粘液的细胞来考察特定多糖如何改变粘液的产生、厚度或渗漏性。由干细胞培养的三维类器官构建迷你肠道管道,可自行分泌粘液;微流控“肠道芯片”平台则引入真实的流动、拉伸与活菌。离体(ex vivo)实验保留新鲜分离的肠组织在短时间内活性,保存天然的粘液层和免疫细胞。每种模型各有利弊:简单的培养皿便于操作但较为人工,芯片和类器官更贴近生理但技术要求高。通过对比这些系统的结果,科学家能将多糖对粘液的直接物理影响与由微生物和免疫系统驱动的间接影响区分开来。
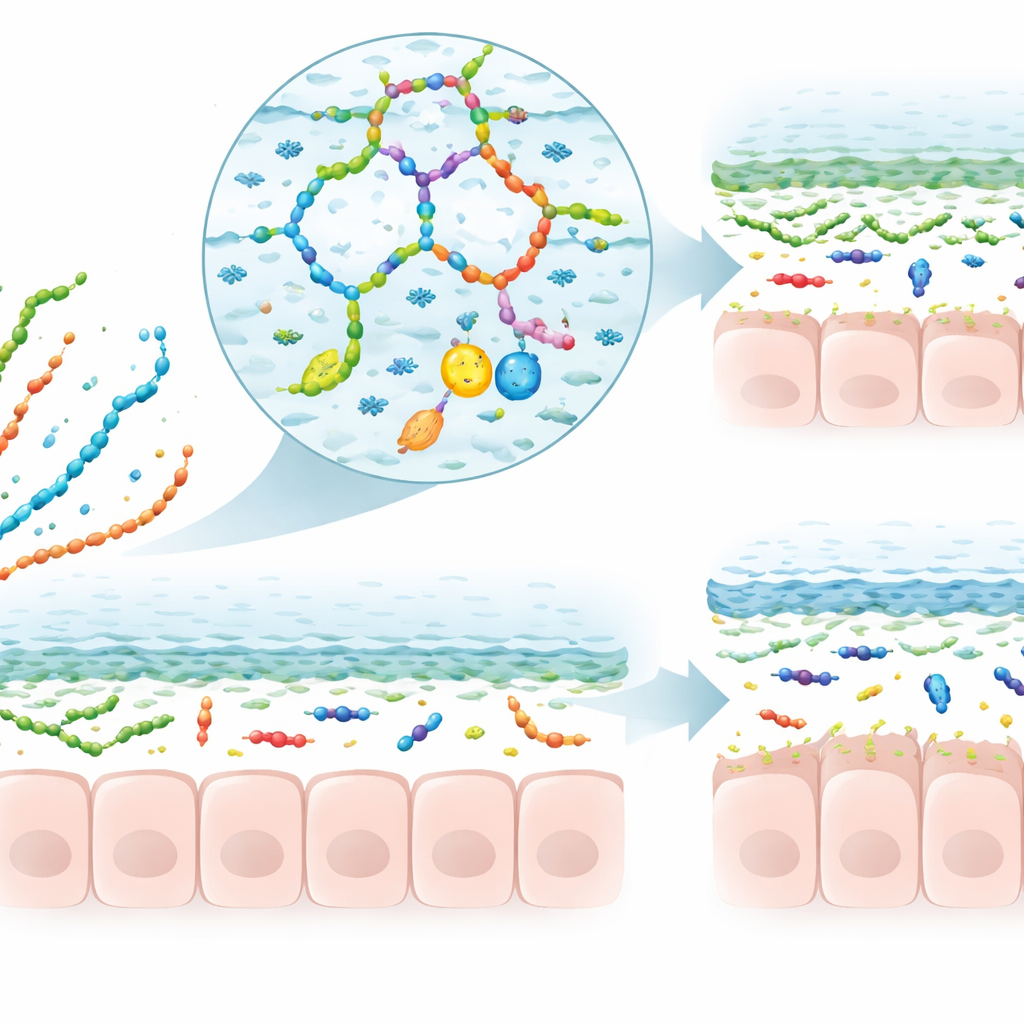
塑造粘液、微生物与免疫反应
综述接着考察了多糖与粘液相遇时在功能上会发生什么。一些带正电的链可暂时松散或重组凝胶,影响颗粒和药物通过粘液的难易程度。另一些则与粘液形成混合网络,使其变厚或更稳定。许多膳食多糖不被人体消化,而被肠道细菌发酵,转化为短链脂肪酸及其它小分子。这些发酵产物会向杯状细胞发出信号,促使其生成更多粘液、调整粘液上的糖装饰,并支持倾向于停留在外层的微生物群。在结肠炎动物模型中,某些植物和真菌多糖可增加杯状细胞数量、恢复粘液厚度并使细菌远离肠壁,通常伴随炎症和氧化应激的降低。
与粘液协同设计食品与疗法
结论中,作者主张可以有意识地设计或选择多糖以支持粘液屏障,而不是无意中损害它。通过将特定结构特征——如电荷与分子量——与粘液厚度、粘度和可穿透性等可测量结果联系起来,他们提出了选择能强化屏障、更有效将药物输送到结肠或温和引导微生物群向有益活动方向发展的多糖的指导原则。对非专业读者而言,核心信息是结肠内的那层黏膜并非被动的黏稠物;它是饮食化学、常驻微生物与免疫防御交汇的主动界面。经过深思熟虑设计的多糖可能成为保持该界面完整并维持肠道平衡的关键工具。
引用: Cheong, KL., Biney, E., Wang, M. et al. Polysaccharides and the colon mucus barrier: a review of biophysical interactions and functional impacts. npj Sci Food 10, 98 (2026). https://doi.org/10.1038/s41538-026-00750-6
关键词: 结肠粘液屏障, 膳食多糖, 肠道微生物群, 粘附性药物递送, 炎症性肠病