Clear Sky Science · zh
番茄红素通过作用于小鼠的Nrf2/选择性线粒体自噬轴缓解T-2毒素诱导的肝脏铁死亡
为何日常谷物中的霉菌毒素值得关注
包括小麦和玉米在内的许多主食可能被一种称为T-2毒素的霉菌毒素污染。这种看不见的污染物能在烹饪和加工中存活,长期暴露会在不声不响中损害重要器官,尤以肝脏为甚。本文总结的研究提出了两个紧迫问题:T-2毒素究竟如何损伤肝脏?一种天然食物成分——番茄和其他果实中的红色色素番茄红素,能否帮助抵御这种伤害?
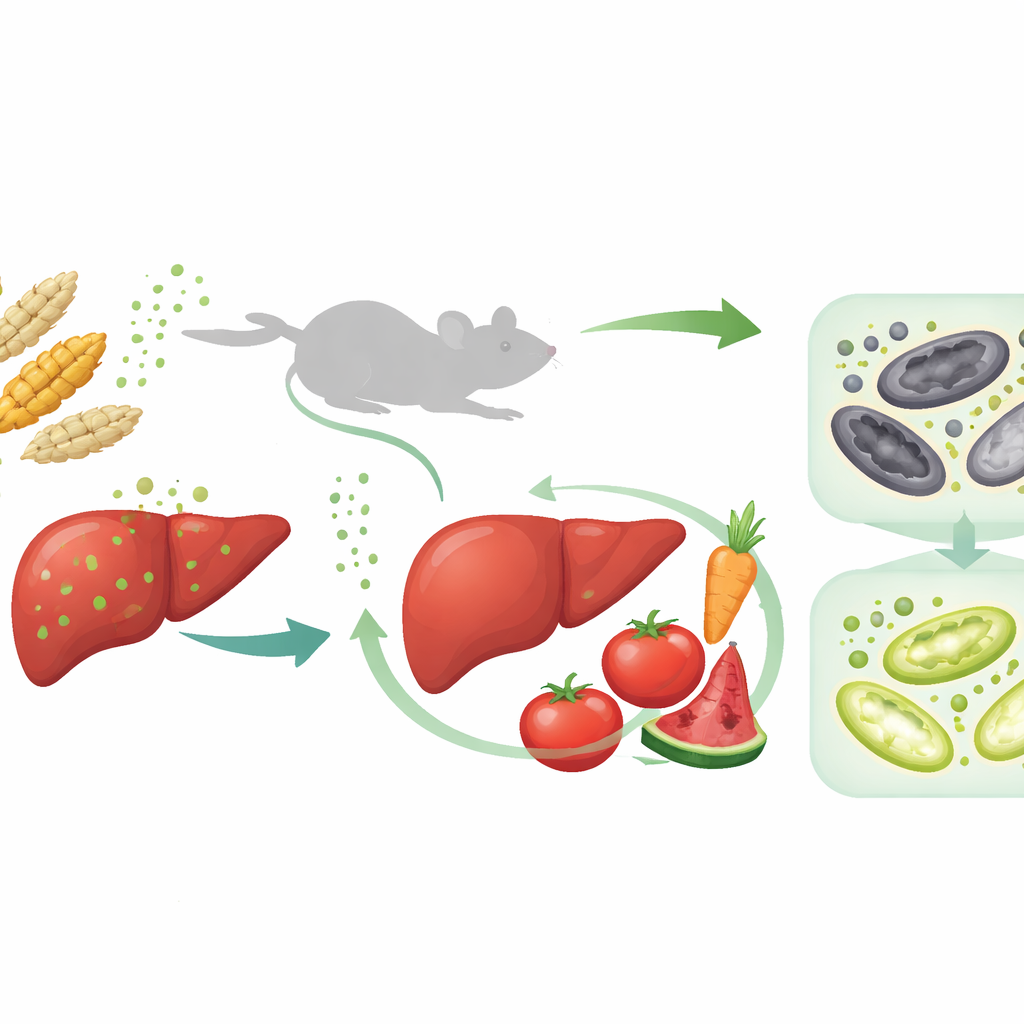
毒素如何损伤肝脏
研究者首先给小鼠喂以不同剂量的T-2毒素,持续四周,以模拟持续的膳食暴露。随着毒素剂量增加,动物体重增长受限,肝脏增大并呈淡黄色,血液检测显示提示损伤的肝酶水平升高。显微镜下,肝组织出现肿胀和结构紊乱,细胞内可见空泡和细胞死亡迹象。对肝样本进行的大规模蛋白质分析显示,多数变化显著的通路与铁代谢、脂质代谢以及一种由铁和脂质氧化失控驱动的特殊细胞死亡形式——铁死亡——有关。
铁超载与类似“生锈”的细胞死亡
进一步探查时,团队检测了典型的铁死亡标志。在受毒素影响的肝脏中,铁含量升高,表明脂质损伤的分子增多,而一种关键保护酶GPx-4的活性下降。细胞内通常用于安全储存铁的蛋白上调,但肝细胞主要的铁“出口”蛋白下调,提示铁被困在细胞内。当科学家给部分小鼠使用一种专门抑制铁死亡的药物时,肝脏结构和功能有所改善:肿胀减轻、损伤评分下降、氧化损伤的化学指标缓和。这坚实地将T-2毒素的肝毒性与一种由铁驱动、类似“生锈”的细胞死亡形式联系起来。
线粒体、细胞清洁与防御开关
研究组随后关注线粒体——细胞内的能量工厂,它们既是氧化应激的来源也是受害者。在受毒素处理的小鼠中,线粒体的能量产出下降,同时细胞色素c外泄和总体活性氧水平上升,电子显微镜显示线粒体萎缩且结构受损。与此并行,细胞的质量控制系统——选择性线粒体自噬(mitophagy),一种去除有缺陷线粒体的清理过程——通过PINK1和Parkin蛋白相关通路被激活。当研究者使用缺失Parkin且因此无法正常启动线粒体自噬的小鼠时,T-2毒素导致更严重的铁积聚、更强的铁死亡信号和更严重的肝损伤。这表明线粒体自噬作为一种保护性制动,限制了毒素引发的损伤。
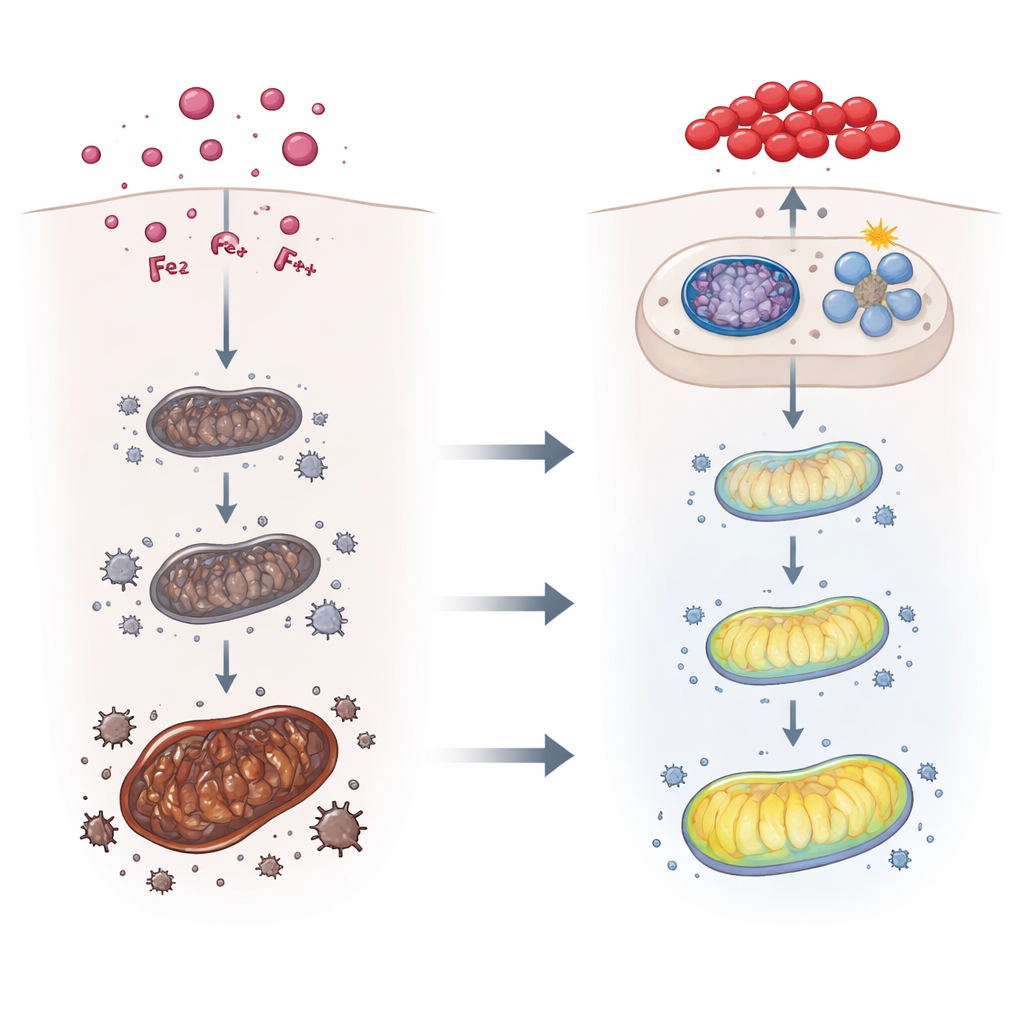
内建的防护通路与番茄红素的作用
因为铁平衡、氧化应激和线粒体自噬似乎相互交织,作者寻找一个上游调控因子并锁定了Nrf2——一个开启抗氧化与解毒基因的主开关。T-2毒素本身能部分激活Nrf2,但当给予能够激活Nrf2的已知化合物时,肝脏铁外排改善、铁死亡标志下降、线粒体自噬增加,所有这些都减轻了毒素的影响。团队接着考察番茄红素是否能作为天然的Nrf2增强剂。计算机模拟表明番茄红素可物理结合Nrf2及其抑制蛋白Keap1,方式有利于Nrf2的激活。在活体小鼠中,暴露前和暴露期间给予番茄红素处理可改善体重、恢复肝脏外观和血液指标、降低铁积累和氧化损伤,并进一步激活Nrf2及PINK1–Parkin线粒体自噬通路。
这对食品安全与饮食意味着什么
简而言之,该研究表明T-2毒素通过将过量的铁困在细胞内、破坏线粒体并诱发铁死亡来损伤肝脏。机体通过激活Nrf2和线粒体自噬来清除受损线粒体并重新平衡铁,但这种防御可能被压垮。番茄红素似乎能增强这一内在防护,帮助肝脏外排铁、清理损坏的线粒体并抵御铁死亡。尽管在将这些发现推广到人类之前仍需更多工作,该研究提示某些植物化合物(如番茄红素)未来可能成为减轻不可避免的食源性毒素健康影响的策略组成部分。
引用: Yang, X., Song, W., Lu, Z. et al. Lycopene mitigates T-2 toxin-induced hepatic ferroptosis by targeting the Nrf2/mitophagy axis in mice. npj Sci Food 10, 94 (2026). https://doi.org/10.1038/s41538-026-00736-4
关键词: T-2毒素, 番茄红素, 肝损伤, 铁死亡, 选择性线粒体自噬