Clear Sky Science · zh
在模拟营养吸收中比较人类肠道类器官与Caco-2细胞的转录组:来自婴儿配方奶与母乳的见解
喂养婴儿与检测他们的食物
家长和科学家都希望了解婴儿配方奶在多大程度上能复制母乳的益处,尤其是对婴儿生长中的肠道。本研究并非在真实婴儿身上进行,而是在先进的体外培养“小肠”模型中检视母乳与几种商业配方奶的差异。通过比较这些喂养选项与更接近真实肠道的模型的相互作用,研究者评估哪种实验系统更像婴儿肠道,以及不同配方加工方法可能如何影响生长、免疫和长期安全性。
培养皿中的微型肠道
为了安全且详细地研究婴儿营养,研究组使用了两种人类肠道的实验模型。一种是长期使用的经典模型:Caco-2细胞——一种单层、相对均一的类肠细胞片。另一种更新、更具生理相关性:三维的人类小肠类器官,常被称为“微型肠道”。这些类器官由干细胞培养而成,包含肠道中常见的多种细胞类型,包括吸收营养的细胞、分泌粘液的细胞以及参与免疫功能的细胞。通过染色和显微镜观察证实,类器官形成了有序的、空腔状结构,含有多样且活跃分裂的细胞,使其成为有前景的婴儿肠道替代模型。
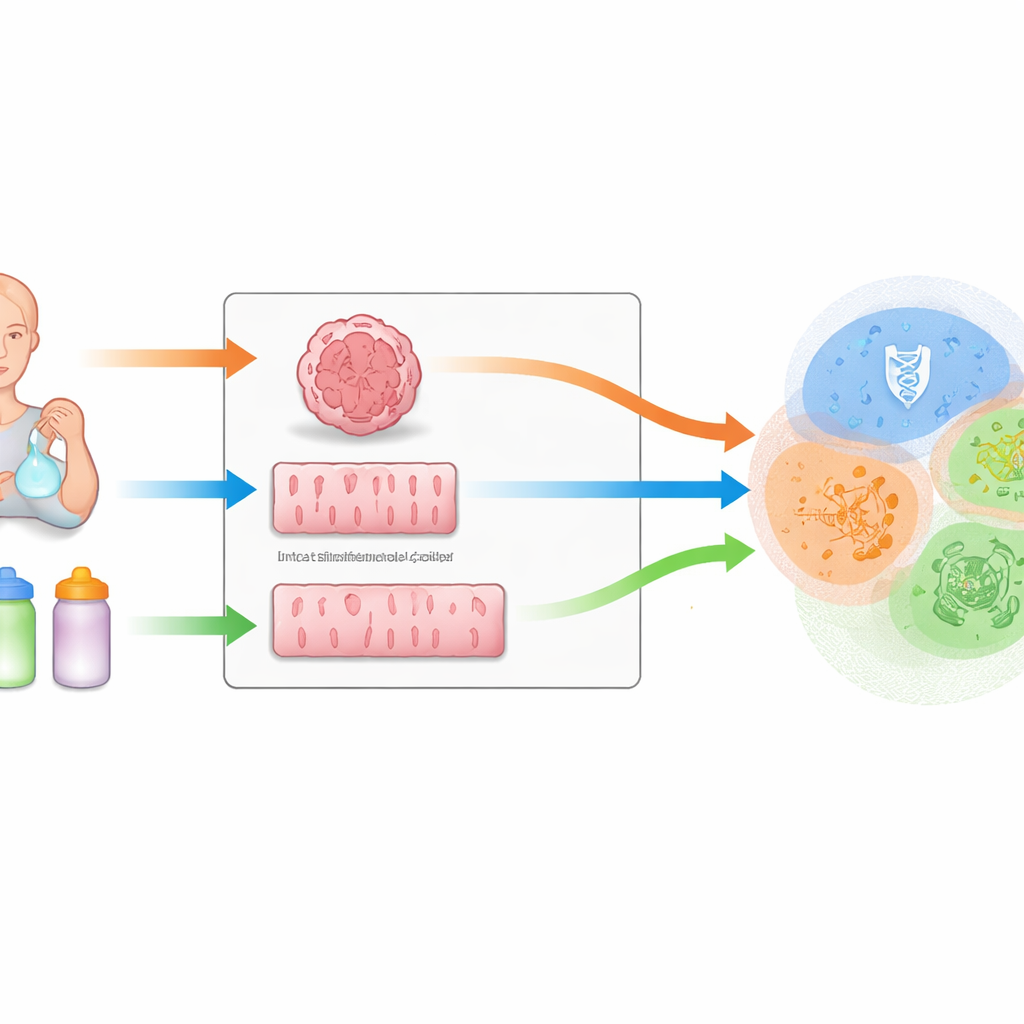
对母乳与配方奶进行消化模拟
研究者随后模拟了奶类在婴儿胃与小肠内的消化过程。他们收集了来自七位健康供乳者的母乳样本,以及三种不同工业加工方法生产的1段婴儿配方奶:干混(IFA)、单步湿混(IFB)和两步湿混(IFC)。所有样品均通过模拟婴儿胃肠条件的体外消化系统处理。将消化后的液体施加到类器官或Caco-2细胞层上,团队使用RNA测序测量这些细胞中成千上万基因的表达开关如何改变。
哪种模型更接近真实肠道?
当科学家比较基因表达模式时,类器官模型明显优于Caco-2细胞。类器官相较未处理对照显示出更大的表达变化,样本按喂养类型清晰分组,并产生更多对母乳与配方奶有响应的差异表达基因。关键的是,与组织生长、器官形态塑造和其他发育过程相关的基因通路在类器官中被强烈激活,而在Caco-2细胞中则不那么一致。同时,在所用剂量下,两种模型都未显示明显的细胞损伤通路被强烈激活,表明这些暴露本身并非明显有毒。总体而言,这些发现表明微型肠道比传统的单层细胞更能捕捉婴儿食物对肠道的细微分子影响。
配方奶与母乳及彼此间的差异
利用类器官数据,研究组将母乳与三种配方奶品牌进行了比较。许多基因变化是共有的,显示配方奶在总体上支持与生长和代谢相关的通路。但也出现了重要差异。母乳具有独特的分子特征,并与其中一种配方共享了众多有益通路,这也说明了为什么母乳仍然是营养学的金标准。所有配方都上调了与组织发育和细胞连接(维持肠道屏障所需)相关的基因。然而,每个品牌各有侧重:IFA特别增强了脂质合成过程以及离子和有机酸转运;IFB强烈支持细胞表面的纤毛结构及其周围支持基质;而IFC在下调过度炎症和促进分泌的基因上更为突出,这种模式可能与其包含的人乳低聚糖有关。
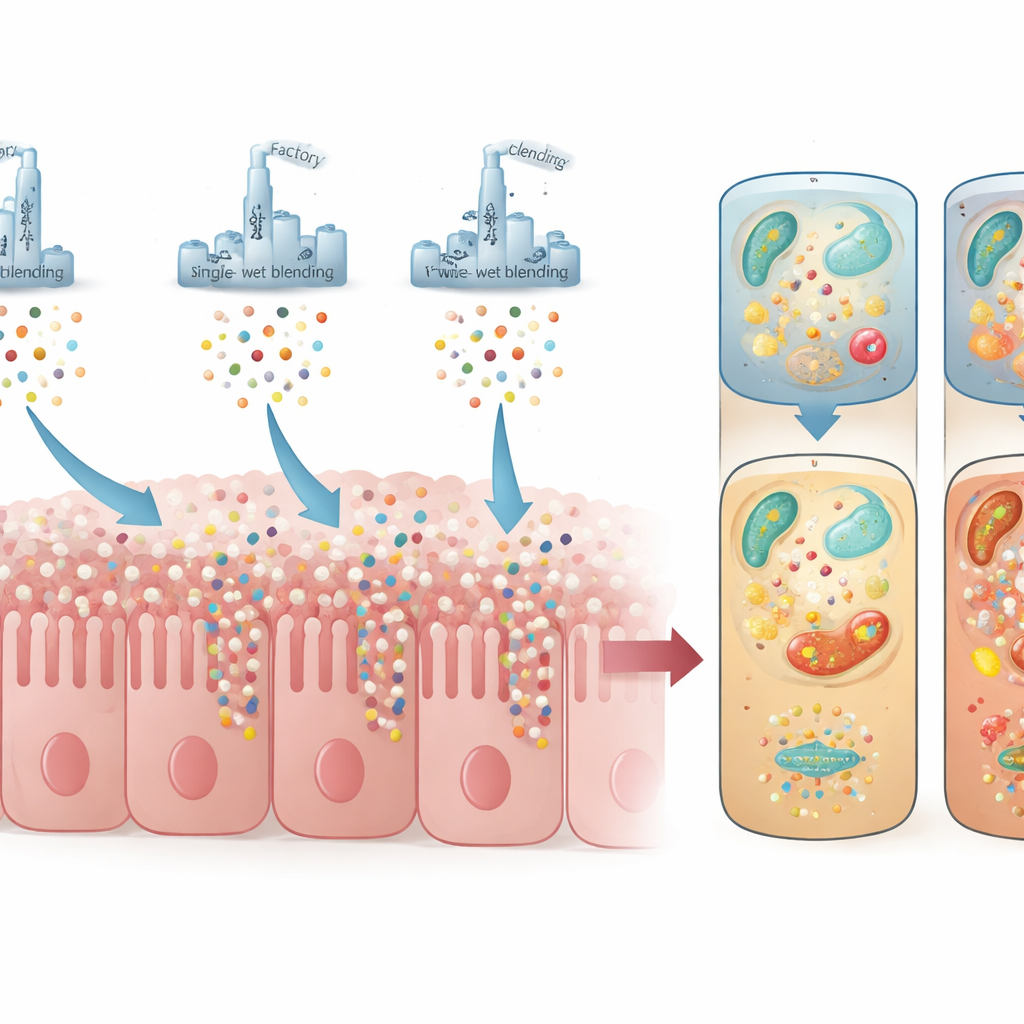
加工的隐性代价
并非所有差异都是积极的。由两步湿混生产的IFC也引发了更强的与毒性物质和氧化应激相关的反应——即对细胞的化学性磨损。后续的代谢物测量证实,与其他配方相比,IFC中与脂质氧化相关的分解产物水平更高。在类器官中,IFC比干混或单步湿混产品更刺激与应激和炎性信号相关的基因。尽管商业粉末的配方并不完全相同,数据仍指向更复杂且更耗热的两步加工过程,可能是导致这种额外氧化负担的一个重要因素。
这对婴儿食物意味着什么
简而言之,这项工作表明,先进的微型肠道模型比传统的单层细胞培养更能揭示婴儿食物如何在分子水平上塑造肠道。母乳仍然占优,呈现出支持生长与免疫平衡的独特信号模式。现代配方确实能激活许多相同的有益通路,但其生产方式很重要:更温和的加工似乎能减少氧化相关副产物的积累,而更为密集、多步的加热处理可能带来额外的长期风险。该研究表明,类器官可以为设计更安全、更适合婴儿的配方提供参考并促进行业改进加工工艺,同时强调在可行时母乳的重要价值。
引用: Wang, X., Zhang, W., Yang, S. et al. Transcriptomic comparison of human intestinal organoids and Caco-2 cells in modeling nutrient absorption: insights from infant formula and breast milk. npj Sci Food 10, 101 (2026). https://doi.org/10.1038/s41538-025-00672-9
关键词: 婴儿配方奶, 母乳, 肠道类器官, 营养吸收, 氧化应激