Clear Sky Science · zh
来源于脂肪的双细胞疗法通过血管整合促进动脉发生和肢体保全以治疗危重型肢体缺血
通过长出新血管来拯救肢体
当腿部动脉逐渐堵塞时,患者可能出现难以忍受的疼痛、顽固性溃疡,甚至面临截肢的风险。这一严重阶段称为危重型肢体缺血,难以治疗,因为许多患者无法接受搭桥手术或其他常规疗法。本文综述的研究探索了一种新策略:从患者自身脂肪中取出两类类干细胞,帮助机体生长坚固的新血管,从而拯救缺血的肢体组织。
常见疾病但治疗选择有限
周围动脉疾病发生时,腿部动脉狭窄,血流受阻。在最严重的形式——危重型肢体缺血中,患者可能持续疼痛、趾端发黑,且丧失肢体局部的风险很高。当前治疗如降脂药、血管成形术或外科搭桥可以发挥作用,但许多患者无效或因病情过重无法承受这些手术。早期单一干细胞类型的尝试多半只促成了脆弱的微小血管,这些血管无法提供足够的血流来可靠地挽救肢体。因此,研究者着手构建更完整的“替代管路系统”,结合两种相互协作的细胞类型。
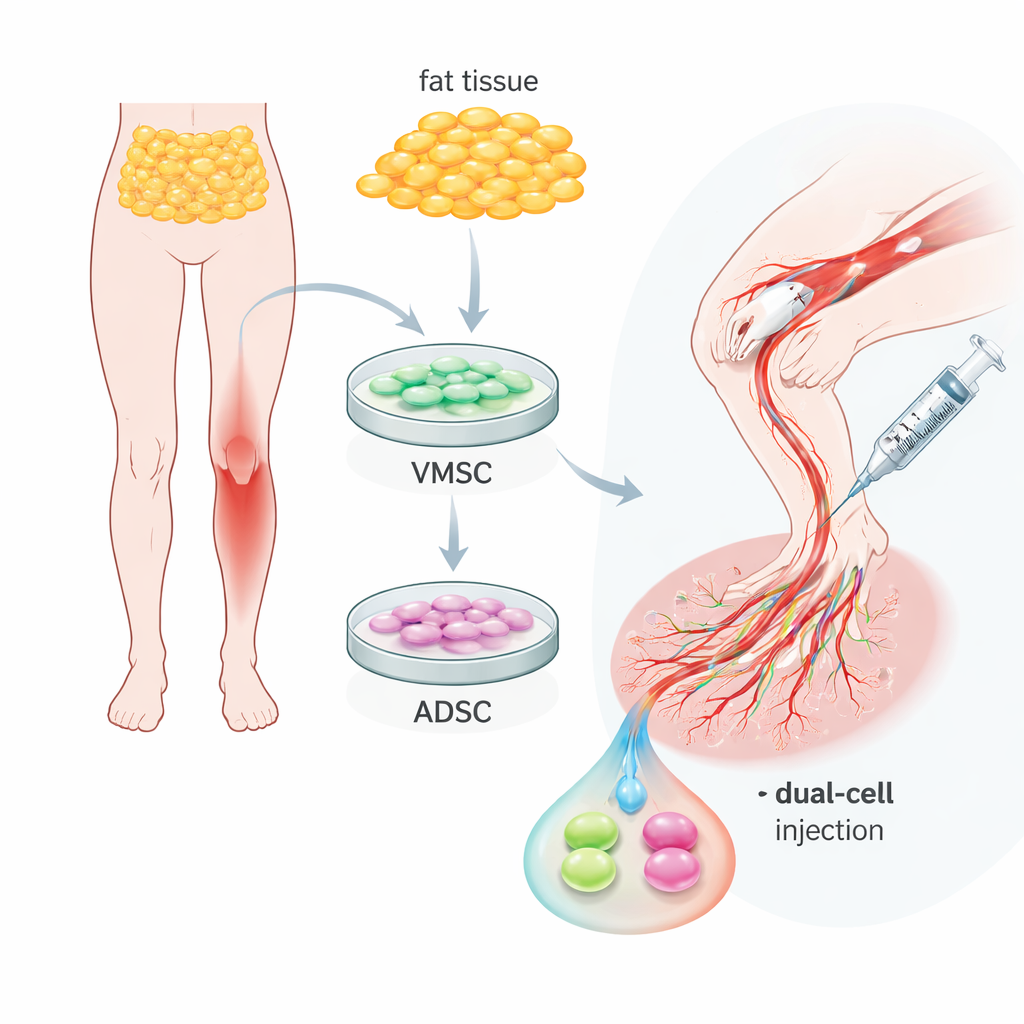
普通脂肪中两种有益的细胞类型
研究团队把注意力放在脂肪组织——普通的体脂上,这类组织可通过相对创伤小的取样获得。从同一样本中,他们分离出两类相关但不同的细胞群。一类称为血管多能干细胞,其行为更像早期的血管内皮细胞:表面带有典型的内皮标志,能在培养皿中组织成毛细血管样的管道。第二类为来源于脂肪的干细胞,更像围绕血管的支持细胞,携带平滑肌和血管周细胞常见的标志。两类细胞都能良好增殖并分化为脂肪、骨或软骨细胞,证明其多能性,但它们在血管周围的天然角色明显不同且互补。
在应激环境下协同工作
为模拟病变肢体中严酷的炎性环境,研究者让这些细胞暴露于强烈的炎性信号中。两类细胞均能存活并通过释放生长因子与酶的混合物来调整行为,这些分子有助于细胞移动并重塑周围组织。在促进血管形成的凝胶上单独培养时,类似内皮的细胞可以形成基本的管道,而支持细胞主要呈团块状。然而,当以二比一的比例混合时,形成的管道更致密、更连续且对炎性应激更具抵抗性。这提示两类细胞合用不仅能产生更多血管,而且能形成更成熟、更稳定的网络。
在病变小鼠肢体中测试双细胞疗法
随后,科学家在一种通过结扎主要腿动脉构建的危重型肢体缺血小鼠模型中进行试验。他们将混合的人源细胞注射到缺血的腿肌内。四周内,未治疗的对照鼠常常出现趾部坏死或整只足丧失,肌肉显示瘢痕化和严重炎症。相比之下,接受双细胞治疗的动物大多保住了肢体。血流成像显示,处理腿的循环恢复到约正常水平的70%,而对照组则不到20%。显微和三维成像揭示了原因:治疗组肌肉中中等和大口径血管——类似小动脉和小动脉分支——明显增多,且有牢固的支持细胞“包膜”,而不是仅仅一团不稳定的微小毛细血管。
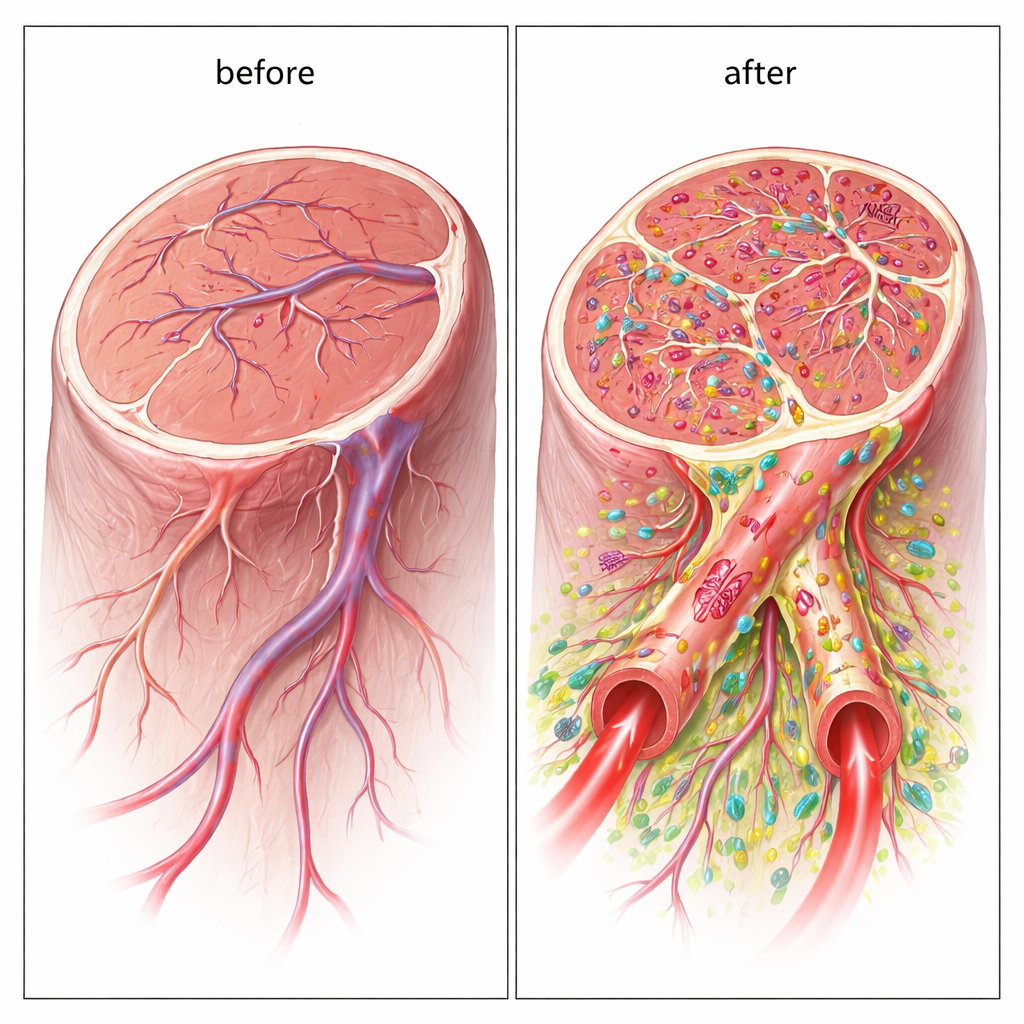
由供体细胞构建的混合血管
重要的是,新形成的血管并非仅被这些细胞促成;移植的人源细胞实际上成为血管壁的一部分。通过人源特异性标记,研究者发现类似内皮的细胞参与了内层衬里形成,而支持细胞则包裹在外层。许多这种混合血管口径足够大,可作为真正的血液通道,而且荧光示踪物证实血液确实通过这些血管流动。这种由细胞直接构建出的、大口径且有灌注的血管使双细胞方法有别于大多数此前主要依赖化学信号而非长期结构整合的干细胞疗法。
这对患者可能意味着什么
对非专业读者而言,结论是科学家可能正在学会如何利用患者自身的脂肪来源细胞来“重新配管”濒死的肢体。通过配对两种细胞——一种形成内层管腔,另一种构建外层支撑——该疗法生成的是坚固、内衬良好的动脉和小动脉,而非脆弱的毛状新生物。在小鼠中,这足以恢复血流并防止肢体丧失。尽管仍需更多工作来证明在人类中的长期安全性和有效性,这项研究指向了这样一个未来:通过微创的脂肪采集即可获得个性化的细胞混合物,用以重建高截肢风险患者的循环系统。
引用: Kim, D.Y., Hwang, D.Y., Park, G. et al. Adipose-derived dual cell therapy enhances arteriogenesis and limb preservation through vascular integration in critical limb ischemia. npj Regen Med 11, 13 (2026). https://doi.org/10.1038/s41536-026-00458-x
关键词: 危重型肢体缺血, 干细胞疗法, 来源于脂肪的细胞, 新生血管形成, 周围动脉疾病