Clear Sky Science · zh
新型铜离子配位的肝素内酯(andrographolide)负载水凝胶通过激活Rac1/JNK1轴促进糖尿病伤口愈合
为什么难愈合的伤口很重要
对于许多糖尿病患者来说,脚上的一个小水泡可能演变成一个长期不愈合的伤口,甚至导致截肢。这些难治性溃疡由感染、失控的炎症和血供不足共同推动。本文总结所述的论文介绍了一种新型凝胶状敷料,旨在同时解决这三类问题,利用植物化合物与微量金属来引导受损皮肤向正常修复转变。
由水凝胶构建的智能创可贴
研究者制备了一种柔软、含水量高的材料——水凝胶,设计用于直接覆盖伤口。该材料由明胶(一种来源于胶原的蛋白)和改性的壳聚糖(一种糖类聚合物)构成。铜离子像微小的连接子一样,将各组分连接成柔性的网络,同时与一种名为肝素内酯(andrographolide)的植物分子结合,该分子具有抗炎、抗菌和降血糖等活性。铜配位显著提高了该药物的水溶性,并使其在凝胶中均匀分布而不会以晶体形式聚集,这对稳定释放到伤口中至关重要。
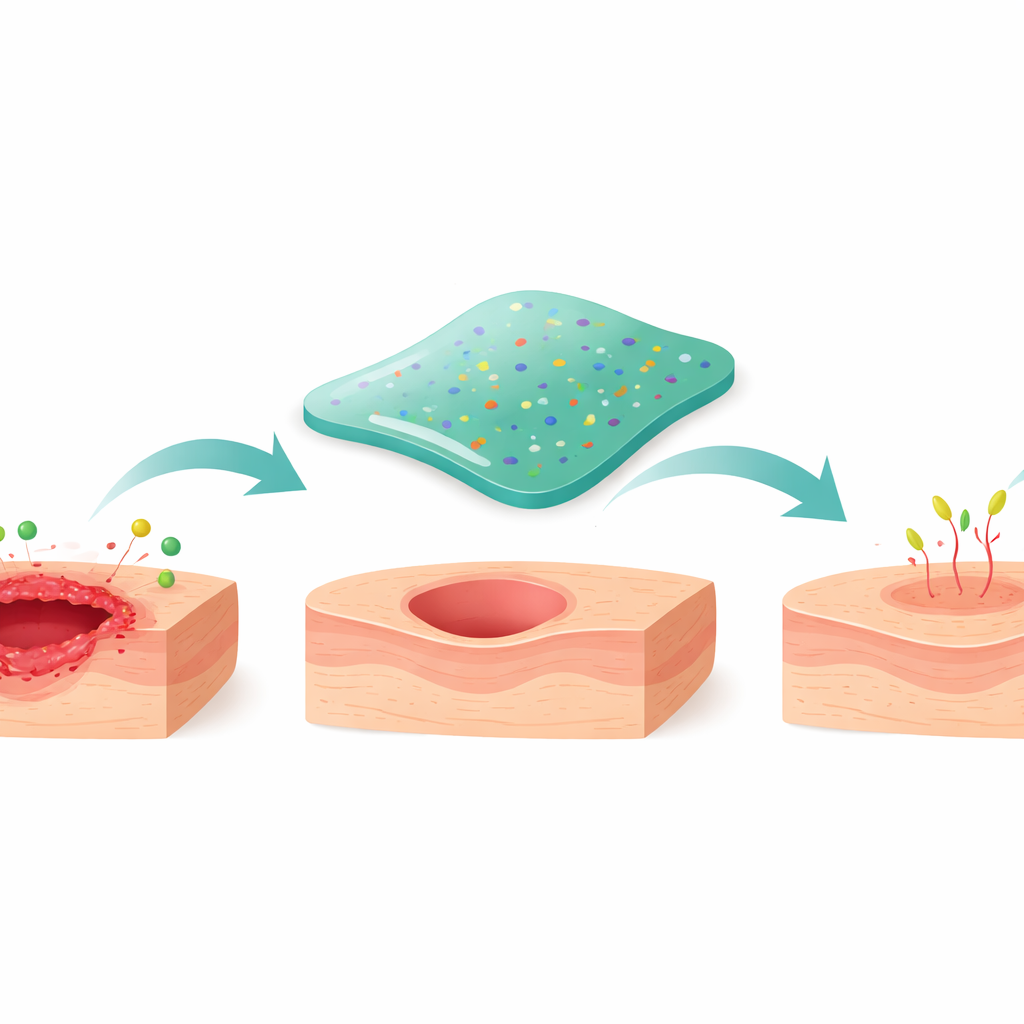
设计为能固定且自愈
伤口敷料必须能贴附在潮湿且会运动的皮肤上、吸收渗出液并保持完整。详尽的物理测试显示,优化后的凝胶(称为ASFH-L)表现为类软固体:它可变形以贴合伤口表面,同时抵抗流动。在显微镜下,其呈现出相互连通的孔隙结构,孔径足以让营养物质和细胞通过,但又不至于松散到解体。当被拉伸或短暂损伤时,其基于铜的连接可重新形成,赋予水凝胶“自愈”能力,使被切开的片段在几分钟内重新融合。在潮湿的猪皮上,ASFH-L在反复弯曲和扭动的水下环境中仍能保持附着,提示其在真实伤口处可在无需频繁更换的情况下提供保护。
抗菌并促进皮肤细胞迁移
慢性糖尿病伤口常被细菌侵扰。在针对金黄色葡萄球菌和大肠杆菌等常见病原体的体外测试中,所有版本的水凝胶均抑制了细菌生长,且含有更多肝素内酯的凝胶产生了更大的抑菌圈。同时,ASFH-L提取物对人体皮肤细胞温和,在合适剂量下24小时内保持细胞活力并促进其增殖。当在高糖环境中培养本会削弱细胞迁移能力的皮肤细胞时,加入凝胶提取物可加速细胞向划痕缺口迁移。这一迁移能力的提升很重要,因为伤口愈合依赖于皮肤细胞爬行以覆盖裸露区域。
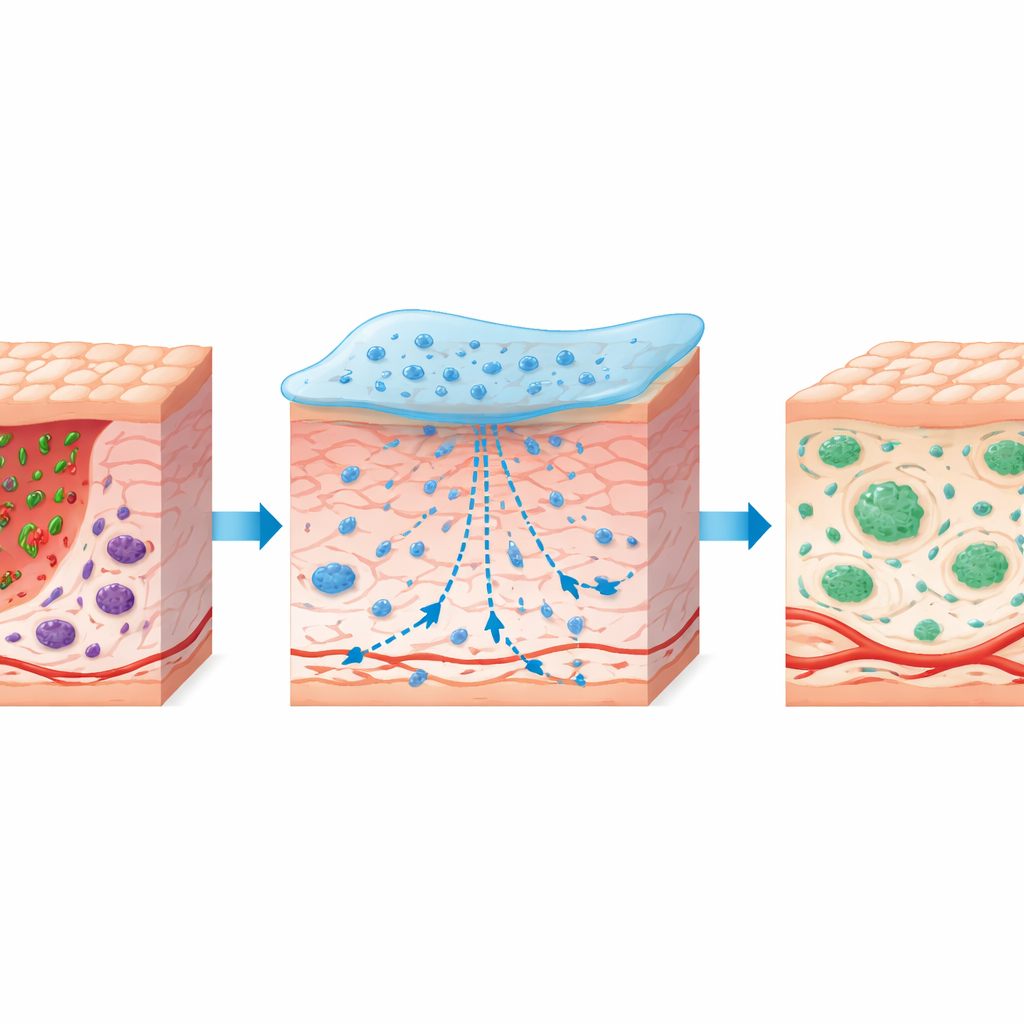
引导机体从炎症走向修复
在带有圆形背部伤口的糖尿病小鼠模型中,与未处理对照组及不含植物药物的类似凝胶相比,ASFH-L水凝胶加速了伤口闭合。接受治疗的伤口显示出更厚的新表皮、更有序的胶原纤维,甚至毛囊再生。血流成像和组织染色显示小血管网络更为致密,且周围支持性的肌样细胞更多,提示更好的营养供给。在免疫水平上,该敷料改变了巨噬细胞的行为——这种一线防御细胞可分为促进炎症的M1型或抑制炎症并支持重建的M2型。ASFH-L减少了促炎的M1群体并扩大了促愈合的M2群体,同时降低了IL‑1β和TNF‑α等有害信号并增加了抚慰性因子IL‑10。这种协调性的转变类似于从早期“清理”阶段向真正组织修复转变的自然过程,而这一过程在糖尿病伤口中常被阻滞。
一个促进愈合的分子开关
为理解凝胶中的植物成分如何协调这些效应,研究组使用了计算建模、数据库挖掘和生物物理测量。他们发现肝素内酯可以直接与一种小型信号蛋白Rac1结合,并通过其激活一系列分子(JNK1、Jun和Fos),这些分子共同调控细胞迁移、增殖、炎症和新血管形成。模拟显示肝素内酯与Rac1之间具有稳定且能量有利的结合,基于表面的实验也实时证实了这一相互作用。在小鼠伤口中,沿Rac1/JNK1/Jun/Fos轴的基因与蛋白在凝胶处理组中活性更高。简而言之,该敷料不仅覆盖伤口;它递送了一种植物成分,从而在细胞内开启了固有的修复开关。
这对患者可能意味着什么
这项工作提出了一种“智能”敷料,将抗感染、免疫镇静和血管生成整合到单一的自愈水凝胶平台中。通过利用铜离子提高肝素内酯的溶解性并实现缓慢释放,该材料将一种难以递送的植物化合物转化为可行的局部治疗方式。在糖尿病动物中,这一策略加速了伤口闭合、规范了疤痕组织并重新平衡了免疫反应,同时作用于明确的分子通路。尽管仍需进行人体试验,但这一概念指向未来能做得远不止覆盖伤口的敷料——它们可以主动引导受损组织完成愈合的每一步。
引用: Ye, P., Dai, Y., Zhang, Q. et al. Novel copper-ion coordinated andrographolide-loaded hydrogel activates Rac1/JNK1 axis for enhancing diabetic wound healing. npj Regen Med 11, 14 (2026). https://doi.org/10.1038/s41536-026-00457-y
关键词: 糖尿病伤口愈合, 水凝胶敷料, 肝素内酯(andrographolide), 巨噬细胞极化, 血管生成