Clear Sky Science · zh
抑制 CDK8 可挽救因缺血导致的骨折愈合受损
血液供应在骨折时为何至关重要
大多数骨折最终会自我愈合,但每年仍有数百万人出现愈合停滞。围绕骨折部位的血流不足——即缺血——会显著增加骨折愈合缓慢、愈合不良或不愈合的风险。本研究从细胞水平探讨了这种情况发生的原因,并测试了一种实验性口服药物,该药物似乎能将修复过程从瘢痕样修复引导回真正的骨再生。
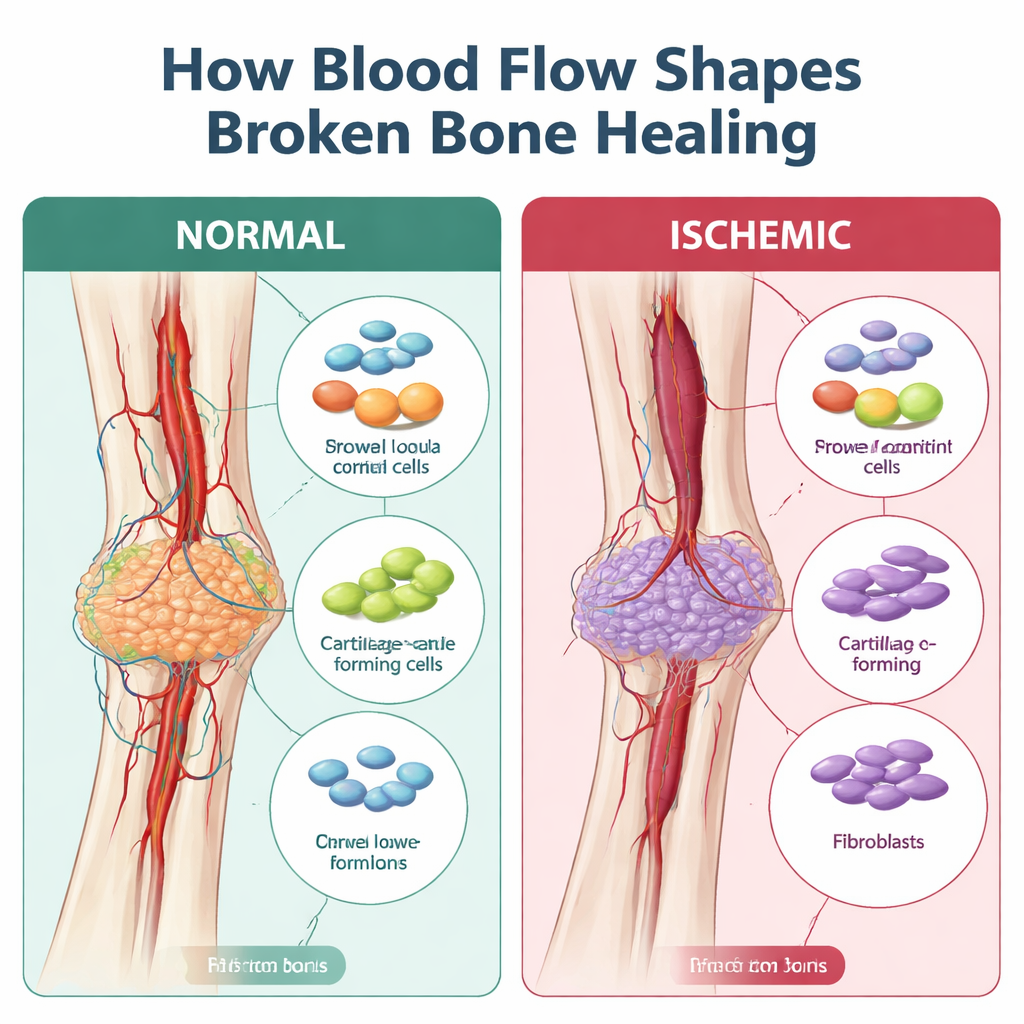
愈合转向瘢痕化而非重建时发生了什么
骨骼通常通过先形成软性软骨桥,然后逐步被硬骨替代来愈合。这个称为骨痂的桥依赖于一群类干细胞的支持细胞、免疫细胞和血管的供应来协调修复。在缺血性骨折中,以前的研究表明骨痂往往更小、更脆弱且充满纤维组织,更像瘢痕而非坚固的新骨。尚缺乏的是一张详尽的图谱,说明在这一偏离正常愈合的过程中,哪些细胞在何时出现异常。
单细胞显示通向纤维化的偏路
研究人员使用了一种小鼠模型,在骨折时通过外科损伤腿部动脉,近似模拟严重损伤或血管疾病、吸烟者中见到的血流丧失。然后他们对骨折骨痂在受伤后第4天和第7天的成千上万个单细胞进行了单细胞 RNA 测序,这是一种读取单个细胞中活跃基因的技术。在血供良好的骨折中,早期骨痂充斥着免疫细胞,随后逐渐被扩增的基质细胞取代——这些支持细胞会成为软骨和骨。在缺血条件下,形成软骨和骨的细胞明显减少,而成纤维细胞增多,成纤维细胞是铺设纤维组织的细胞。计算性的“轨迹”分析显示,缺血骨中的基质细胞往往不是平滑地从早期祖细胞成熟为软骨,而是经过一种类成纤维细胞状态偏离路径,这与显微镜下观察到的更像瘢痕的骨痂一致。
对成骨细胞的分子制动
深入分析这些细胞的基因活动,团队发现缺血骨痂存在强烈的细胞应激信号,包括高表达热休克蛋白。其中最显著的变化之一是名为 Cdk8 的基因活性激增,该基因编码的调控酶位于一个主要的转录复合体中,能够减缓或重定向细胞对信号的响应。Cdk8 在其他背景下已被发现会阻止细胞分化。在本研究中,Cdk8 在缺血骨的早期基质祖细胞中特别升高。在低氧实验条件下培养的人类间充质基质细胞——模拟血流不足——也上调了 CDK8,直接将氧气短缺与这一可能对软骨和骨形成的“制动”联系起来。
关闭 CDK8 以挽救修复
研究人员接着探问阻断 CDK8 是否能让基质细胞恢复正常愈合能力。在细胞培养中,用选择性 CDK8 抑制剂处理小鼠和人类祖细胞可以提升关键的软骨基因并增加软骨基质的生成,同时当这些细胞被诱导向成骨方向分化时,矿化也有所增强。团队随后在缺血骨折小鼠中测试了一种可口服的 CDK8/19 抑制剂 SNX631-6。在早期软骨形成窗口给予该药物时,骨痂中的软骨量增加;当治疗延长至软骨向骨转变的后期阶段时,骨痂在微型 CT 扫描和组织切片上显示出更多的总骨量、更高的矿物质含量和更大的整体体积,表明结构修复更为强健。
从实验室发现到潜在新疗法
综合来看,结果表明缺血通过上调 CDK8 在一定程度上将愈合细胞引导向应激性、纤维化的命运,从而抑制它们成为软骨和骨的能力。阻断该酶似乎可以释放这种制动,使早期形成更多软骨,后期沉积更多骨,即使在血供受限时也是如此。由于 CDK8 抑制剂已在癌症患者中开展试验,它们有朝一日可能被重新用于帮助那些高风险骨折愈合不良的人群——例如老年人、吸烟者或有血管疾病者——重新长出坚固的骨骼,而不是脆弱的瘢痕组织。
引用: Capobianco, C.A., Song, M.J., Farrell, E.C. et al. Inhibition of CDK8 rescues impaired ischemic fracture healing. npj Regen Med 11, 12 (2026). https://doi.org/10.1038/s41536-026-00456-z
关键词: 骨折愈合, 缺血, CDK8 抑制剂, 间充质基质细胞, 纤维化