Clear Sky Science · zh
在角膜基质细胞中激活的Hedgehog信号导致基质僵硬并损害角膜再生
为什么眼睛的透明窗会变得混浊
角膜是眼睛的前窗,其透明性对于清晰视力至关重要。然而,烧伤、外伤和某些疾病可以使这层透明组织变得浑浊并形成瘢痕,有时会导致失明。本研究提出了一个简单但重要的问题:为什么有些角膜可以干净愈合,而有些则留下长期损伤?作者关注角膜内支持细胞与受伤后恢复光滑、透明表层的上皮细胞之间的一种隐秘对话。
表面下的隐秘支持细胞
角膜的大部分由一种坚韧而透明的中间层——基质组成。它充满有序的胶原纤维和分散的细胞,称为角膜基质细胞(keratocytes)。在健康成年眼中,这些基质细胞处于静息但活跃的状态:它们维护胶原框架并释放滋养表面上皮的生长因子,而上皮层则由角膜边缘的干细胞持续更新。研究者发现,在幼年小鼠中,一种称为Hedgehog的分子通路在这些基质细胞中是活跃的,但随着眼睛成熟而关闭。当他们在成年基质细胞中基因性阻断Hedgehog信号时,角膜仍然表现正常,这表明在健康、透明的角膜中,静息而非持续活跃才是该通路的自然状态。
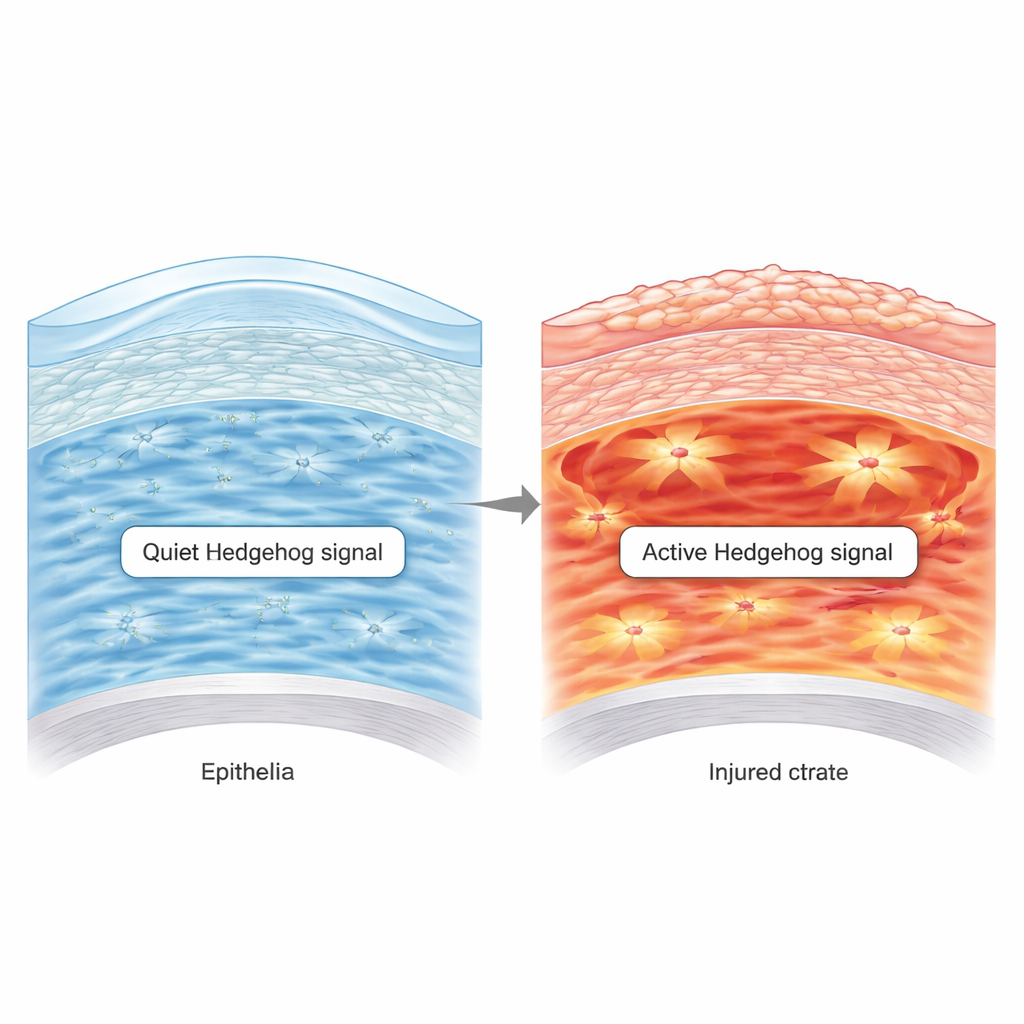
化学灼伤唤醒沉睡通路时发生了什么
角膜表面的浅表擦伤通常在一到两天内愈合:干细胞分裂、新的上皮细胞迁入,而基质大体保持稳定。化学灼伤则具破坏性得多。在一种碱性灼伤小鼠模型中,团队观察到长期缺陷——表层变薄、分层差,而基质紊乱。他们发现化学损伤后,Hedgehog信号在基质细胞中被强烈再激活,而简单的擦刮后则没有。这一激增与炎性分子有关,尤其是细胞因子TNF‑α,作者在体外培养的基质细胞中显示TNF‑α能直接开启Hedgehog程序。结果表明,灼伤后的严重炎症将通常处于静息的基质细胞推入一种有害的过度活跃状态。
从有益的维护者到僵硬的瘢痕制造者
为了解Hedgehog持续开启时会发生什么,科学家构建了基质细胞中Hedgehog长期激活的小鼠模型。即使在没有损伤的情况下,这些角膜也逐渐出现更薄、更僵硬的基质。对分离基质细胞的基因谱分析显示,它们在改变身份:经典的基质细胞标志物减少,而成纤维细胞和类间充质干细胞相关基因增多。与此同时,关键细胞外基质成分的产生——例如胶原和一种叫角膜蛋白(keratocan)的结构蛋白——下降。在显微镜下,胶原纤维变得拥挤,而机械测试显示基质组织的刚度比正常高出两倍以上。这些改变将支持性基质转变为刚性支架,这是瘢痕组织的标志。
僵硬的“床”如何阻止表面愈合
故事中一个出人意料的转折来自角膜表面。在基质细胞中Hedgehog长期激活的小鼠中,上皮最初按时闭合伤口,但随后未能正确成熟。表层保持薄弱,存在许多未成熟细胞而成角膜特异性、完全分化的细胞很少。团队将这一缺陷追溯到上皮细胞的机械信号系统——Hippo–YAP通路,该通路感知下方组织的硬度。在僵硬的基质中,Hippo信号被开启,进而抑制了YAP,而YAP通常促进健康的分化。当研究者应用小分子抑制剂抑制Hippo信号时,YAP活性恢复,上皮层接近恢复到正常的厚度和结构——即使基质本身仍然较薄。这表明基质“床”的刚性可以直接决定表面能否正确重建。
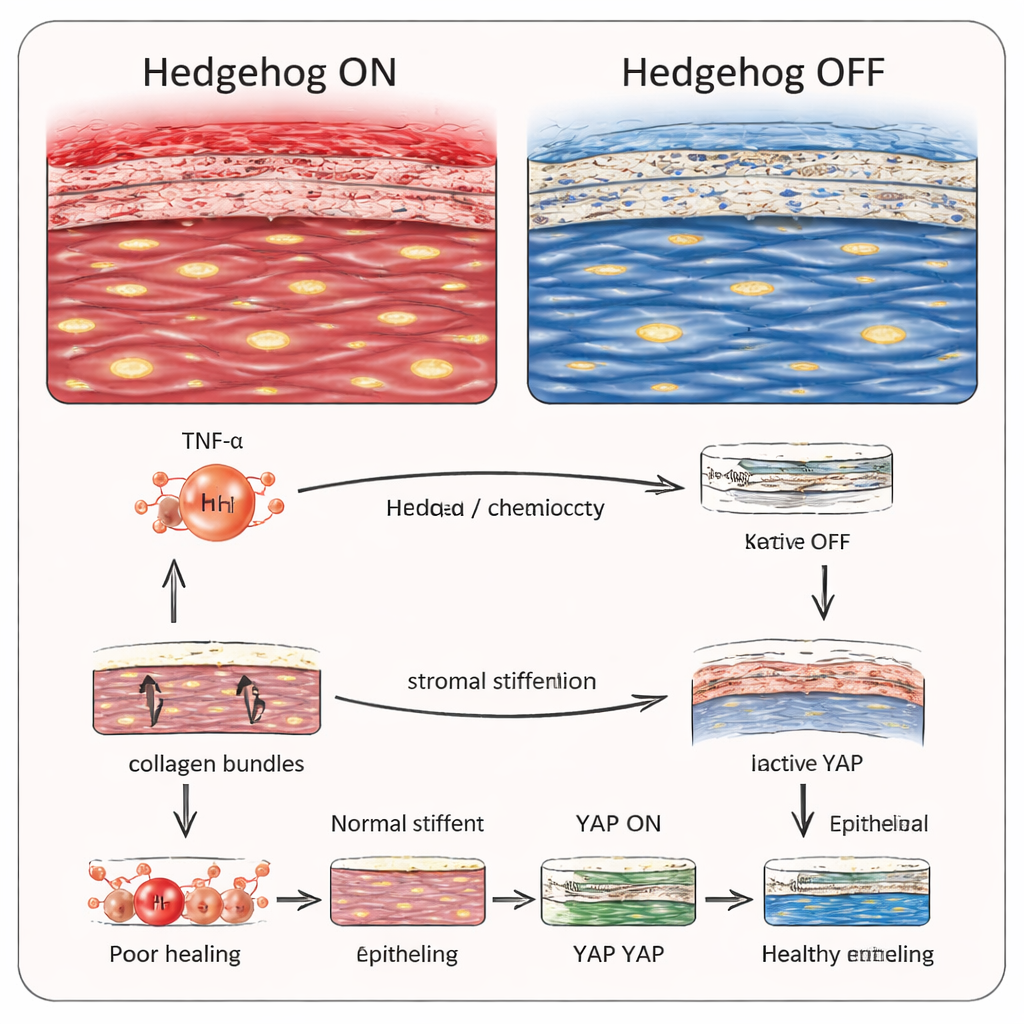
通过抑制Hedgehog拯救视力
工作中最令人鼓舞的部分来自将Hedgehog信号调低的实验。在基因性激活Hedgehog的小鼠中,使用阻断该通路关键转录因子的药物能恢复基质结构并挽救表面细胞的分化。在另一组实验中,缺失基质细胞中核心Hedgehog成分的小鼠在化学灼伤后免于常见的瘢痕形成和上皮缺陷。最后,在正常小鼠碱性损伤后将阻断Hedgehog的药物直接应用于眼睛,也明显改善了角膜结构且无明显副作用。对普通读者而言,结论是:角膜支持细胞中过度激活的“修复”通路反而会通过使组织僵硬并干扰表面细胞,破坏愈合。通过谨慎抑制该通路,或许可以引导角膜朝清晰而非混浊方向愈合,为治疗化学灼伤及其他如糖尿病相关的慢性愈合障碍提供一种新途径。
引用: Yu, Q., Li, P., Du, Z. et al. Activated Hedgehog signaling in keratocytes leads to stromal stiffness and impairs corneal regeneration. npj Regen Med 11, 9 (2026). https://doi.org/10.1038/s41536-026-00453-2
关键词: 角膜伤口愈合, Hedgehog信号, 基质僵硬, 角膜基质细胞, 化学性眼损伤