Clear Sky Science · zh
在过表达人类野生型α-突触核蛋白的帕金森病转基因小鼠模型中,嗅觉感受图被扰动
为何嗅觉丧失在帕金森病中重要
许多人将帕金森病视为运动障碍,但对大多数患者而言,最先受损的往往是嗅觉。这种丧失可能在震颤或僵硬出现前数十年出现,使其成为一个强有力的早期预警信号。本文所述的研究探讨了一个基础但尚未解答的问题:当与帕金森病相关的变化开始时,大脑的嗅觉回路究竟发生了什么?通过在一个精心设计的小鼠模型中研究这一问题,研究者揭示了一个关键的帕金森蛋白如何扰乱大脑内部的“气味地图”,并指向一种新的、易于获得的早期疾病线索来源。
大脑的嗅觉地图
我们的鼻腔包含数以百万计的专门化嗅觉细胞,每种细胞对特定的气味分子作出反应。这些细胞将细长的纤维投射到大脑前部,在嗅球内汇聚成称为球囊的小型中枢。每种气味激活特定的球囊模式,形成一幅精确的感受图,使大脑能区分咖啡与肉桂、烟雾与香水。在健康小鼠中,表达同一嗅觉受体的细胞(称为M72)与另一类(称为P2)可靠地各自投射到每个嗅球的两个明确球囊,形成高度有序且可重复的地图。
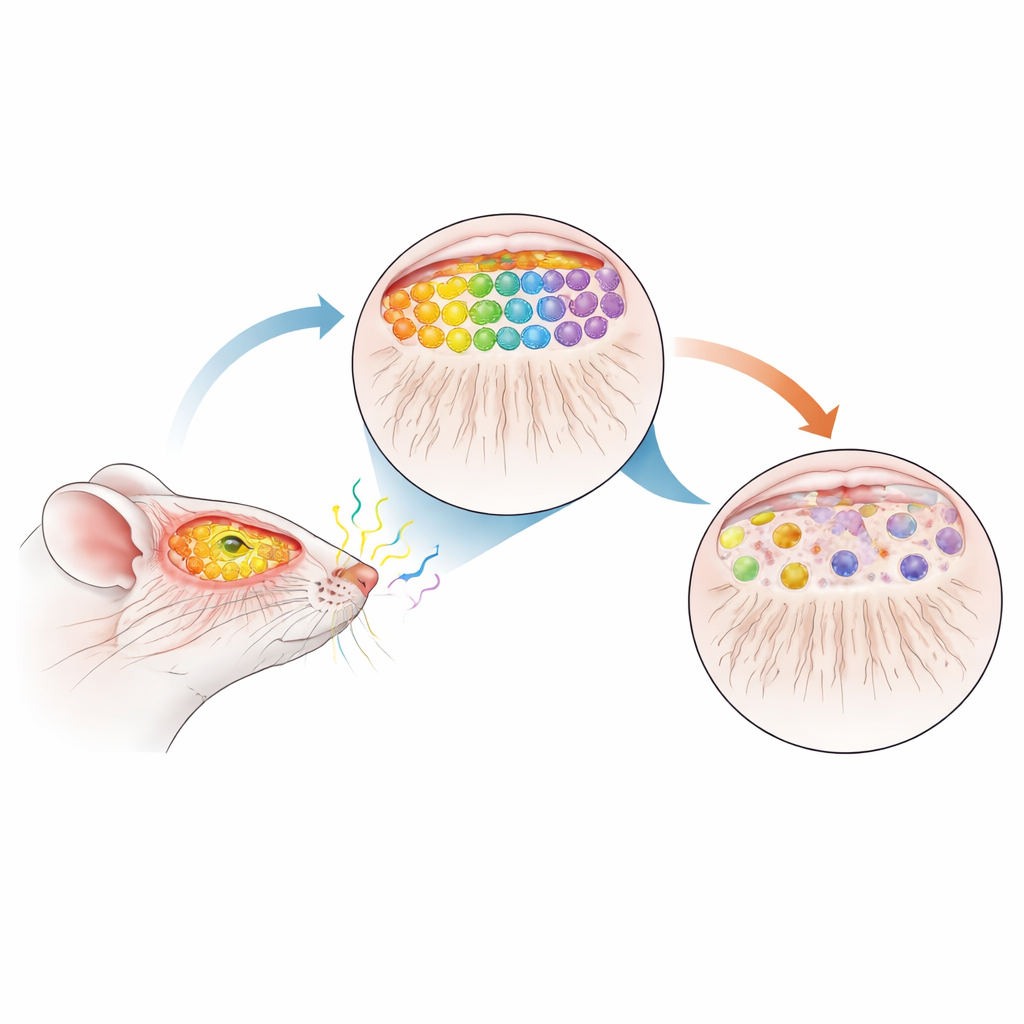
用于模拟早期帕金森病的小鼠模型
为观察帕金森病可能如何扰乱这幅地图,研究团队使用了过度产生人类正常α-突触核蛋白的小鼠——这正是在人类帕金森大脑中发生聚集的蛋白。他们随后将这些小鼠与带有M72和P2标记的小鼠交配,以便可视化追踪特定嗅觉细胞及其连接。重要的是,额外的α-突触核蛋白仅在出生后被激活并随年龄逐渐积累,模拟了人类疾病缓慢、进展性的过程。在12个月龄时——大鼠的中年阶段,可比作人类的前驱期或诊断前阶段——研究者对这些动物的嗅觉系统进行了详细检查。
当嗅觉地图瓦解时
通过染色这些被标记的神经元并追踪它们的路径,科学家们在过表达α-突触核蛋白的小鼠中发现了嗅觉地图显著的崩溃。鼻腔中M72和P2神经元的数量急剧下降——M72约损失四分之三,P2近一半——它们通往嗅球的纤维也大幅减少。原本应整齐汇聚为两个稳健球囊的纤维,剩余者常常形成多个更小且大小、位置各异的球囊。这些“额外”中枢在不同小鼠间并不出现在一致的位置,表明正常拓扑精确性的丧失。嗅觉细胞末梢的一个广泛标志物VGLUT2在嗅球中也下降了约44%,表明这种退行性变化远超这两种被标记的受体类型。
将回路破坏与嗅觉丧失联系起来
结构损伤转化为可测量的嗅觉问题。年长的α-突触核蛋白小鼠在寻找隐蔽食物时耗时更长、分辨不同气味的能力更差,并且不会偏好标有自身气味的区域——这些行为学测试共同显示出嗅觉减退和气味辨别受损。它们还需要更高浓度的气味才会有反应,显示出敏感性下降。这些缺陷在较年轻的小鼠中并未出现,而这些年轻鼠的被标记神经元及其地图仍大体正常,将功能丧失的时机与随后感觉地图的瓦解而非早期发育问题联系在一起。值得注意的是,尽管致病蛋白在嗅球中丰富,但在鼻腔的感受上皮中并未检测到,这指向嗅球内部回路的变化——特别是将嗅觉信息传递出去的颗粒细胞/投射细胞(如粒-主细胞)——很可能是地图紊乱的驱动因素。
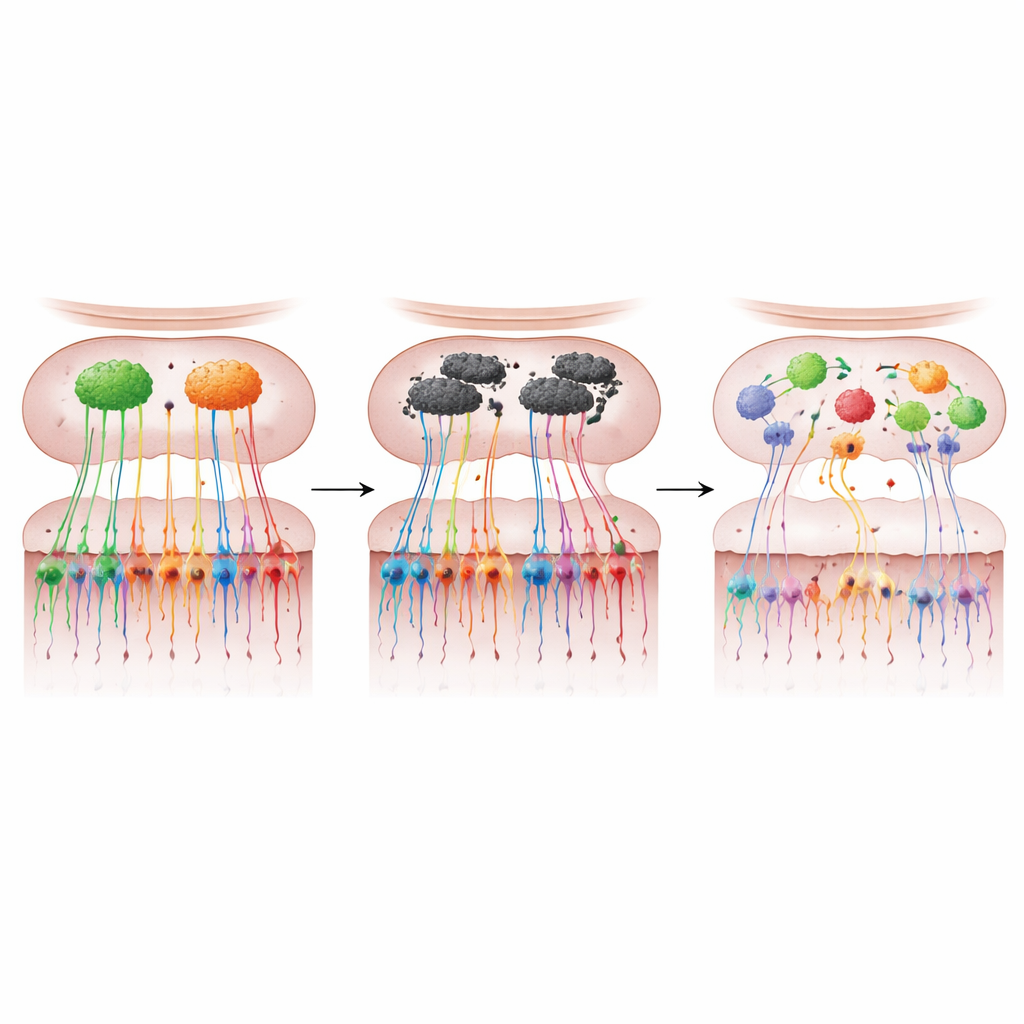
嗅觉细胞:洞察早期疾病的窗口
综合来看,这项工作为非专业读者传达了一个明确信息:在这个类帕金森小鼠模型中,嗅球中α-突触核蛋白的过度产生导致嗅觉神经元的丧失与错误连线,扭曲了大脑的气味地图并引发早期嗅觉问题。由于鼻腔的感受细胞在发育上与大脑相关联,但可以通过微创拭子或活检采样,作者认为在人类中发生的类似变化可能成为强有力的帕金森病早期生物标志物。他们建议,对这些细胞的分子指纹进行绘制,不仅有助于在运动症状出现前数年识别出高风险个体,还可能为理解疾病如何起始与传播——以及如何减缓或预防——提供新的见解。
引用: Biju, K.C., Hernandez, E.T., Stallings, A.M. et al. Olfactory sensory map is perturbed in a human wild-type α-synuclein overexpressing transgenic mouse model of Parkinson’s disease. npj Parkinsons Dis. 12, 70 (2026). https://doi.org/10.1038/s41531-026-01288-w
关键词: 帕金森病, 嗅觉功能障碍, α-突触核蛋白, 感受图, 生物标志物