Clear Sky Science · zh
LRRK2R1627P 突变放大环境风险因素引起的大鼠肠道慢性炎症及α-突触核蛋白聚集
为何肠道在一种脑病中很重要
帕金森病以震颤和运动障碍最为人所知,但越来越多的证据表明,其根源可能远离大脑,深藏于肠道。本研究探讨了一种在亚洲人群中与帕金森病相关的特定基因变异,如何与衰老和毒物暴露共同作用,逐步损伤大鼠的肠道。通过在动物一生中观察肠道发生的变化,研究者追踪了日常免疫防御如何转向慢性炎症,从而为疾病相关蛋白的积累创造条件,这些蛋白最终可能威胁大脑。
消化道中的高风险基因
科学家们聚焦于名为 LRRK2 的基因的一个变体,该基因长期以来与帕金森病和某些炎症性肠病相关。他们制造了携带相应突变、称为 LRRK2R1627P 的大鼠,并与正常大鼠在生命周期内进行比较。尽管肠道中 LRRK2 基因的转录水平未见变化,但总的 LRRK2 蛋白及其一个关键活性标志物减少,表明该突变削弱了该蛋白在肠道中的正常功能。这种微妙的分子改变并未导致早期明显损伤,但在动物随年龄增长时,悄然改变了肠上皮细胞的更新和组织方式。
在缓慢而持续压力下的老化肠道
随着时间推移,携带突变的大鼠出现了明显的肠道结构异常。小肠变短,用于吸收营养的绒毛和隐窝变小。上皮中产生保护性黏液与抗菌物质的特殊细胞——杯状细胞和潘氏细胞减少,同时帮助相邻细胞形成紧密、抗渗漏连接的蛋白也下降。显微镜下,这些连接变得更短或更宽,提示屏障功能减弱。重要的是,整体结构并未崩溃;相反,肠道呈现出较为隐匿的更新与防护能力下降模式,这会使其更易受刺激和感染。 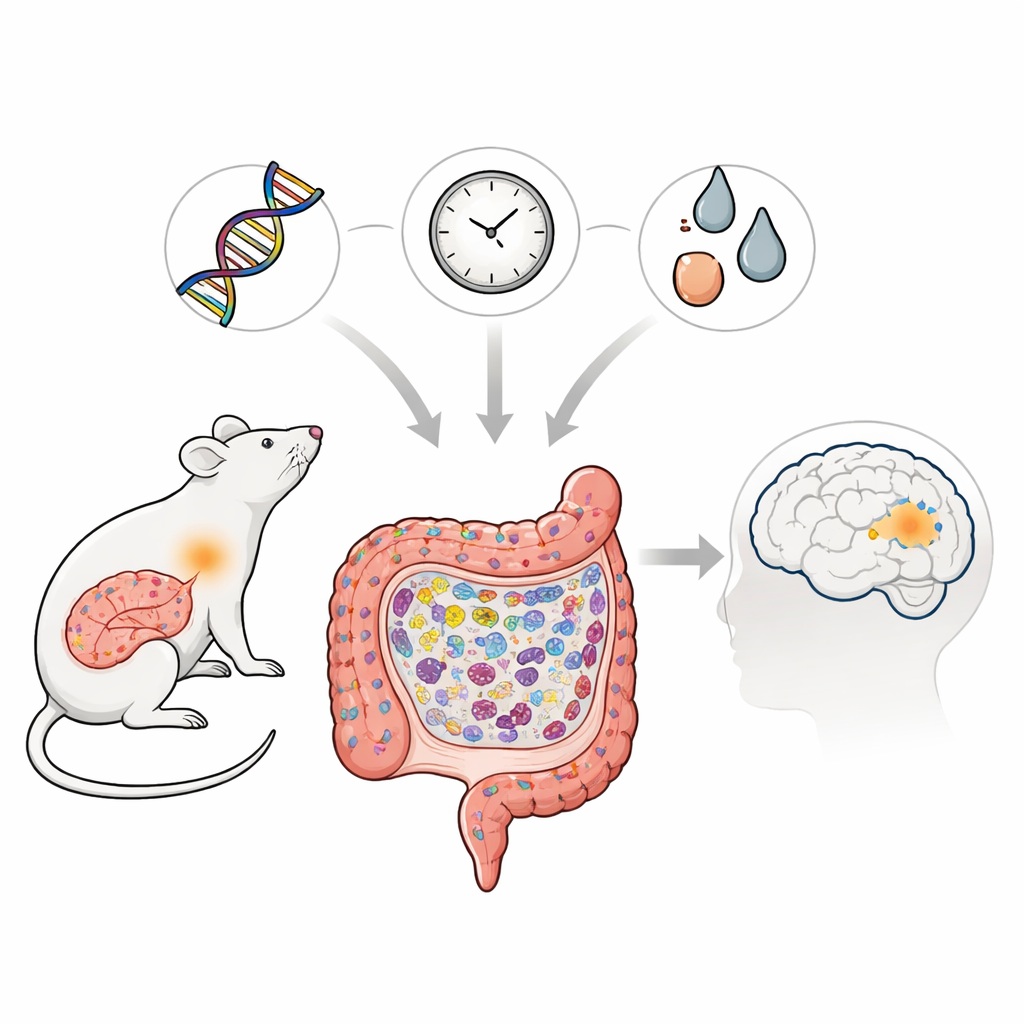
处于高度兴奋的免疫系统
为了解肠道为何失衡,研究团队检查了肠道壁的基因表达和免疫细胞。他们发现与传感器 TLR4 及其伴侣 NF-κB 相关的通路在年长突变大鼠中异常活跃。这些传感器通常帮助机体识别有害微生物,但在此情形下驱动了以“先打再说”为特征的 M1 巨噬细胞积累。这些细胞大量分泌炎症分子,使肠道处于慢性刺激状态。值得注意的是,与帕金森病相关的蛋白α-突触核蛋白(以其疾病关联的磷酸化形式)并未在肠神经元中积累,而是在小肠内这些被激活的巨噬细胞中堆积,尤其在年长动物中更为明显。
对环境冲击更为敏感
单靠基因突变并不能解释全部。在对年轻大鼠短暂暴露于细菌毒素(LPS,刺激 TLR4)时,携带 LRRK2 突变的动物出现比正常对照更严重的肠道炎症。它们的肠上皮脱落更多,屏障蛋白进一步下降,促炎性的巨噬细胞激增,再次伴随异常α-突触核蛋白的积累。这提示携带类似突变的人可能对扰乱肠道的环境损伤(如某些感染或毒物)格外敏感,从而放大其长期风险。
关闭警报信号
由于 TLR4 处于这场炎症风暴的核心,研究团队测试了一种专门抑制 TLR4 信号的药物 TAK-242。将该抑制剂在数月内给予中年大鼠,结果在很大程度上恢复了小肠的长度、绒毛与隐窝尺寸、黏液产生细胞及屏障蛋白。它减少了过度活化的巨噬细胞,降低了炎症分子,并显著减少了肠道中异常α-突触核蛋白的积累。同时,它也纠正了失衡的微生物群:多样性增加,乳酸杆菌的过度增殖减轻,若干有益细菌群体回升,预测的微生物功能也从与疾病相关的模式转变。 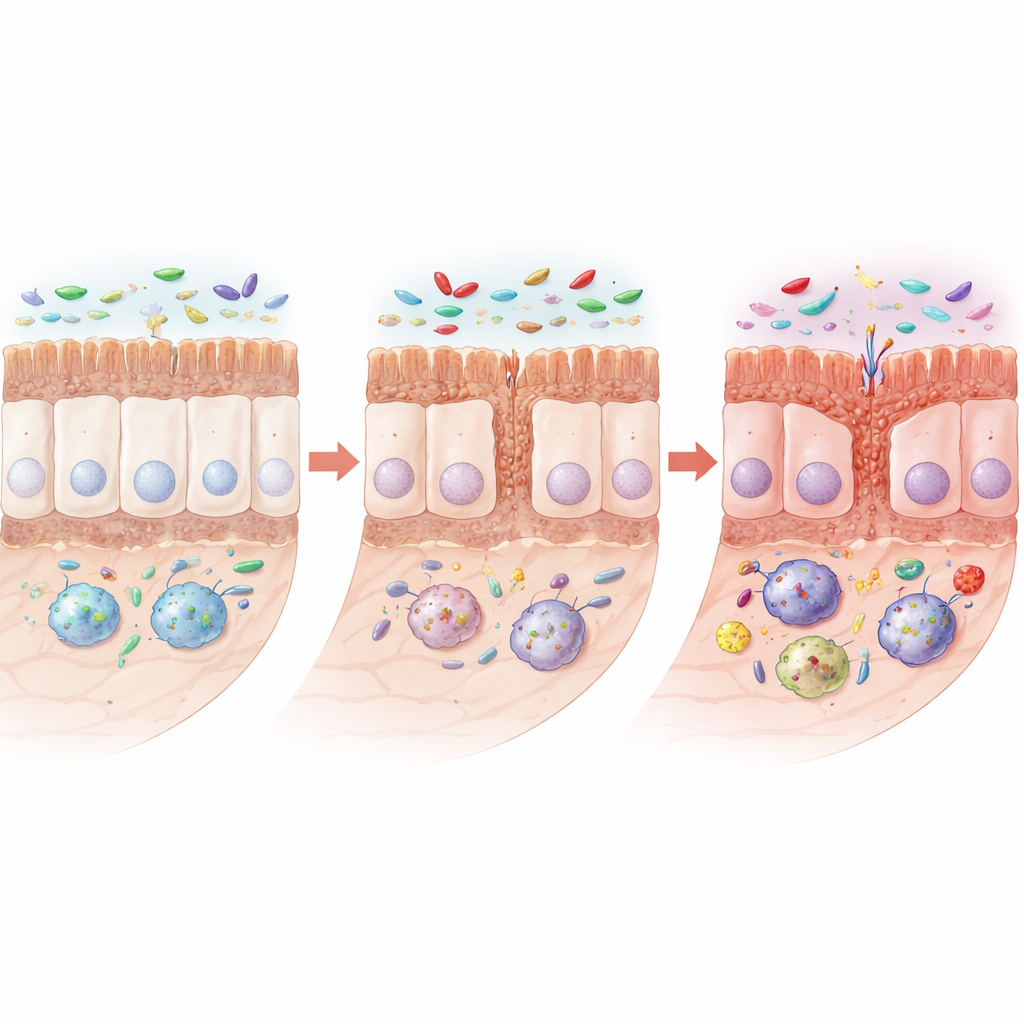
这对帕金森风险意味着什么
对非专业读者而言,结论是“帕金森基因”可能随着时间悄然重塑肠道的免疫防御,特别是在衰老与环境压力存在时。在这些大鼠中,结果是慢性、低水平的炎症削弱了肠道屏障,扰乱了常驻微生物,并导致与帕金森相关的蛋白在免疫细胞中积累——这尚非完全发作的帕金森病,但构成了可能有利于将来脑部疾病发生的生物学环境。研究显示,阻断单一肠道免疫通路即可逆转许多这些变化,突出了肠道作为切实可行的早期靶点:保护肠道健康并抑制肠道炎症或有助于延缓或预防携带遗传风险者的帕金森病。
引用: Pang, S., Lu, J., Wang, Y. et al. LRRK2R1627P mutation amplifies environmental risk factors induced chronic inflammation and α-synuclein aggregation in the gut of rats. npj Parkinsons Dis. 12, 68 (2026). https://doi.org/10.1038/s41531-026-01281-3
关键词: 帕金森病, 肠道炎症, LRRK2 突变, 微生物组, 先天免疫