Clear Sky Science · zh
系统评估线粒体形态调控因子以改善神经元α-突触核蛋白病变
为何这些微小“发电站”在脑病中至关重要
线粒体,作为细胞的“发电厂”,对维持神经元存活及其连接功能至关重要。在帕金森病等脑部疾病中,这些微小结构常常表现出受损或破碎的形态,但很难判定哪些变化是有害的以及我们可以安全地调节哪些开关来保护它们。本研究在一种帕金森相关蛋白累积的实验模型中系统性地检测了关键的线粒体“形态调控因子”,并借助人工智能工具在神经元不同区域内测量线粒体形态。研究结果指出了一个特定的调控因子——Fis1,作为在不引起新副作用的情况下维持线粒体和突触健康的有前景靶点。
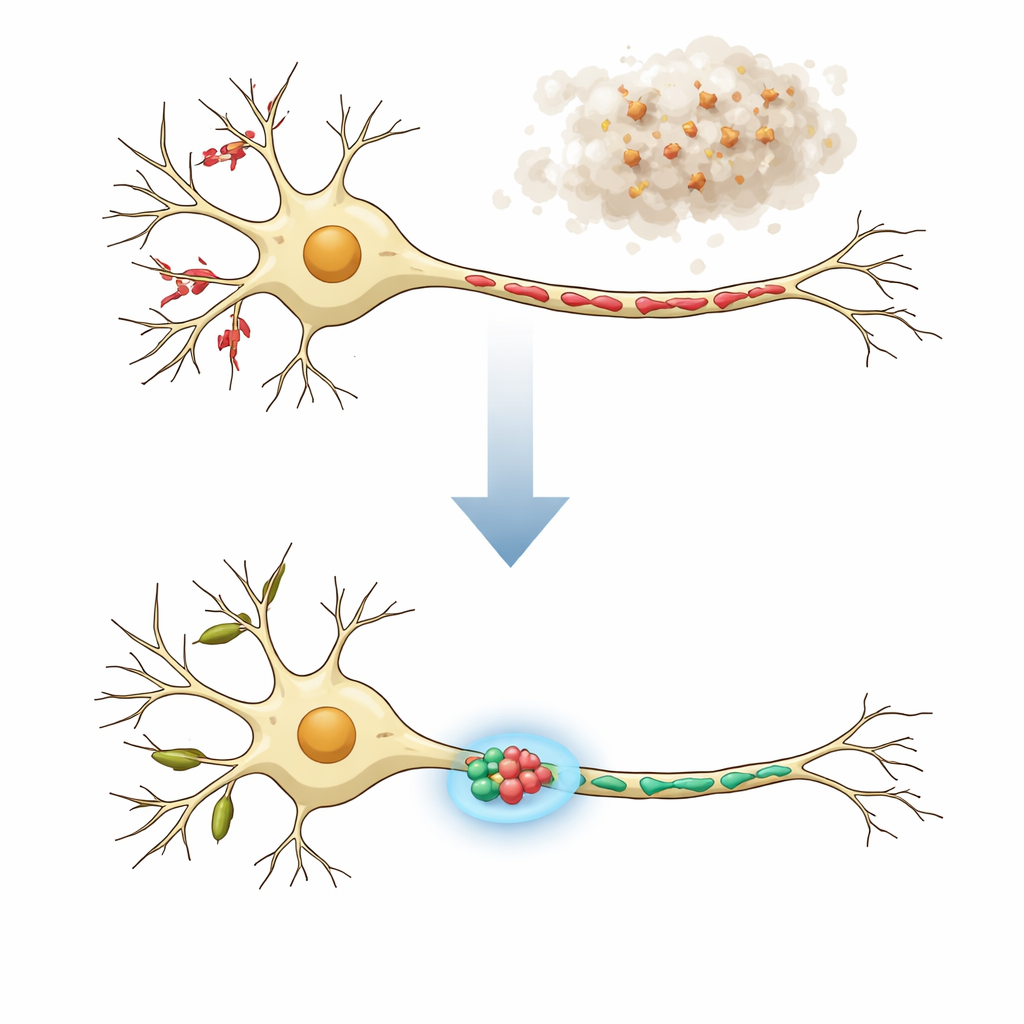
神经元的两个“社区”
神经元并非均质:其树状分支(树突)和长长的轴突承担不同任务,且所含线粒体形态迥异。在健康神经元中,树突中往往含有较长的管状线粒体,有助于支持局部蛋白质合成和树突棘处的灵活通信;而负责发送信号的轴突则携带许多较短的线粒体,供能并帮助控制突触前末梢的钙水平。在神经退行性疾病中,这些线粒体的功能与结构都可能受扰,表现为碎裂、肿胀或串珠状。作者推断,真正有效的治疗必须将树突和轴突中的线粒体分别恢复到各自正常的、区室特异的形态。
构建类帕金森的应激测试
为模拟帕金森病及相关疾病的一个关键特征,研究人员将培养的鼠皮层神经元暴露于预成纤维化的α-突触核蛋白,这种蛋白能聚集成有害的团块。数日内,这些纤维作为种子在细胞内诱发异常的α-突触核蛋白累积,并导致树突和轴突中的线粒体明显碎裂。研究团队使用MitoVis这一深度学习图像分析系统,能够在显微镜图像中自动区分树突与轴突,并测量每幅图像中数百个线粒体的长度、面积与形状,其速度约为人工描画的十倍。该高通量方法确认了疾病样状态使线粒体变短并更趋圆形,这与动物模型和患者组织的报告一致。
测试线粒体形态的开关
接着,研究团队探讨是否通过调整特定的融合与分裂蛋白可以阻止这种损伤。增强两种融合蛋白(Mfn1和Mfn2)或下调一种分裂蛋白(Mff)确实能保护树突线粒体免受α-突触核蛋白诱导的缩短,并维持树突棘不被丢失。然而,这些相同操作使轴突线粒体过度变长,而既有研究将轴突线粒体过长与突触释放与轴突分支问题联系在一起。相比之下,下调另一种分裂蛋白Fis1能在不导致过度延长的情况下,将树突和轴突的线粒体长度恢复到近似正常值。重要的是,在该实验条件下,降低Fis1并未导致神经元死亡,并且像其他干预一样,保护了在α-突触核蛋白胁迫下本会缩小的树突棘密度。
维持钙稳态
鉴于轴突内的线粒体在电活动期间有助于缓冲钙,研究人员检验了改变线粒体形态是否会扰乱这一微妙平衡。他们使用定位于突触前小泡线粒体的荧光钙传感器,并用短暂的动作电位串刺激轴突。在α-突触核蛋白条件下,略微缩短的轴突线粒体的钙处理表现与正常相似。但当轴突线粒体因过度表达Mfn1或敲低Mff而被拉长时,它们在刺激后比平常吸收更多钙。这种增强的钙摄取可能干扰突触前功能。相反,降低Fis1(将线粒体长度恢复但不超调)保留了与健康对照非常相近的线粒体钙反应,提示更少的隐性权衡。
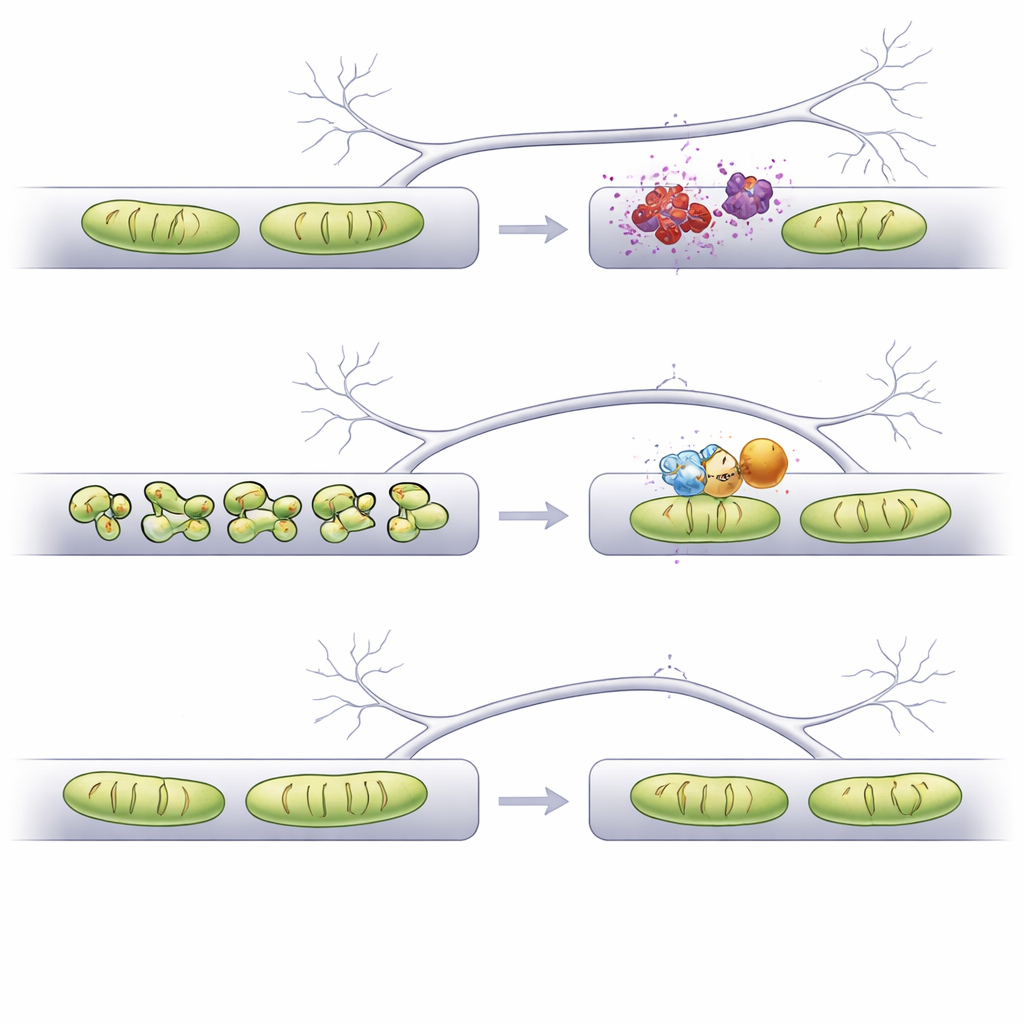
这对未来治疗意味着什么
总体而言,该研究表明单纯让线粒体变长并不足够——关键是将其在恰当区室恢复到合适的尺寸。通过AI辅助的成像流程,作者确定Fis1为一个特别有吸引力的靶点:下调Fis1可在树突和轴突中维持线粒体结构稳定,防止树突棘丢失,并避免突触前终端异常的钙处理。研究结果支持这样一种观点:通过精细调节线粒体形态(例如以靶向Fis1的小分子或反义寡核苷酸),可能有助于保护帕金森相关α-突触核蛋白病变中易受损的突触,并可能对其他线粒体功能失调的脑病产生益处。
引用: Kim, S.Y., Choi, J., Jang, D.C. et al. Systematic evaluation of mitochondrial morphology regulators for amelioration of neuronal α-synucleinopathy. npj Parkinsons Dis. 12, 58 (2026). https://doi.org/10.1038/s41531-026-01277-z
关键词: 帕金森病, 线粒体, α-突触核蛋白, 突触功能障碍, 神经退行性疾病