Clear Sky Science · zh
抑制新生神经酰胺合成减轻帕金森病小鼠模型中的α-突触核蛋白病理
大脑脂质为何与帕金森有关
帕金森病最为人熟知的是手抖和运动迟缓,但在大脑深处正上演着更为隐蔽的灾变。控制运动的神经细胞随着一种名为α‑突触核蛋白的蛋白质凝聚成黏性聚集体而逐渐死亡。本研究显示,一类称为神经酰胺的脂质家族助长了这种损伤——阻断其合成可在小鼠和人类细胞模型中保护神经细胞。该研究指出了一个意想不到且可用药物干预的通路,未来有望不只是缓解症状,而是减缓或预防帕金森病的进程。
来自死后脑组织的线索
为弄清神经酰胺是否参与帕金森及相关疾病,研究人员首先检查了患有路易体痴呆者的死后脑组织——这种疾病与帕金森存在相同的有毒蛋白质聚集体。通过灵敏的化学测定,他们发现许多类型的神经酰胺在中脑区域明显高于健康脑,尤其是那些长链脂肪尾的形式。随后,他们重新分析了人脑细胞的大型基因数据集,发现合成和处理神经酰胺的基因在帕金森患者的多巴胺能神经元中更为活跃,某些支持性细胞如星形胶质细胞和少突胶质细胞中也表现出相似变化。总体而言,这些发现表明在病变大脑中多种细胞类型的神经酰胺平衡受到扰动。
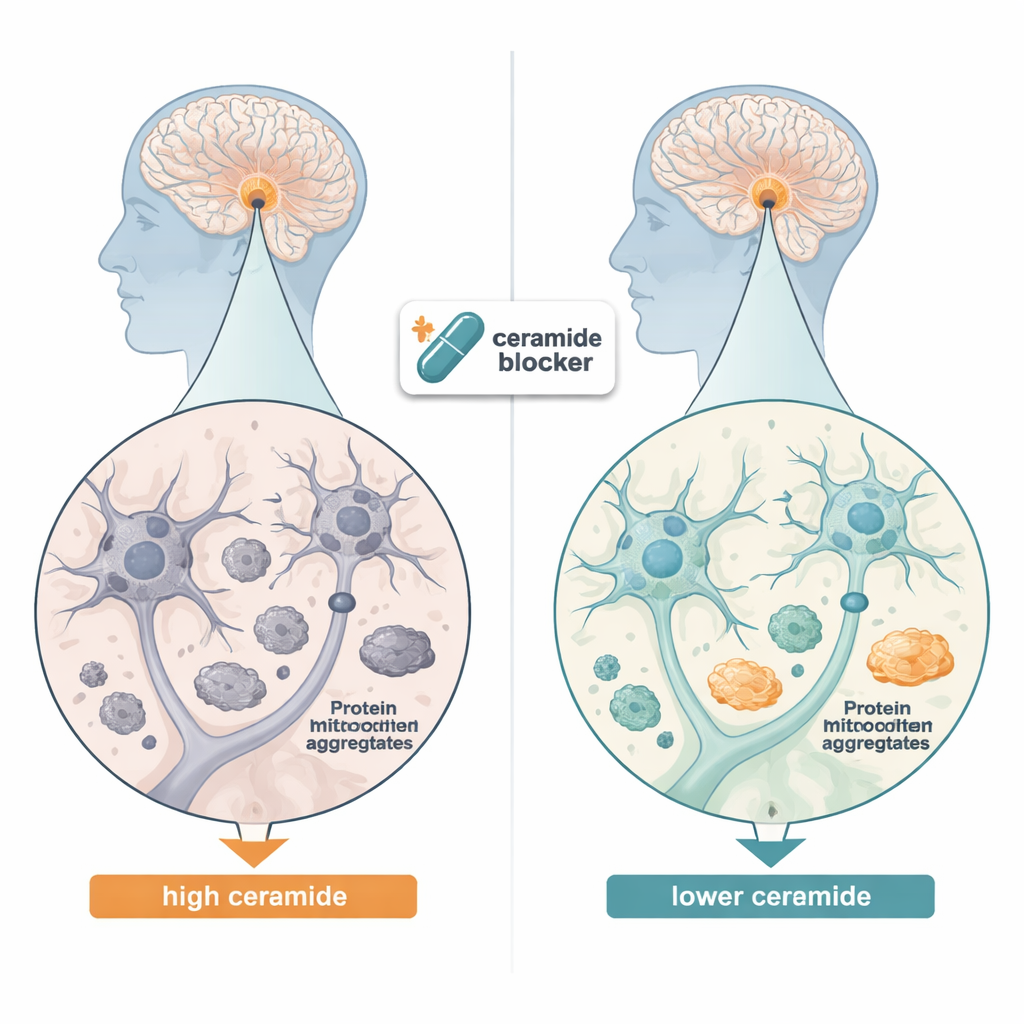
在细胞中清除蛋白质聚集
团队接着询问降低神经酰胺水平是否能减少在培养的类神经细胞中的蛋白质积累。他们使用经工程改造的人类神经母细胞瘤细胞,使其过度表达易形成聚集的突变型α‑突触核蛋白。当他们通过沉默关键酶基因或添加名为myriocin的药物关闭神经酰胺合成的第一步时,不溶性α‑突触核蛋白聚集体的数量显著下降。与此同时,线粒体自噬(细胞用于识别并回收受损线粒体的专门系统)的标志物上升,标记不需要蛋白质以便降解的机制也更为活跃。这些变化表明,过量神经酰胺通常抑制细胞的清理系统,而去除这种脂质负担让细胞更有效地清除损坏的线粒体和蛋白质聚集体。
在小鼠中保护脑功能
最关键的检验是这种策略在活体大脑中是否有效。研究人员用一种广泛采用的小鼠模型进行试验,该模型过度表达突变人α‑突触核蛋白,并逐步出现运动与记忆障碍。从中年起,一些小鼠连续数月接受myriocin注射,另一些则接受对照注射。myriocin明显降低了动物血液和中脑的神经酰胺水平。行为测试显示,接受治疗的小鼠行走距离更远,在依赖空间工作记忆的简单迷宫任务中表现更好。来自这些动物的脑切片显示,在关键区域存活的多巴胺能神经元更多,易磷酸化并易聚集的α‑突触核蛋白含量减少。中脑的大规模基因表达谱分析进一步表明,myriocin下调了炎症通路,同时恢复了与突触传递和健康线粒体维护相关的基因表达。
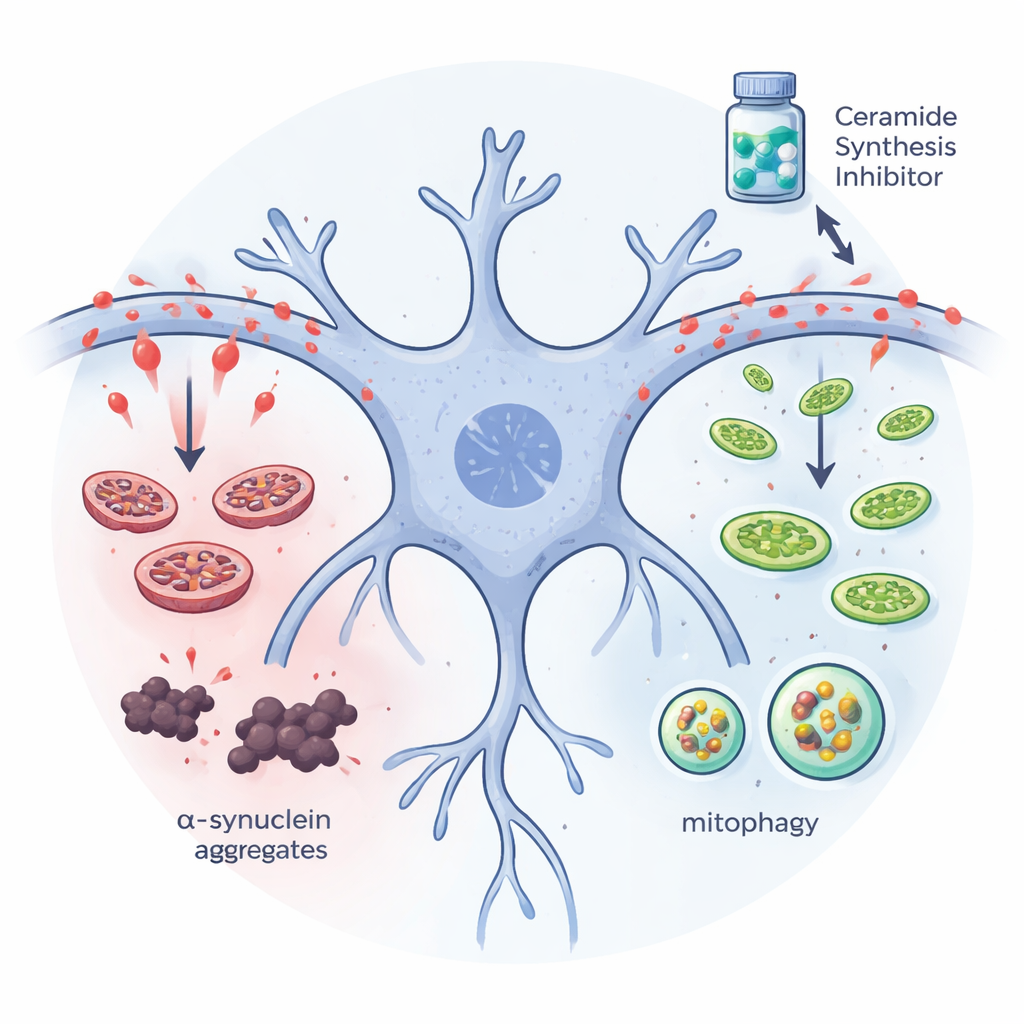
人体神经元与类脑组织的证据一致
为使结果更贴近患者,团队使用来源于帕金森病患者的诱导多能干细胞培养出神经元和三维中脑“类器官”。在带有线粒体自噬荧光传感器的患者来源神经元中,myriocin处理增强了标记受损线粒体被运送到细胞回收中心的信号,并改善了线粒体网络的结构。在中脑类器官中,myriocin维持了多巴胺能细胞并减少了有害的α‑突触核蛋白聚集。当研究者向这些迷你大脑补充额外神经酰胺时,出现相反效应:蛋白质聚集增加,尤其是在来自帕金森供体的类器官中,多巴胺神经元丧失加剧。这些实验支持了神经酰胺积累在与人类相关的组织中直接产生有害作用的观点。
这对未来治疗意味着什么
对非专业读者而言,核心信息很直白:在多种帕金森模型中,某类大脑脂质过量似乎通过促进蛋白质聚集、损坏线粒体和持续炎症来毒害细胞。通过阻断这些脂质主要合成通路——使用实验性药物myriocin——可以缓解这些问题,保护易受损的神经元并改善小鼠的行为,同时在体外挽救人类神经元。作者强调,长期安全性和人体剂量尚不明确,且帕金森的成因远不止神经酰胺一项。不过,这项工作开辟了新的攻击方向:未来的疗法或许不仅是增强逐渐消失的多巴胺信号,还可以通过规范脂质代谢与细胞清理机制,给予神经细胞更大的抵抗神经退行性损伤的机会。
引用: Lee, E., Park, My., Park, M. et al. Inhibition of de novo ceramide synthesis mitigates alpha-synuclein pathology in a Parkinson’s disease mouse model. npj Parkinsons Dis. 12, 49 (2026). https://doi.org/10.1038/s41531-026-01263-5
关键词: 帕金森病, 神经酰胺, α-突触核蛋白, 线粒体自噬, 神经变性