Clear Sky Science · zh
UQCRC1 缺陷通过 PINK1 依赖机制损害帕金森病的线粒体自噬
这项研究为何与普通人息息相关
帕金森病最广为人知的是运动问题——震颤、僵硬和动作迟缓——但这些症状的背后,是脑细胞在产生能量和清理损伤方面的内部挣扎。本研究探讨了一种鲜为人知的蛋白质 UQCRC1,如何帮助脑细胞维持其“发电厂”的健康,以及它的功能失常如何可能为帕金森病打开大门。理解这套隐秘的机械装置,可能指引出能够减缓甚至预防疾病(而不仅仅缓解症状)的治疗途径。
脑细胞内部的能量问题
我们的脑细胞依赖线粒体——常被比作细胞的发电厂——来产生所需能量。UQCRC1 是线粒体某个执行该功能的复合体中的关键组成部分。早期研究显示,UQCRC1 的罕见遗传突变可通过给这些“发动机”施加压力而引发类似帕金森的疾病。在本研究中,作者提出了一个更广泛的问题:UQCRC1 水平降低是否也参与了更常见的、非遗传(“特发性”)帕金森病?
在患者大脑数据中发现共同信号
为回答这一问题,研究者汇总了 19 组公开可得的脑组织数据,来自既往死于或未死于帕金森病的人群。他们聚焦于黑质——帕金森病中多巴胺产生神经元退化的深部脑区。在 150 例对照和 185 例帕金森或相关病例中,研究者一致发现帕金森大脑中 UQCRC1 基因活性水平降低——平均约减少 20%,且结果不太可能由偶然或发表偏倚导致。他们通过测定来自两个独立来源的大脑样本中的 UQCRC1 蛋白以及携带疾病相关 UQCRC1 突变的人类类神经细胞,证实了这一点;在每种情况下,帕金森状态下的 UQCRC1 水平明显较低。 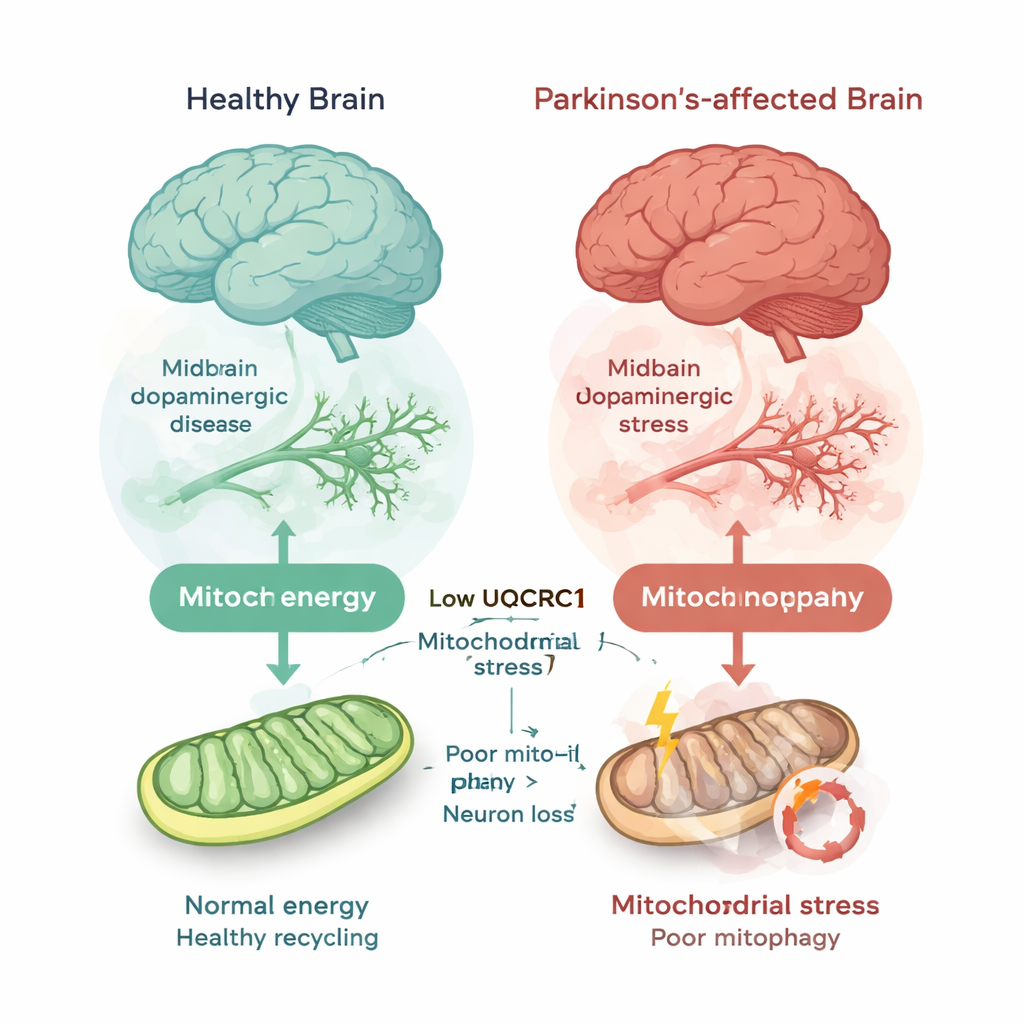
当清理队伍失灵时
线粒体不仅产生能量;当受损时也需要定期检查并清除。细胞使用一种名为线粒体自噬(mitophagy)的质量控制过程来标记磨损的线粒体并将其送到回收区。团队在人体细胞和果蝇中使用荧光报告器观察这一过程。在通常会触发线粒体自噬的压力下,具有 UQCRC1 突变或 UQCRC1 水平降低的细胞产生的“线粒体溶酶体”(标志着成功处置受损线粒体的结构)明显更少。在果蝇多巴胺神经元中,降低 UQCRC1 同样导致被回收的线粒体减少,类似于阻断核心自噬基因时的缺陷。这些发现表明,UQCRC1 的丧失并不只是削弱能量产生——它还破坏了对故障“发电厂”的清理工作。
一个缺失的开关和一个有前景的靶点
研究者随后关注 PINK1——一个在线粒体自噬中充当传感器和开关的蛋白。当线粒体受压时,PINK1 会在其表面积累,招募另一种叫 Parkin 的蛋白,并启动导致回收的标记过程。对患者大脑数据的荟萃分析显示,PINK1(而非 Parkin)在帕金森中脑中也下降了,大约降低了 22%。在人类细胞和具有 UQCRC1 问题的果蝇中,PINK1 水平下降,PINK1–Parkin 途径的早期步骤——Parkin 转移到线粒体并对其打标签——受到抑制。引人注目的是,在果蝇中提升 PINK1 可恢复其爬行能力并使线粒体自噬恢复正常,表明将该开关调高可以弥补 UQCRC1 的缺失。 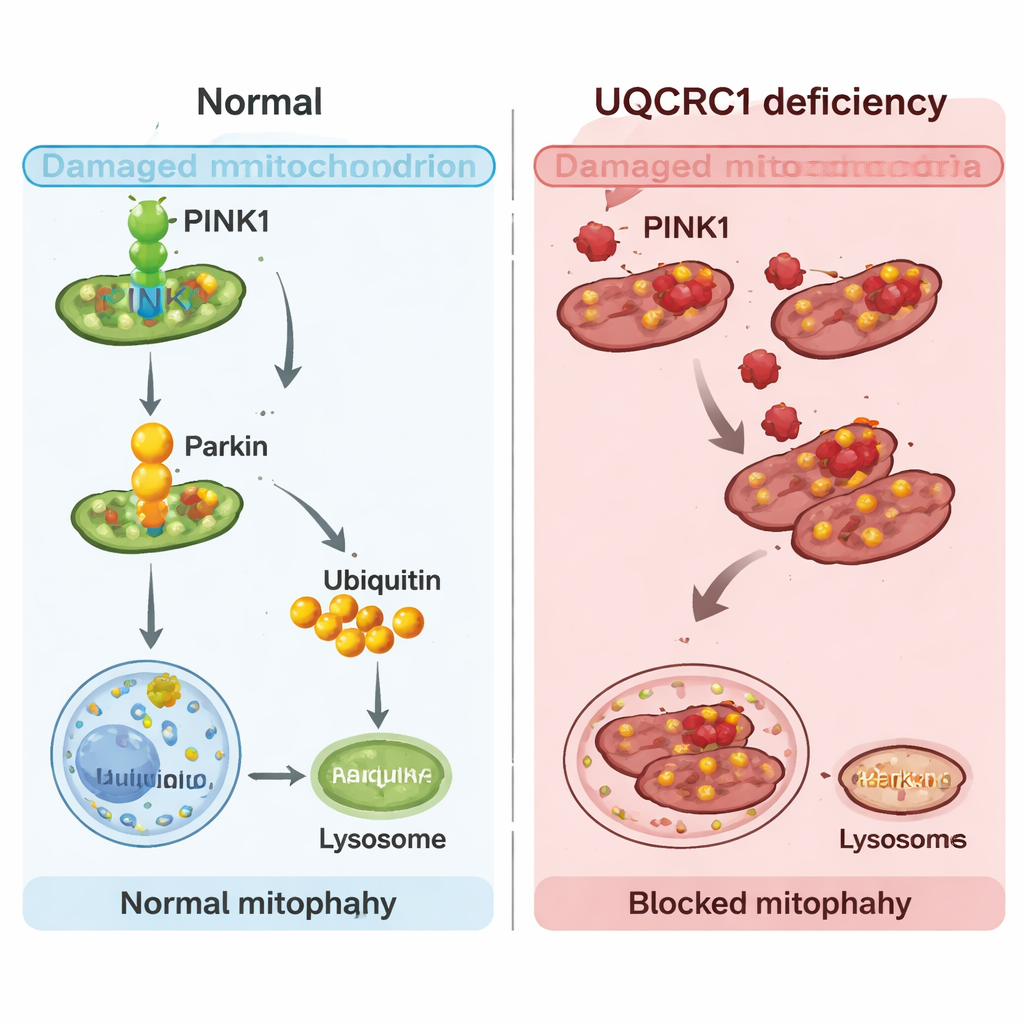
测试能激活清理通路的药物样化合物
由于直接补充 PINK1 在患者中并不可行,团队测试了已知能增强 PINK1 活性的几种小分子:kinetin 和 MTK458。在具有 UQCRC1 缺陷的果蝇中,饲喂这些化合物改善了运动并保护了易受损的多巴胺神经元。在 UQCRC1 降低的人类类神经细胞中,MTK458 延长了萎缩的神经突起并恢复了受损的线粒体自噬。这些益处依赖于 PINK1,支持了这样一种观点:谨慎激活该通路可以帮助细胞应对由低 UQCRC1 引起的线粒体应激。
这对未来帕金森治疗可能意味着什么
总体来看,这项研究将 UQCRC1 的下降与一连串反应联系起来:线粒体受压、PINK1 驱动的清理能力减弱,最终导致多巴胺神经元丧失。对普通读者而言,这意味着部分帕金森病例可能来自于那些不仅运转不良而且不断堆积、细胞无法清除的“发电厂”。尽管还需进一步工作以绘制每一步的细节并在人体中验证安全性,结果强调了 PINK1 激活剂作为潜在精准药物的前景,尤其适用于那些以线粒体缺陷(如 UQCRC1 缺失)为特征的帕金森患者。这类治疗的目标不是仅掩盖症状,而是恢复细胞维持和更新其能量工厂的自身能力。
引用: Li, JL., Huang, SY., Huang, PY. et al. UQCRC1 deficiency impairs mitophagy via PINK1-dependent mechanisms in Parkinson’s disease. npj Parkinsons Dis. 12, 48 (2026). https://doi.org/10.1038/s41531-026-01262-6
关键词: 帕金森病, 线粒体, 线粒体自噬, PINK1, UQCRC1