Clear Sky Science · zh
利用压电聚乳酸提高主动脉瓣环成形术的传感能力
倾听心脏的缝合处
当外科医生修补漏血的心脏瓣膜时,常在主动脉基部加固一个支撑环。这种修复需要承受数百万次心跳,但目前医生通常只能通过术后较晚的影像快照来检查其状况。本研究探索了一种新型短期、体内友好的电子环,它可以感知心脏的运动并将其转换为微弱电信号,提供一种实时“倾听”修复情况的方法,且无需留下永久性硬件。 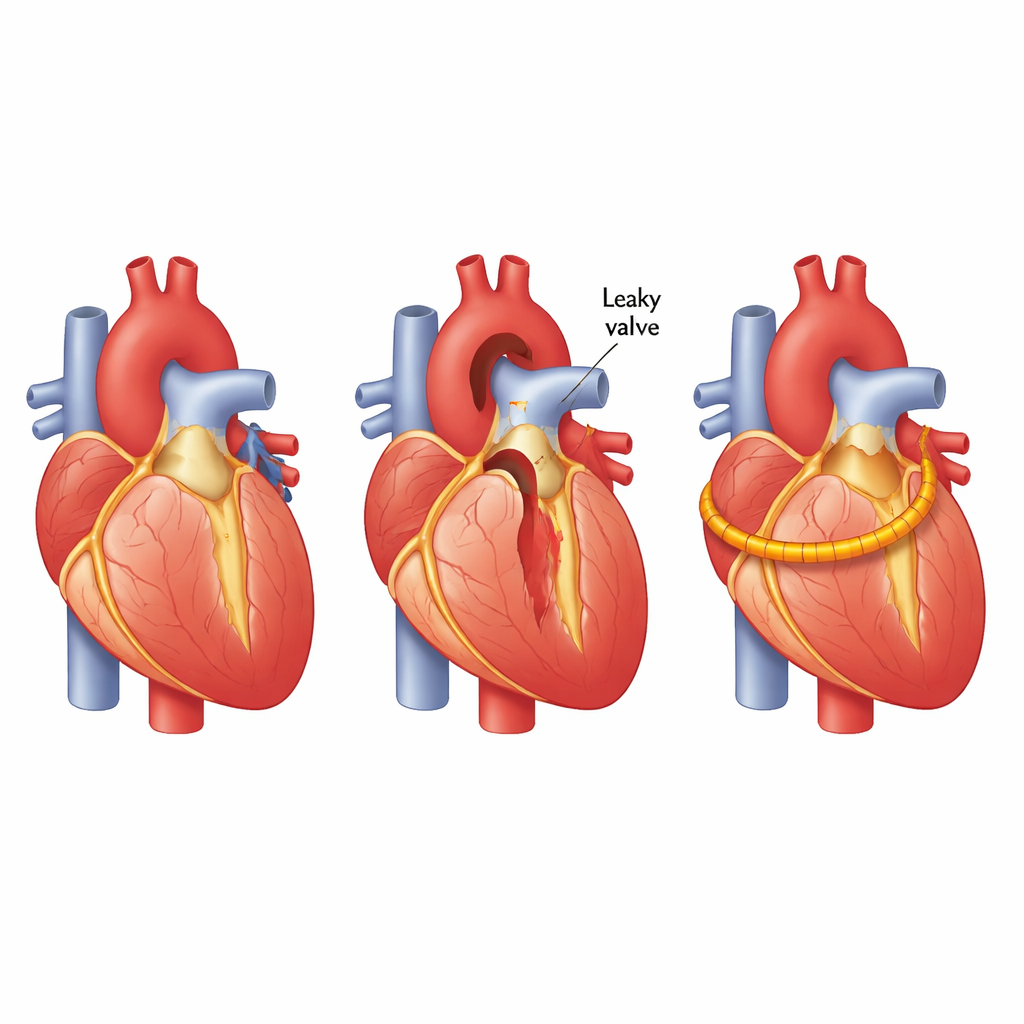
修补心脏瓣膜为何如此棘手
主动脉瓣控制心脏向全身的血流。在一些患者中,主动脉基部扩张或瓣膜发生返流,迫使心脏更费力地工作,最终导致严重疾病。外科医生可以通过收紧该区域并放置瓣环来避免用机械瓣替换,从而保留患者自身的瓣膜并避免终生服用抗凝药。然而,一旦胸腔关闭,医生几乎无法直接获知心跳时施加在瓣环上的实际力。现有的测量工具笨重、不可降解,不适合长期留置体内,因而无法提供修复随时间变化的行为信息。
一种会感知并最终消失的塑料
研究人员转向聚乳酸(PLLA),这是一种已在医用缝线和植入物中使用的塑料,因为人体可以在数月或数年内安全将其分解。PLLA还有另一项有用特性:当其内部分子以适当方式排列时,会呈现压电性,即在受压、拉伸或弯曲时产生微小电压。但未经处理的PLLA本身产生的信号不足以作为传感器使用。研究团队采用了一种简单且节能的工艺:将PLLA溶解、铸造成薄膜,将薄膜拉伸至原长的两倍,然后进行温和加热。该处理重组了材料的微观结构,提高了其将机械运动转换为电信号的能力,同时保留了强度和可生物降解性。
将智能环付诸测试
为评估经处理的PLLA的性能,团队对薄膜施加了不同形式的运动:反复拉伸、敲击、弯曲和受控振动。未经处理的薄膜几乎没有电响应,但经拉伸和热处理后,同一材料产生了大得多的电压和电流。薄膜被拉伸得越多,信号越强,证实材料的微观重排确实将其转变为敏感的运动探测器。这些实验还表明,薄膜对力和振动频率的变化反应可预测,这是在心脏这一持续运动环境中使用的重要要求。 
在实验室模拟跳动的心脏
基于这些结果,研究人员用响应最强的PLLA薄膜制作了一个环形传感器,并加上了薄银电极以收集其产生的微弱电压。然后他们将这个柔性环安装在一个3D打印的主动脉根模型周围,搭建了一个模拟人体左心室的实验装置。通过泵送流体以产生逼真的血压,他们能够将模型“主动脉”中的压力波与环的电输出进行比较。当模拟血压从正常升高到高值时,PLLA环产生了更大的电压摆幅:在低压时约为-0.5到+0.5伏,高压时约为-1.1到+1.3伏。信号稳定、随每次心跳重复出现,并且与压力脉冲的时序和幅度紧密对应。
这对未来心脏手术意味着什么
对非专业读者来说,关键信息是:团队已创造出一种薄而柔性的塑料环,能够感知心脏在修复处的拉推力量并将其转化为简单的电信号。由于材料具备生物相容性和可生物降解性,此类环原则上可以仅在需要的时间内留置,随后随着患者愈合安全消失。尽管这项工作是在逼真的实验模型中完成而非人体内进行,但它表明可溶解传感器能够可靠监测类似心脏的压力。未来,类似设备可能在外科医生调整瓣膜修复时提供指导,并在术后持续监测,提供无需体内永久电子设备的连续反馈。
引用: Merhi, Y., Montero, K.L., Johansen, P. et al. Harnessing piezoelectric poly L lactic acid for enhanced sensing in aortic annuloplasty. npj Flex Electron 10, 31 (2026). https://doi.org/10.1038/s41528-026-00533-9
关键词: 主动脉瓣修复, 可生物降解传感器, 压电塑料, 心脏手术监测, 柔性电子学