Clear Sky Science · zh
转录组分析揭示雄激素受体阳性三阴性乳腺癌用雄激素受体抑制剂放射增敏的机制
这项研究对面临乳腺癌患者的重要性
放射治疗是许多具有侵袭性乳腺癌患者的主要治疗手段,但不同肿瘤对放射的敏感性存在差异,其中一些肿瘤天生更难被放灭。该研究提出了一个具有临床现实意义的问题:一种已在前列腺癌中使用、阻断男性激素信号的药物类别,能否让某些三阴性乳腺癌对放射更加脆弱——以及为什么这种组合在有些情况有效而在另一些情况无效?
一种难治的乳腺癌类型
三阴性乳腺癌缺乏三种常见的分子靶点——雌激素受体、孕激素受体和 HER2——因此患者往往只能依靠手术、化疗和放疗。然而,其中一部分肿瘤表达雄激素受体,这是一种对类似睾酮的激素有反应并可驱动肿瘤生长的蛋白。早期工作表明阻断该受体可以抑制这些癌症并可能增强放疗效果,但其具体机制以及哪些药物和肿瘤能获益仍不明确。
在放疗条件下测试现代抗雄激素药物
研究人员使用了若干实验室模型的三阴性乳腺癌细胞系,这些细胞主要在表达雄激素受体的多少上有所不同。他们关注两种较新的抗雄激素药物:阿帕鲁他胺(apalutamide)和达罗他胺(darolutamide),并将短期用药与标准剂量X射线放疗联合使用。在高表达雄激素受体的细胞中,阿帕鲁他胺明显增加了放射损伤,使能形成新菌落的细胞大幅减少。相比之下,达罗他胺在相同细胞中对放射敏感性几乎没有影响,而且在雄激素受体表达极低的细胞中,两种药物都无明显帮助。这些发现表明,不是所有抗雄激素药物在乳腺癌中的作用相同,并且肿瘤须强烈依赖该受体时,联合治疗才可能奏效。
观察细胞内关键蛋白的移动
为了解激素信号或放疗后癌细胞内发生了什么,研究团队追踪了雄激素受体自身的位置。当细胞暴露于合成雄激素时,受体会进入细胞核——基因开关所在的控制中心。单独放疗并不会将受体驱出细胞核;事实上,放疗后受体仍留在核内,准备影响基因活性。然而,当细胞在放疗前接受抗雄激素药物恩杂鲁胺(enzalutamide)处理时,核内受体水平下降,更多受体滞留在细胞外液中。这支持了这样一种观点:阻断受体进入细胞核会干扰其在放疗后启动保护性基因程序的能力。
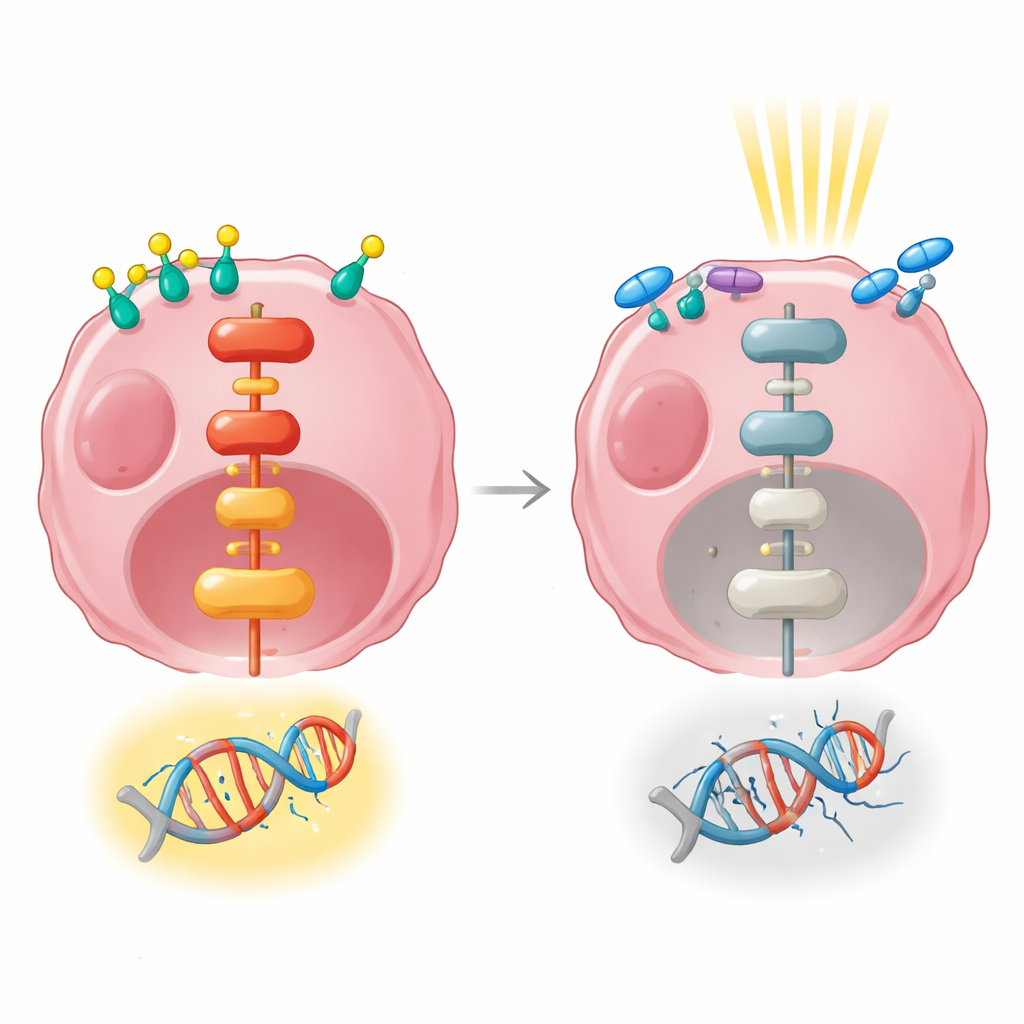
将激素信号与抗性联系起来的基因信号
随后,研究者使用RNA测序对激素刺激、放疗或两者联合后基因表达的全景进行了快照式观察。仅激素处理就改变了数百个基因的活性,并强烈影响控制细胞生长、黏附和与周围环境交流的通路。单独放疗在早期时间点影响的基因要少得多。当激素刺激与放疗合并时,许多相同的生长相关通路被激活,包括一个主要信号通路——MAPK/ERK,该通路将来自细胞表面的信号传递到细胞核。已知该通路有助于细胞存活并修复DNA损伤。
探查保护DNA的生存通路
由于在分析中反复出现MAPK/ERK信号,研究者测试了增强该通路是否会抵消雄激素受体阻断在放疗中的益处。他们对癌细胞进行了改造,使其过表达一种持续活化的ERK(该通路的关键成分),然后重复放疗加阿帕鲁他胺的处理。在这种条件下,阿帕鲁他胺不再使细胞对放射更敏感:放大的ERK信号似乎为细胞提供了屏障。结合蛋白水平的测量,这些结果指向MAPK/ERK信号作为雄激素受体活动与细胞修复放射诱导DNA断裂能力之间的关键联系。
这对未来乳腺癌治疗的意义
简而言之,这项工作表明,一些三阴性乳腺癌通过利用与雄激素相关的信号来开启内部生存回路,从而在放疗中幸存并修复受损DNA。像阿帕鲁他胺和恩杂鲁胺这样的药物可以在强烈依赖雄激素受体的肿瘤中中断这一回路,使放疗更有效;而受体水平低或存在替代生存路径的肿瘤可能无益。通过绘制涉及的基因通路——尤其是MAPK/ERK通路——本研究为更精确地将抗激素药、通路抑制剂和放疗组合起来打下了基础,可能改善这种难治性乳腺癌患者的结局。
引用: McBean, B., Hauk, B., Michmerhuizen, A.R. et al. Transcriptomic analysis to uncover the mechanism of radiosensitization of AR-positive triple-negative breast cancers with AR inhibition. npj Breast Cancer 12, 50 (2026). https://doi.org/10.1038/s41523-026-00916-1
关键词: 三阴性乳腺癌, 雄激素受体, 放射治疗, 放射增敏, MAPK ERK 信号通路