Clear Sky Science · zh
通过时空可控释放CpG寡脱氧核苷酸、吉西他滨和紫杉醇的可编程局部免疫化疗治疗三阴性乳腺癌
将顽固的乳腺癌变为可局部打击的目标
三阴性乳腺癌是最难治疗的乳腺癌类型之一,因为它缺乏许多现代药物所针对的常见分子标靶。患者往往不得不依赖大剂量全身化疗,这会带来严重副作用,并且长期控制效果常常不尽如人意。本研究探讨了一个不同的思路:与其将药物充斥全身,不如在肿瘤旁放置一个微小的可编程药物储库,在最需要的部位按精心设计的时序释放化疗药物和免疫激活剂。
小小储库,雄心不小
研究者构建了他们所称的可编程局部免疫化疗(PLICT)平台。可以把它想象成一个柔软、可注射的小珠,置于乳腺肿瘤旁并在数周内缓慢释放治疗药物。该小珠将一种亲水凝胶(可迅速释放一种免疫刺激剂和一种化疗药吉西他滨)与微米级塑料小球(缓慢释放第二种药物紫杉醇)结合在一起。免疫刺激剂是称为CpG的短链DNA,旨在激活局部免疫细胞;配合的两种化疗药物直接攻击肿瘤细胞并重塑肿瘤微环境,使免疫细胞得以进入并发挥作用。
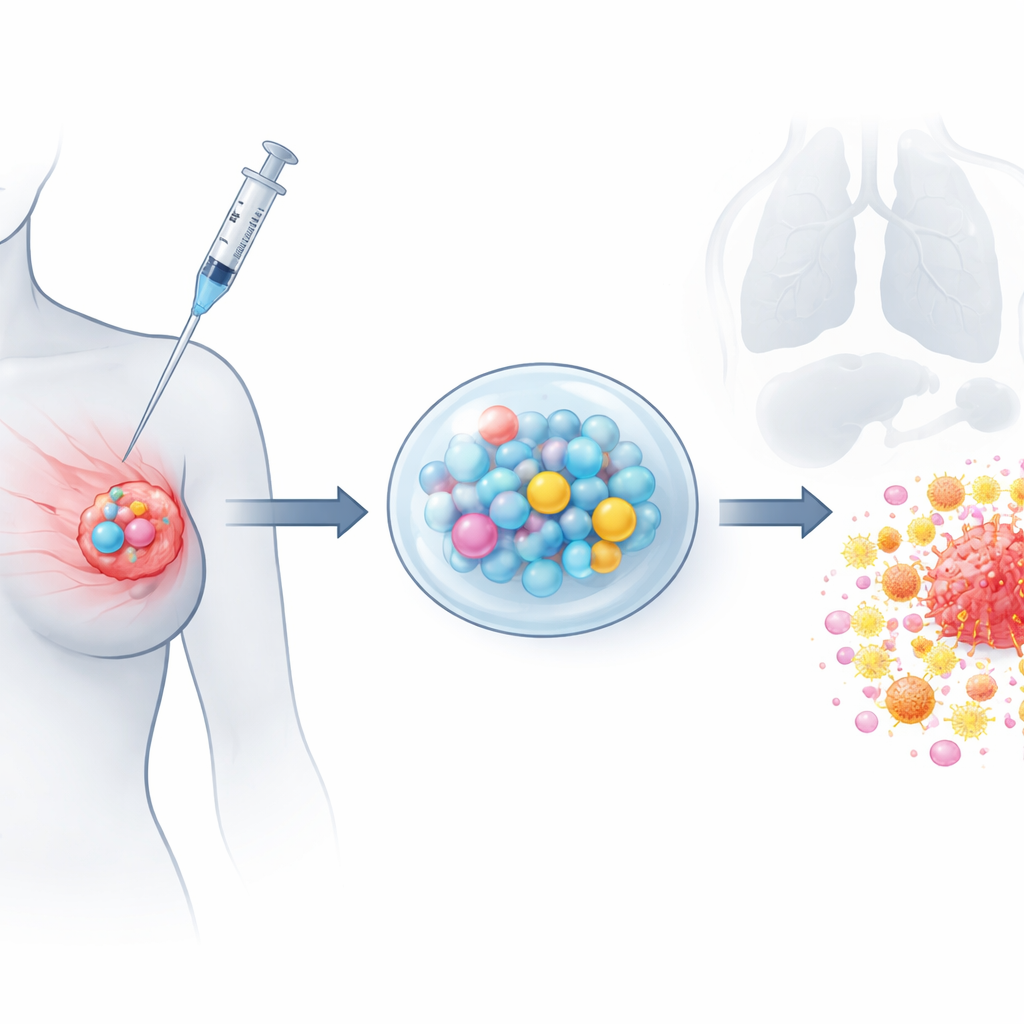
设计一个定时释放的抗癌方案
为构建该系统,团队采用高压“电喷雾”方法由可生物降解聚合物制备出均一的负载紫杉醇的微球。成像显示这些颗粒光滑球形,直径约为人发丝的十分之一;体外试验证实紫杉醇在至少一个月内稳定持续释放且没有早期突释。另将吉西他滨和CpG嵌入一种温度敏感凝胶中,该凝胶在低温时为液体,在体温下变为半固体。化学指纹分析验证了两种药物在载体内保持完整。组合后,凝胶提供快速的早期吉西他滨和CpG剂量,而微球则持续缓慢释放紫杉醇,从单次局部给药模拟出长期低剂量化疗的益处。
在小鼠中检验局部策略
随后团队在三阴性乳腺癌小鼠模型中测试了PLICT。小鼠先长出小肿瘤,然后分别接受传统单独注射紫杉醇、紫杉醇加吉西他滨,或在肿瘤旁植入单次局部PLICT。四周观察期内,对照组肿瘤快速生长,接受常规化疗的肿瘤生长较慢,但PLICT处理的肿瘤在体积和重量上显著更小。整体及器官影像显示,PLICT比传统药物注射更有效地减少了癌症向远处转移,尤以肺转移减少为著。药物浓度测量揭示了原因:PLICT处理的肿瘤内紫杉醇高度富集,而远端脂肪组织中含量低,血液中的水平相近,提示实现了强烈的局部滞留并减少了非靶向暴露。
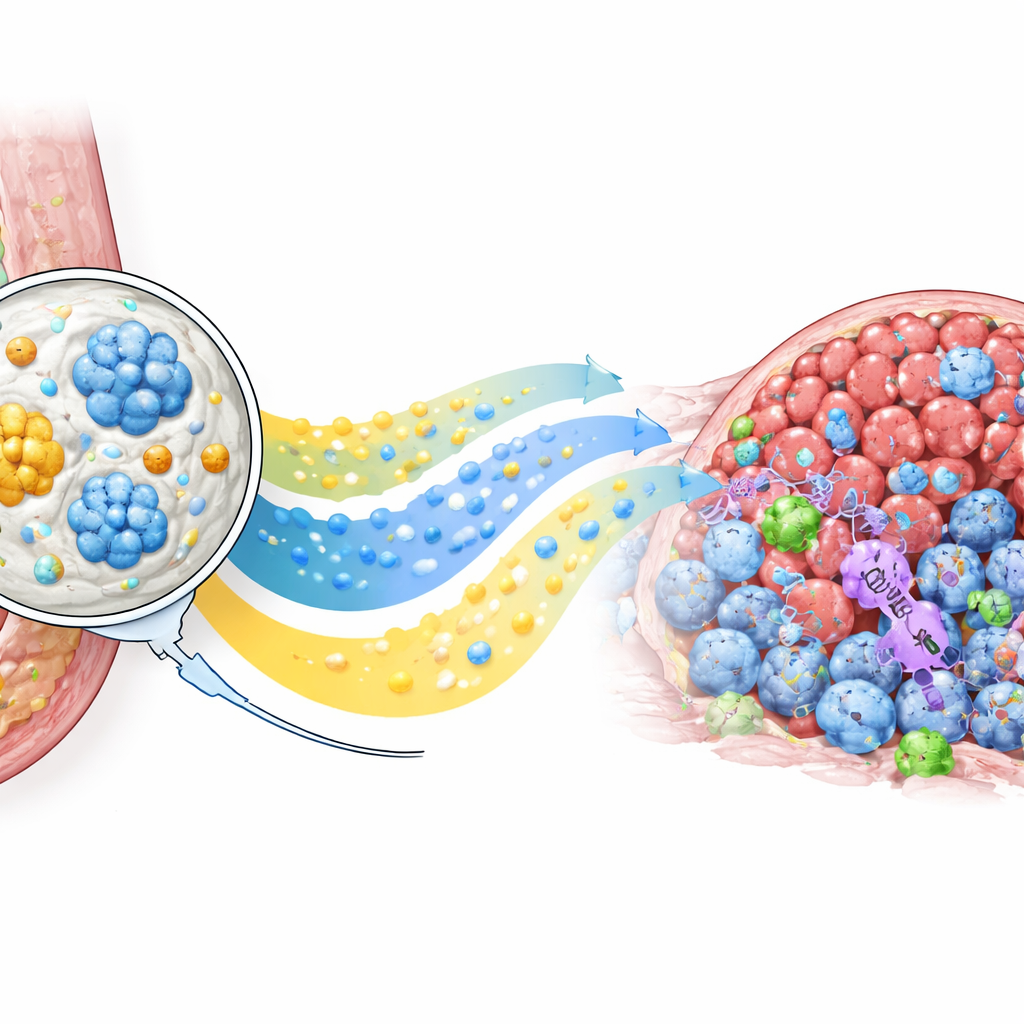
动员机体自身的防御力量
除了缩小肿瘤外,PLICT还改变了肿瘤内的免疫格局。细胞分析显示,与其他所有组相比,PLICT处理的肿瘤中杀伤癌细胞的CD8 T细胞显著增加,同时某些通常抑制免疫攻击的调节性T细胞减少。针对最近被激活T细胞标志物CD69的组织染色证实,许多浸润的细胞处于被激活并准备行动的状态。与此同时,常规化疗在肝脏组织中造成明显损伤,而PLICT处理小鼠的器官在显微镜下几乎正常。综合来看,这些发现表明局部储库不仅提高了肿瘤内的药物暴露,还激发了更有利、受抑制较少的免疫反应,同时未给重要器官带来额外负担。
这对未来癌症治疗可能意味着什么
对非专业读者来说,结论很直白:通过将化疗和免疫刺激转化为一种缓慢、精确分阶段的滴注并直接置于肿瘤旁,这种方法在动物中比传统药物注射实现了更强的肿瘤控制和更少的全身副作用。这项工作仍处于临床前阶段,关于该系统在人类或不同治疗情境中的表现仍有许多问题需要回答。但可注射、可编程的“药物储库”按顺序静默释放多种药剂的概念,可能为治疗像三阴性乳腺癌这样侵袭性肿瘤开辟新途径——把战斗集中在最关键之处,同时尽量保护身体其他部位。
引用: Hsieh, CH., Hsu, MY., Lin, CF. et al. Programmable local immunochemotherapy for triple-negative breast cancer via spatiotemporally controlled release of CpG oligodeoxynucleotides, gemcitabine, and paclitaxel. npj Breast Cancer 12, 45 (2026). https://doi.org/10.1038/s41523-026-00910-7
关键词: 三阴性乳腺癌, 局部药物递送, 免疫疗法, 可控释放, 水凝胶微球