Clear Sky Science · zh
CXCL10/CXCR3 轴对应维持三阴性乳腺癌免疫休眠至关重要
为何有些癌症“睡着”而不是扩散
乳腺癌有时表现得像一个潜伏的特工。初次治疗后,少数癌细胞可能在体内潜伏数年,增长不足以在影像学上被发现——但仍有可能在之后苏醒并引发危及生命的转移。本文探讨为何这种被称为休眠的“睡眠”状态会出现在一种特别侵袭性的病型——三阴性乳腺癌中,并发现了一种帮助免疫系统控制这些细胞的化学信号。
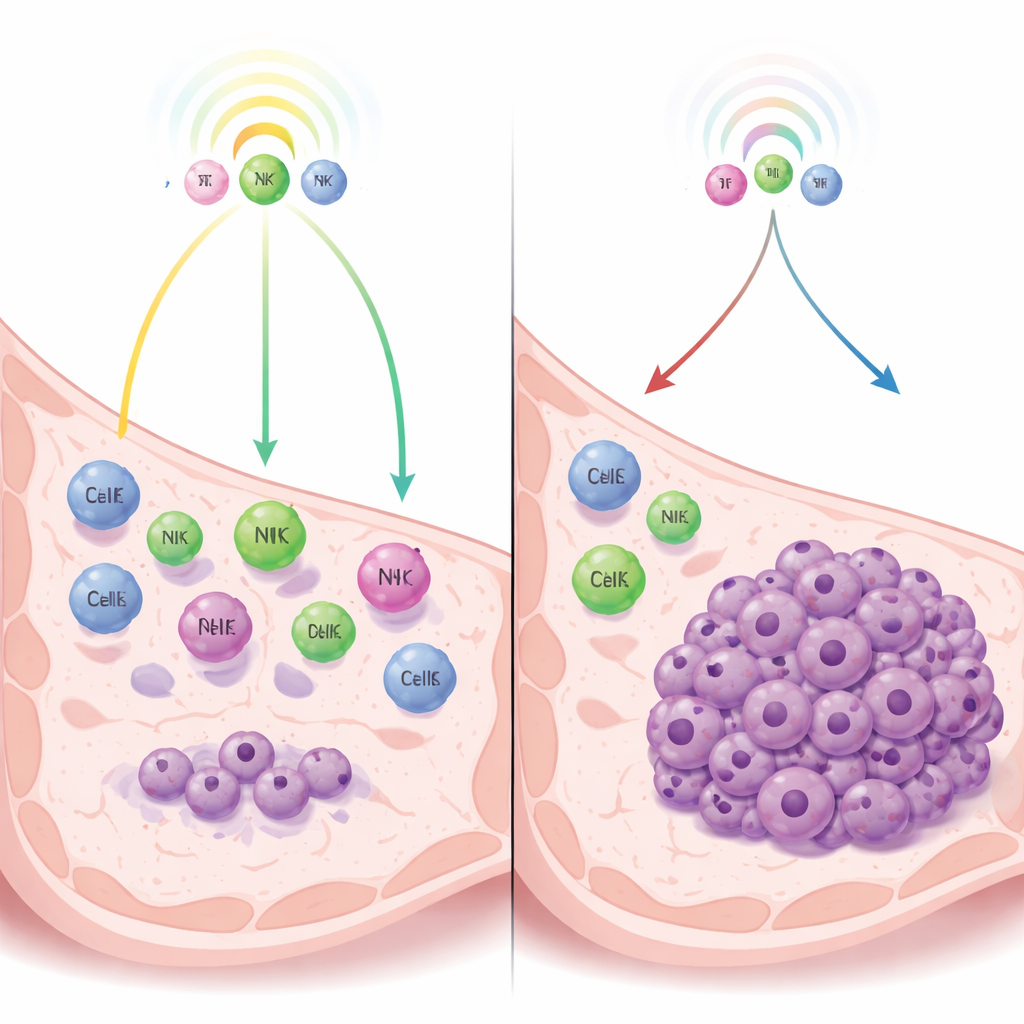
癌症与免疫系统之间的拉锯战
作者关注的一类休眠并非由血供不足或细胞内抑制机制主导,而是由免疫监视控制——免疫细胞持续守望,可以压制肿瘤而不将其彻底清除。通过三阴性乳腺癌的小鼠模型,他们比较了自然保持休眠的肿瘤细胞与形成快速生长肿瘤的密切相关细胞。通过检测哪些基因被激活,他们发现休眠细胞强烈激活干扰素通路——这类免疫警报系统会刺激释放吸引免疫细胞进入肿瘤区域的化学信使。
保持肿瘤“安静”的关键化学信使
在休眠细胞上调的众多分子中,有一个尤为突出:CXCL10,一种像信标一样吸引携带其配对受体 CXCR3 的免疫细胞的小蛋白。与侵袭性细胞相比,休眠的癌细胞产生更多的 CXCL10。当研究者有意关闭休眠细胞中的 CXCL10 并将其植入具有完整免疫系统的小鼠时,曾经沉寂的细胞迅速形成肿瘤。用抗体阻断 CXCR3 受体也有类似效果。在这两种情况下,癌细胞都能打破免疫僵持并开始生长,表明 CXCL10/CXCR3 轴不仅与休眠相关——它是维持休眠所必需的。
局部环境改变如何改变平衡
降低 CXCL10 的影响不仅限于单一通路;它重塑了整个局部免疫景观。在失去 CXCL10 的肿瘤中,有益的 CD4 和 CD8 T 细胞减少,而某些可抑制免疫反应的髓系细胞变得更多。自然杀伤细胞和树突状细胞的数量也发生变化。这一模式在原发肿瘤和癌细胞可迁移并潜伏的肺部均可观察到。即使肺部转移灶小到显微镜下难以看到,分子标志显示在缺乏 CXCL10 时更多癌细胞能够在肺部落地,且侵入这些组织的 T 细胞更少。然而在完全缺乏功能性免疫系统的小鼠中,去除 CXCL10 并无影响——休眠细胞照样生长——这进一步强调该信号通过免疫控制起作用,而非直接抑制癌细胞生长。
为何增强信号有益但非万能开关
研究团队也验证了相反的设想:增加 CXCL10 能否将侵袭性肿瘤转为休眠?当他们将快速生长的癌细胞改造为产生额外 CXCL10 时,肿瘤生长变慢、出现时间延后,血液中某些免疫细胞类型也增多。然而,完全的休眠并未形成;最终所有小鼠仍然长出肿瘤。这表明,虽然在其他免疫机制到位时 CXCL10 对维持休眠是必需的,但它本身无法独立建立这一复杂状态。还需要其他通路协同,才能在免疫攻击与癌细胞存活之间建立长期平衡。
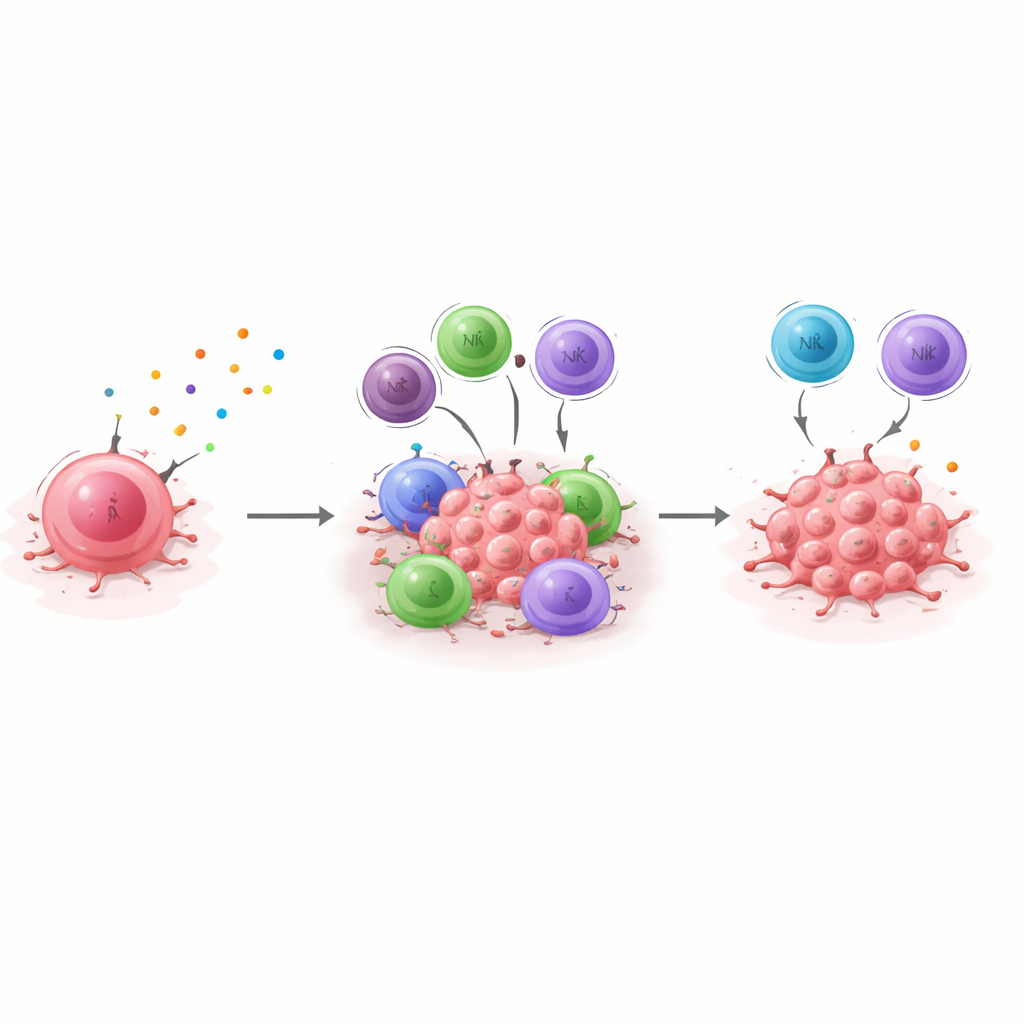
从小鼠实验到患者前景
为将发现与人类疾病联系起来,研究者构建了一个“休眠特征”——一组在休眠细胞中持续升高且在 CXCL10 被沉默时下降的基因。随后他们在大规模乳腺癌患者数据库中考察该特征与生存的关系。在三阴性乳腺癌中,表达该休眠特征较高的患者整体生存更长,且往往更长时间无复发,这与免疫控制的休眠状态延缓复发的假设一致。在激素受体阳性肿瘤中并未观察到相同的效应,凸显了乳腺癌亚型之间的生物学差异。总体来看,这些结果表明 CXCL10/CXCR3 轴是三阴性乳腺癌免疫介导休眠的核心支柱,测量该休眠特征或可帮助识别更可能从强化免疫控制疗法受益的患者——反之,也能提示哪些患者可能需要更密切的长期监测,因为其癌症更难以被控制。
引用: Yilmaz, A., Haerri, L., Granda, M.E. et al. The CXCL10/CXCR3 axis is essential for sustaining immunological dormancy in triple-negative breast cancer. npj Breast Cancer 12, 36 (2026). https://doi.org/10.1038/s41523-026-00903-6
关键词: 三阴性乳腺癌, 肿瘤休眠, 免疫监视, 趋化因子信号, CXCL10 CXCR3 轴