Clear Sky Science · zh
空间基因表达分析揭示乳腺癌极早期淋巴结转移的驱动因素
为什么微小迁移的癌细胞很重要
当乳腺癌扩散出乳房时,通常首先停留在附近的淋巴结——这些小滤器有助于抵御感染。临床医生知道,在这些淋巴结中发现癌细胞通常预示疾病复发的风险更高。但在真实患者体内,当只有少数细胞刚到达淋巴结的最初瞬间到底发生了什么,一直几乎无法观测到。本研究采用一种新的显微“地图”来描绘基因活动,前所未有地观察这些最早的步骤,揭示了哪些细胞成功、哪些失败,以及这些差异对患者结局为何重要。
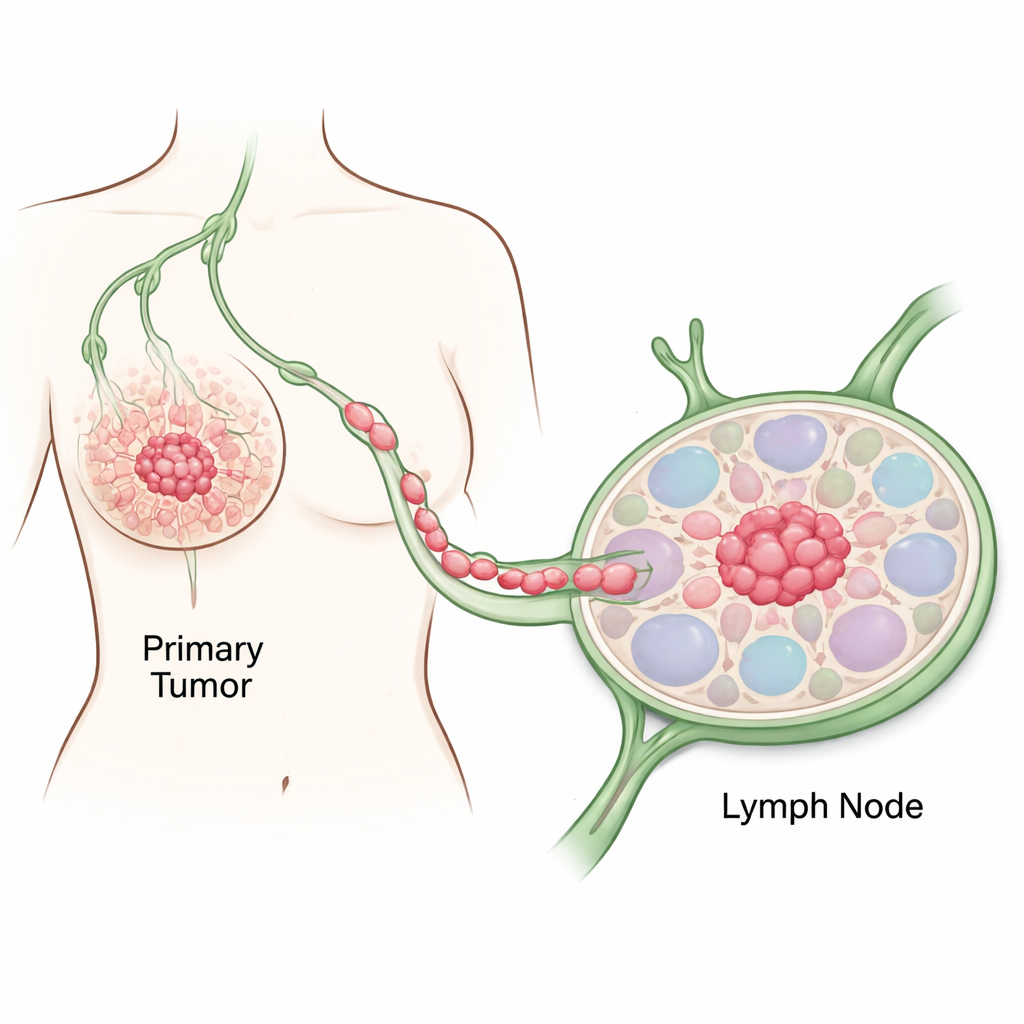
追踪癌症的第一步
研究人员聚焦于一名80岁女性患者的组织样本,该患者患有侵袭性HER2阳性乳腺癌。他们取样了看似正常的乳腺区域和近旁的肿瘤区域,随后使用多种DNA和RNA检测追溯普通细胞如何演变为癌细胞。与健康组织相比,肿瘤区域显示出癌症的经典特征:细胞黏附受损、细胞分裂过度活跃、大规模DNA甲基化变化以及控制生长和基因组稳定性的关键基因突变。这些分子变化与病理学家在显微镜下看到的形态学改变相吻合,证实了从正常乳腺细胞向完全恶性细胞逐步演进的过程。
变形的细胞在迁移
为了解肿瘤细胞如何开始迁移,研究团队使用了一种高分辨率技术,在保留细胞在组织中精确位置的同时读取其基因活动。这使他们能够重构癌细胞离开正常乳腺结构并走向转移时的身份变化。研究发现,癌症似乎起源于一种特定类型的成熟乳腺细胞,该细胞随后逐渐获得一种称为上皮—间充质转化(EMT)的特征——这是一种有助于细胞松动、移动和侵袭邻近组织的“变形”过程。细胞并非简单地开关切换,而是处于混合状态的谱系中,既有“上皮”特征(有序、紧密结合),又有“间充质”特征(可移动、具侵袭性)。其中一些混合状态的细胞在肿瘤中散布开来,而另一些则聚集成更为进阶的癌细胞群,这些群体更易于向淋巴结扩散。
淋巴结中的第一个远端滩头堡
在一个按常规临床检测被判断为无转移的淋巴结中,科学家们发现了令人惊讶的情况:只有大约30个零散的肿瘤细胞,分布在约200微米宽的区域——大约是人类头发宽度的两倍。这些孤立的肿瘤细胞来自数种不同的混合状态,每种都有其独特的基因表达模式。通过对相关癌细胞进行分群,团队定义了六种具有不同作用的亚型。其中一种强烈的“间充质型”亚型在抗凋亡和逃避免疫攻击方面表现尤为突出。另一种恢复更多上皮特征的亚型则在能量利用上发生显著转变,更倾向于脂肪酸代谢。只有这种代谢重编程、更偏上皮样的群体成功在淋巴结中形成小型菌落,提示燃料选择——而不仅仅是侵袭性——有助于决定早期到达者能否扎根。
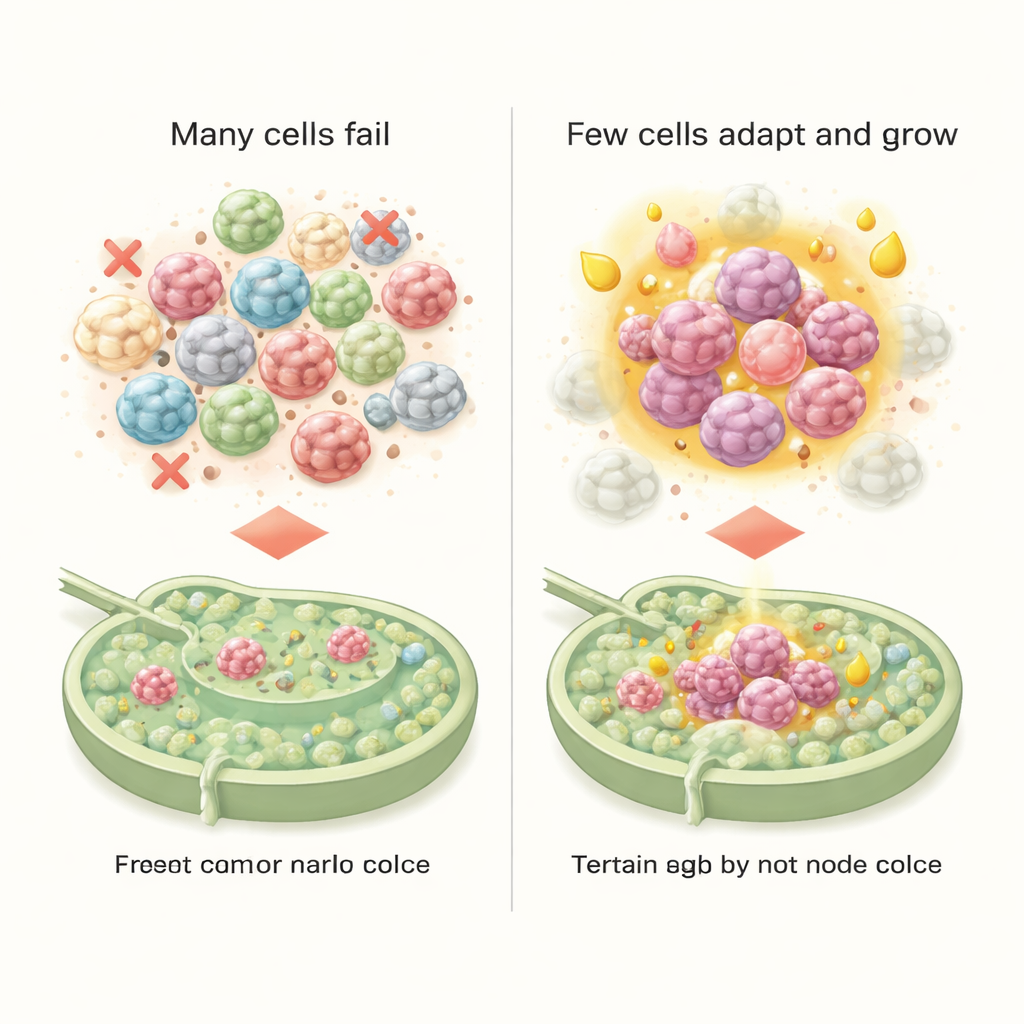
静悄悄助长癌症的淋巴结
研究还考察了淋巴结微环境如何响应这些入侵者。即便在可见转移形成之前,免疫细胞、血管细胞和结缔组织已经在发出信号,削弱免疫反应并支持肿瘤存活。免疫细胞之间的某些受体—配体配对暗示了早期免疫耐受,而其他配对则鼓励新生血管生长和组织支架的重塑。综合来看,这些变化构建了一个出乎意料地有利于代谢适应型癌细胞的生态位,帮助它们存活、生长并可能播种未来的扩散。
对患者意味着什么
通过将他们的发现与大型现有患者数据集进行比较,研究者得出一个反直觉的发现。那些最擅长形成早期淋巴结菌落的细胞,甚至具有最强间充质特征的细胞,并不对应最差的临床结局。相反,患者的预后最差出现在肿瘤含有某些以高细胞周期活动和以MYC等基因为驱动的糖酵解(耗糖)程序为特征的侵袭性混合细胞类型时。换言之,不同的变形细胞状态似乎各有专长:有些擅长悄无声息地在新部位定殖,而另一些则推动快速生长和复发。理解并针对这些不同的细胞状态及其代谢偏好,可能带来更精准的治疗——既能更可靠地检测最早期的扩散,也能切断最有可能导致致命复发的肿瘤细胞类型。
引用: Nagasawa, S., Kajiya, K., Ishikawa, E. et al. Spatial gene expression analysis reveals drivers of extremely early lymph node metastasis in breast cancer. npj Breast Cancer 12, 28 (2026). https://doi.org/10.1038/s41523-026-00897-1
关键词: 乳腺癌转移, 淋巴结, 上皮-间充质转化, 空间转录组学, 癌症代谢