Clear Sky Science · zh
间充质干细胞共同递送趋化因子CXCL9与共刺激配体TNFSF9,重编程三阴性乳腺癌的免疫微环境
为何这种新的乳腺癌策略重要
三阴性乳腺癌是最危险的乳腺癌类型之一,因为它生长迅速、早期易转移,并且缺乏许多药物所针对的常见激素受体。免疫疗法带来了希望,但在许多患者体内,防御性免疫细胞无法以足够数量进入肿瘤发挥作用。本研究探索了一种富有创造性的策略:将活细胞作为“定向运输车”,把增强免疫的信号直接送入难治性肿瘤,可能使更多患者有资格接受更强效的免疫治疗。
一种难以对付且免疫支援不足的癌症
三阴性乳腺癌的标准治疗——手术、化疗与放疗——常常无法阻止复发,晚期疾病的平均生存期仍不足两年。一个关键原因是许多这类肿瘤是“冷的”,即肿瘤内缺乏抗癌免疫细胞。大型患者数据库显示,肿瘤天然分泌较多两种免疫相关分子CXCL9和TNFSF9的患者,生存期更长,肿瘤内的T细胞与自然杀伤(NK)细胞也更多。CXCL9是一种将免疫细胞召集到组织的化学信号,而TNFSF9则像一个额外的“启动”开关,帮助这些细胞更强烈地攻击。该模式表明,直接在肿瘤内提高这两种信号可能会将平衡倾向于免疫系统。
将干细胞变成智能运输车
研究者聚焦于取自献血人类脐带的间充质干细胞。这类细胞有一个有用特性:当注入带有乳腺肿瘤的小鼠血液中时,它们会自然趋向肿瘤部位并在此滞留数天,同时在很大程度上避开正常器官。研究团队对这些干细胞进行了基因工程改造,使其分泌CXCL9并在细胞表面展示TNFSF9,创造出一种双重功能的细胞疗法,命名为MSC‑T9C9。体外试验表明,改造后的细胞大量分泌CXCL9并强烈激活小鼠的T细胞与NK细胞,同时不改变自身的生长行为也不会引起肿瘤形成,这使它们成为有前景的靶向免疫助推候选者。
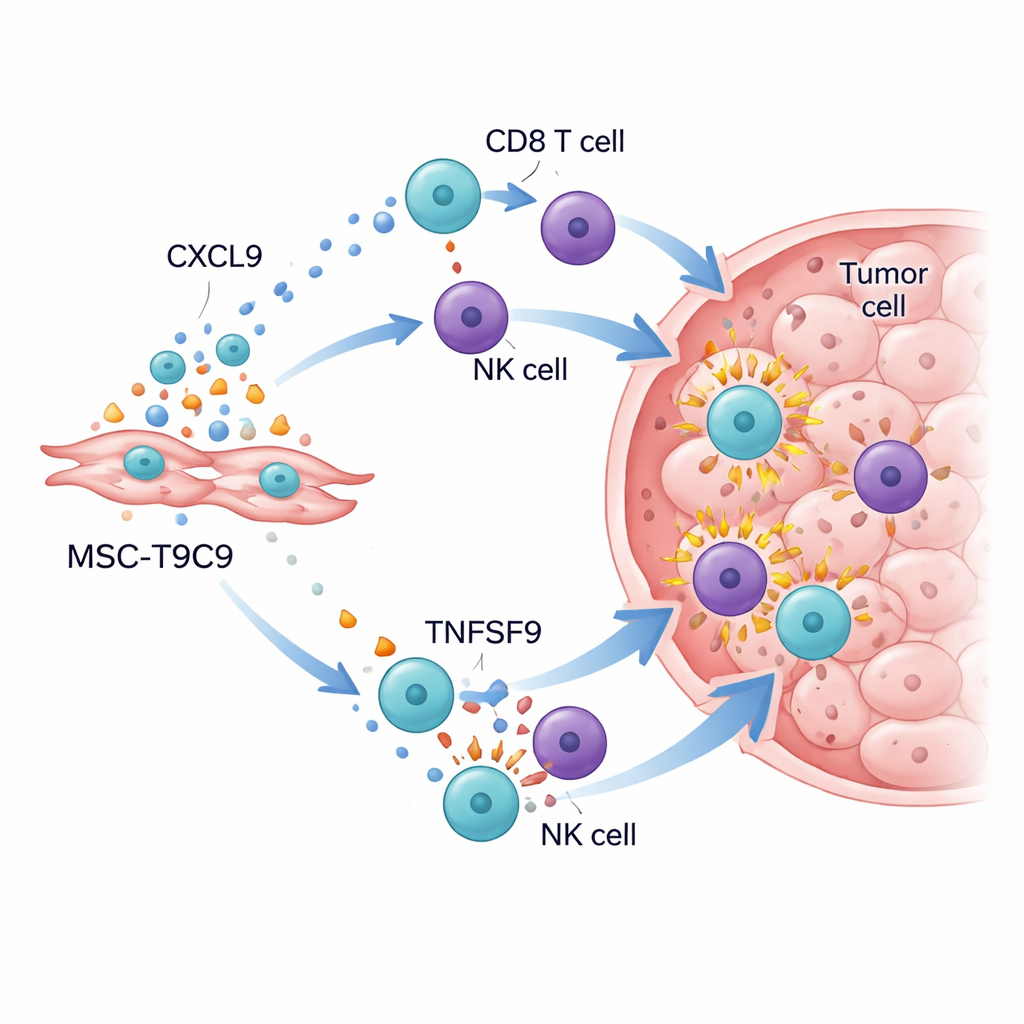
唤醒肿瘤内的免疫战场
将工程化细胞给予携带三阴性乳腺肿瘤的小鼠后,结果令人瞩目。在具有完整免疫系统的小鼠中,反复注射MSC‑T9C9显著减缓肿瘤生长并增加癌细胞死亡,而对照干细胞几乎没有效果。对肿瘤的详细分析显示,CD8“杀伤”T细胞和NK细胞数量显著上升,同时强效攻击分子如颗粒酶B、干扰素‑γ、肿瘤坏死因子‑α和白细胞介素‑2水平均提高。与此同时,肿瘤环境从抑制状态发生转变:有益的炎性巨噬细胞增加,尽管调节性T细胞仍然存在,但已被新一波的战斗细胞所压倒。在缺乏免疫的老鼠模型中(T细胞和NK细胞缺失),MSC‑T9C9未能减缓肿瘤生长,证实其疗效依赖于动员机体自身防御。
为检查点疗法做准备
现代免疫疗法药物如抗‑PD‑1抗体可以解除T细胞的分子“制动”,但当肿瘤内已有足够T细胞时效果最佳。研究发现MSC‑T9C9不仅将更多CD8 T细胞吸引到肿瘤中,还将它们推向一种高度活跃但对制动敏感的状态,以PD‑1受体为标志。在小鼠模型中,将MSC‑T9C9与抗‑PD‑1药物联合使用,比单独任何一种治疗都产生了最强的肿瘤缩小和最长的生存期。对人类癌症数据集的分析支持这一观点:TNFSF9与CXCL9联合水平较高的患者更可能从检查点阻断疗法中获益,提示相同的生物学机制可能适用于人体。
安全性与未来前景
任何增强免疫的治疗都会引起关于危险副作用的担忧,如全身性炎症或器官损伤。令人鼓舞的是,接受MSC‑T9C9的小鼠体重和行为保持正常,主要器官未见明显损伤,血液及肝肾功能检测也正常。重要的是,免疫活性的激增主要局限在肿瘤本身,血液中的炎性信号没有升高。尽管在进入人体试验之前仍需更多工作——包括在更真实的模型中验证和谨慎的剂量探索——本研究表明,利用工程化干细胞定向至肿瘤以招募并激活免疫细胞,可能为将“冷”三阴性乳腺癌转变为对免疫疗法反应更好的“热”肿瘤,提供一种更有针对性且更安全的途径。
引用: Ye, P., Wen, Y., Liu, R. et al. Co-delivery of chemokine CXCL9 and costimulatory ligand TNFSF9 by mesenchymal stem cells reprograms the immune microenvironment for triple-negative breast cancer. npj Breast Cancer 12, 30 (2026). https://doi.org/10.1038/s41523-026-00893-5
关键词: 三阴性乳腺癌, 免疫疗法, 间充质干细胞, 肿瘤微环境, 检查点阻断