Clear Sky Science · zh
使用合成噬菌体载体CRISPR-Cas递送系统针对性消除金黄色葡萄球菌乳腺炎感染
抗击代价高昂的乳品感染
奶牛及其他农场动物的乳汁可能会受到一种称为乳腺炎的疼痛性乳房感染的影响,这类感染常由细菌金黄色葡萄球菌引起。治疗这些感染通常需要长期使用抗生素,既昂贵又给动物带来压力,并助长抗生素耐药性问题。本研究探讨了一种截然不同的方法:将一种天然的类病毒细菌寄生体改造为精确武器,能够选择性切割细菌DNA并清除感染,同时不传播耐药基因。
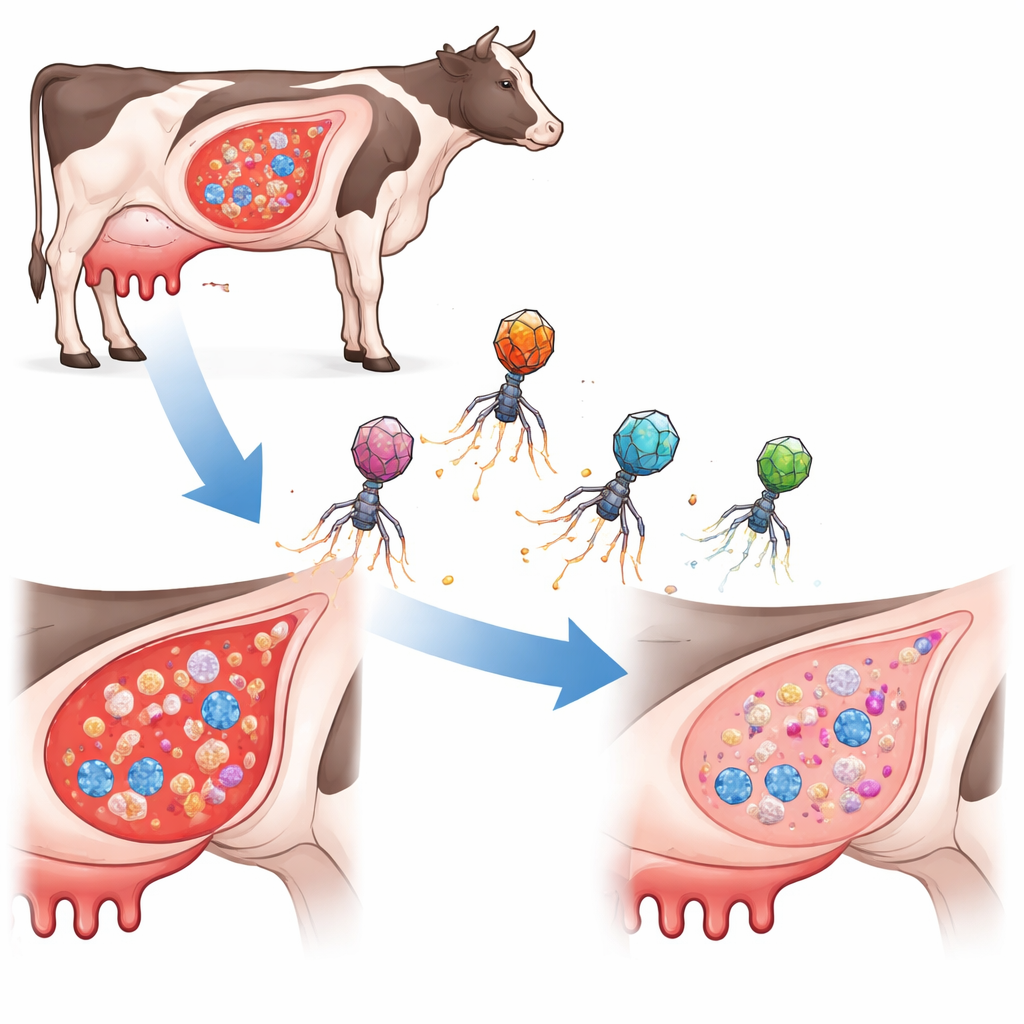
一种新型的靶向细菌猎手
研究人员没有使用传统抗生素或普通噬菌体(感染细菌的病毒),而是设计了携带DNA的微小元件,称为噬菌体诱导染色体岛(phage‑inducible chromosomal islands)。在自然界中,这些岛会寄生在噬菌体外壳内,借此在细菌之间传播。在本研究中,团队将其重构为“ePICI”,携带基因编辑工具CRISPR‑Cas9以及针对金黄色葡萄球菌三种重要调控小RNA的短引导序列。当ePICI进入目标细胞时,Cas9被表达并在所选位点切割细菌染色体,从内部杀死细胞。关键在于,这些工程化颗粒本身不具备自我复制能力,从而限制了它们的扩散并降低了意外移动有害基因的风险。
细菌保护层如何改变战局
金黄色葡萄球菌常通过形成生物膜存活于治疗之中——这是由细胞自生成的基质包埋起来的粘性群落。团队比较了两种常见的基质类型:一种主要由名为Bap的蛋白构成,另一种由称为PIA/PNAG的多糖组成。在实验室测试中,富含Bap的生物膜强烈保护细菌免受ePICI和标准辅助噬菌体的攻击,像致密的护甲阻挡了感染。相反,基于该多糖的生物膜则使细菌更易被杀死,可能是因为病毒外壳上的酶能分解这些糖类,帮助颗粒到达目标细胞。
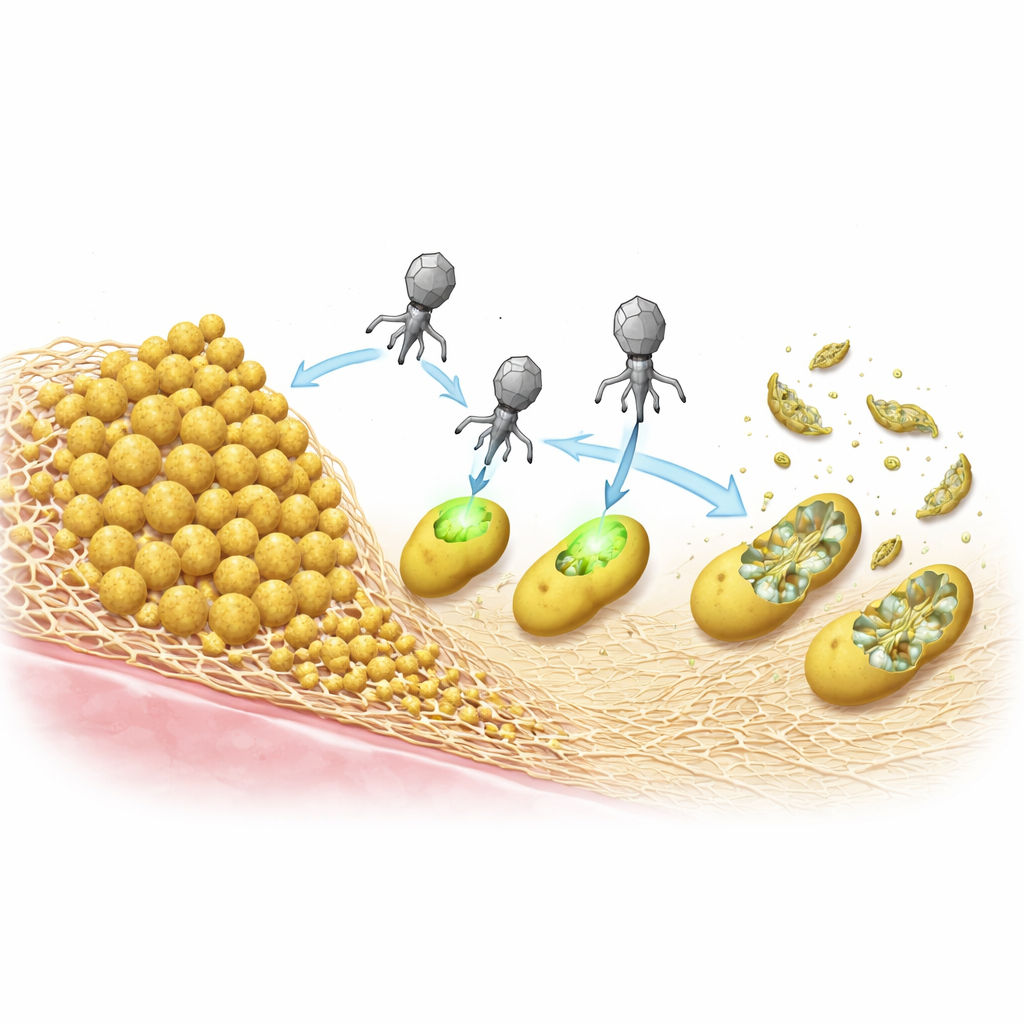
在不整合其DNA的情况下杀死细菌
ePICI进入细胞后可整合入细菌染色体,但研究人员质疑该步骤是否对杀伤是必需的。他们构建了无法进行整合的版本,并证明只要该颗粒在供体菌株中正确产生,其对金黄色葡萄球菌的致死性与原版相当。这意味着CRISPR系统可以直接从进入的环状DNA上表达、完成任务然后随着细胞死亡而消失。这种无需整合的作用进一步降低了意外基因转移的几率,并将这些颗粒与依赖病毒复制和细胞裂解传播的传统噬菌体疗法区分开来。
从培养皿走向被感染的乳腺
由于产Bap株在乳腺炎中常见,团队在模拟乳腺感染的小鼠模型中测试了其表现最佳的构建体ePICIrsaE。在牛奶和实验室培养物中,富含Bap的生物膜明显削弱了ePICI的活性。然而在乳腺组织内,对ePICIrsaE的多次给药显著降低了所有测试菌株的细菌数量,包括那些产生Bap的菌株。其效果可与万古霉素(一种强效的最后线抗生素)相媲美。这些结果表明,活体组织中的条件——例如Bap产量降低、存在自由浮动的细菌或奶中的有利成分——使得工程化颗粒比静态实验室生物膜中表现得更为有效。
这对农场及更广范围意味着什么
研究表明,非复制型、噬菌体封装的CRISPR系统可以在不自我扩散或同时大量裂解细胞的情况下,有选择性地消除与生物膜相关的顽固金黄色葡萄球菌感染。尽管需要高剂量颗粒且从小鼠推广到奶牛存在挑战,这些颗粒为局部感染如乳腺炎提供了一种有前景且可控的抗生素替代方案。更广泛地看,该工作强调在简单的实验室测试中看似不理想的治疗方式,在动物复杂环境中仍可能成功,并为构建针对不同细菌、病毒外壳和引导序列的定制ePICI库打开了大门。
引用: Garmendia-Antoñana, N., Dorado-Morales, P., Gil, C. et al. Targeted elimination of Staphylococcus aureus mastitis infections with synthetic phage-based CRISPR-Cas delivery systems. npj Biofilms Microbiomes 12, 67 (2026). https://doi.org/10.1038/s41522-026-00931-x
关键词: 牛乳腺炎, 金黄色葡萄球菌, CRISPR疗法, 基于噬菌体的治疗, 生物膜感染