Clear Sky Science · zh
肠道微生物群介导慢性多房棘球蚴感染小鼠的抑郁样行为
当隐匿的感染影响心智
大多数人把寄生虫视为肠道或肝脏的问题,而非心智问题。然而,许多长期感染的患者报告情绪低落、乏力和失去愉悦感。本研究探讨了一个出人意料的关联:一种寄居于腹腔和肝脏的慢性绦虫感染如何通过改变肠道细菌和化学物质,促使小鼠出现抑郁样行为。理解这一连串事件最终可能为那些与顽固感染共存的人群保护心理健康提供新思路。
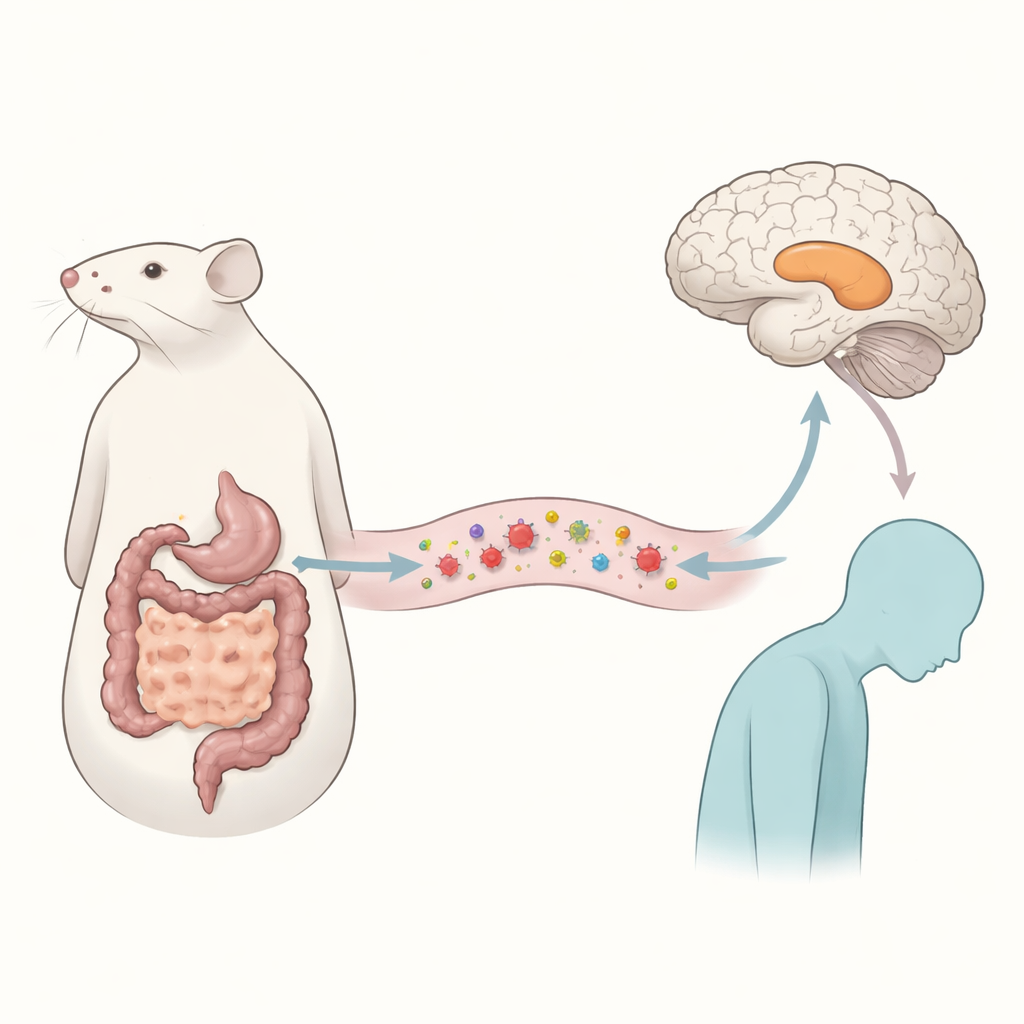
寄生虫旅客与情绪变化
研究者聚焦于多房棘球蚴(Echinococcus multilocularis),该寄生虫引发的包虫病主要严重累及肝脏。患有此病的患者常报告心理健康欠佳,但原因尚不清楚。为探明这一点,研究团队用寄生虫感染小鼠并等待两个月,足以模拟慢性感染。动物随后接受了一系列行为学测试,以区分简单的疾病反应与更特异的情绪改变。感染小鼠的运动量与健康小鼠相当,学习与记忆也正常,但它们表现出明显的抑郁样特征:对甜味奖励兴趣减退,在常用来测量啮齿类动物绝望样状态的应激测试中不动时间增加。
细微的大脑变化与免疫信号
在大脑检测中,科学家将注意力集中在海马和杏仁核——与情绪和应激密切相关的区域。总体结构保持完好,但显微镜下可见部分神经元萎缩或形状异常,细胞核外膜出现皱缩。脑内常驻免疫细胞小胶质细胞在某些区域数量增加,且树突分支更少更简单——这是它们从平静、警戒状态向活化状态转变的典型特征。同时,感染小鼠的肠组织和血液中炎性分子水平升高,尤以细胞因子IL‑6和MCP‑1为著,部分这些信号的基因在海马中的表达也更活跃。综合来看,这些发现指向一种从肠道延伸到大脑的慢性低度炎症状态,推动脑内免疫细胞失衡。
肠道细菌与丧失的化学信使
研究团队接着探究肠道微生物群是否参与其中。通过DNA测序,他们发现感染重塑了肠道微生物群:像乳酸杆菌(Lactobacillus)和双歧杆菌(Bifidobacterium)等有益类群显著减少,而一些属类如瘤胃球菌属(Ruminococcus)和拟杆菌属(Prevotella)扩大。友好菌群减少的个体往往在肠道和血液中具有更高的炎性细胞因子水平。与此同时,血液检测和广泛的代谢物谱分析显示色氨酸—血清素通路的关键成分被耗竭。感染动物的色氨酸(膳食氨基酸)、其中间体N‑乙酰血清素以及神经递质血清素(5‑HT)水平均下降。这些变化类似于重性抑郁症患者报道的改变,并且与特定肠道微生物的丰度密切相关。
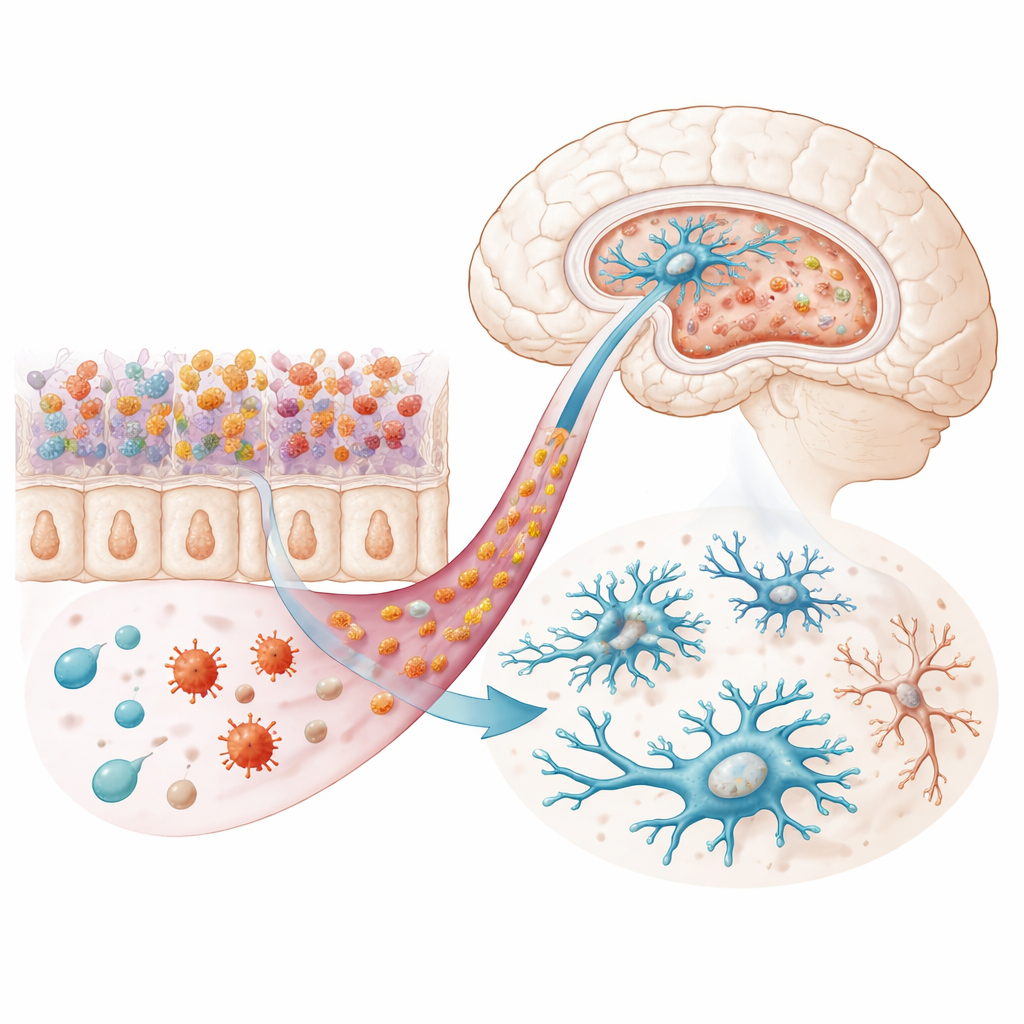
移植微生物群,移植情绪
为检验改变后的微生物群是否足以改变行为,研究者进行了粪菌移植。他们先用抗生素清除健康小鼠的肠道菌群,然后引入来自感染者或未感染供体的粪便。令人惊讶的是,接受来自感染供体微生物群的受体即使自身从未暴露于寄生虫,也会出现抑郁样行为并在开放场地中心区表现出类似焦虑的回避。这些小鼠还表现出炎症增强、血液中色氨酸和血清素相关分子水平降低,以及小胶质细胞呈现与直接感染动物相似的形态——在某些区域更为丰富、分支更少,并充满类似溶酶体的结构,暗示细胞应激或清理活动增加。
对人类健康的意义
对普通读者而言,主要结论是:体内的慢性感染可以扰乱肠道微生物群及其参与生成的化学信使,而这些变化又能影响大脑的免疫细胞和情绪回路。该研究并不主张这种绦虫会直接导致人类的临床抑郁,但它提供了一条详尽的路径图,说明长期寄生、肠道炎症、微生物群失调与色氨酸—血清素化学改变如何协同作用产生抑郁样行为。这个新出现的图景提示,未来治疗慢性感染相关的心理健康并发症可能不仅要清除寄生虫,还需平抑炎症并恢复健康的肠道微生物群。
引用: Wen, R., Xin, Y., Bao, S. et al. The gut microbiota mediates depression-like behaviors in mice with chronic Echinococcus multilocularis infection. npj Biofilms Microbiomes 12, 63 (2026). https://doi.org/10.1038/s41522-026-00929-5
关键词: 肠-脑轴, 微生物组, 寄生虫感染, 抑郁, 色氨酸代谢