Clear Sky Science · zh
膳食纤维缺乏通过富含 miR-6240 的肠道细胞外囊泡加剧肠道炎症
你饮食中的纤维比你想象的更重要
越来越多的人食用经高度加工、被去除天然纤维的食品。本项小鼠研究探究了缺失的纤维对肠道的真实影响。结果显示,低纤维饮食不仅使有益微生物挨饿,还促使肠道上皮释放微小颗粒,这些颗粒会重新编程免疫细胞并加重炎症。理解这一隐藏的链式反应有助于解释现代饮食为何与肠道疾病相关,并可能指向新的治疗途径。
从空盘子到愤怒的肠道
研究者先让小鼠连续四周食用正常饮食或无纤维饮食。缺纤维的小鼠很快出现肠道问题的迹象:结肠变短、损伤增加,保护肠表面的黏液层变薄。显微镜下,组织显示更多损伤和更少的黏液产生细胞。血液和结肠样本显示促炎分子升高、具有保护作用的抑炎分子降低。肠内免疫细胞向更具攻击性的状态转变,连接肠细胞的分子“封闭”变弱,提示肠道屏障更容易漏。
肠道微生物传递第一道信息
由于纤维是肠道细菌的重要食物来源,研究团队还检查了微生物群的变化。无纤维饮食的小鼠微生物组成发生重排:如双歧杆菌和Prevotella等有益群体缩小,而若干机会性或以黏液为食的菌种扩增。为检验仅凭微生物是否足以致病,科学家将来自缺纤维或正常供体的小鼠肠道细菌移植到其原有菌群被清除的新小鼠。尽管这些受体小鼠都吃相同的标准饲料,但接受来自缺纤维供体的细菌者出现了与原先缺纤维动物相似的结肠损伤、炎症和屏障问题。这表明低纤维生活方式可以“刻印”出一种促病微生物群,并能将肠道问题传递给他人。
微小囊泡将饮食信号转化为免疫问题
随后研究超越了微生物,考察了机体自身细胞。肠上皮细胞持续释放纳米级囊泡,称为细胞外囊泡,它们携带分子信息。作者从正常和无纤维小鼠中分离出这些囊泡并给予健康动物。来自缺纤维肠道的囊泡足以诱发结肠损伤、黏液减少、促炎分子升高以及屏障蛋白减弱,即使受体动物饮食未改变。在这些囊泡内部,团队发现了一组独特的小型调控RNA谱,其中一种名为 miR-6240 的小RNA 在低纤维状态下显著增加。当将这种单一RNA导入培养皿中的免疫细胞时,它促使这些细胞走向更具炎症性的表型,并间接损伤邻近的肠细胞。
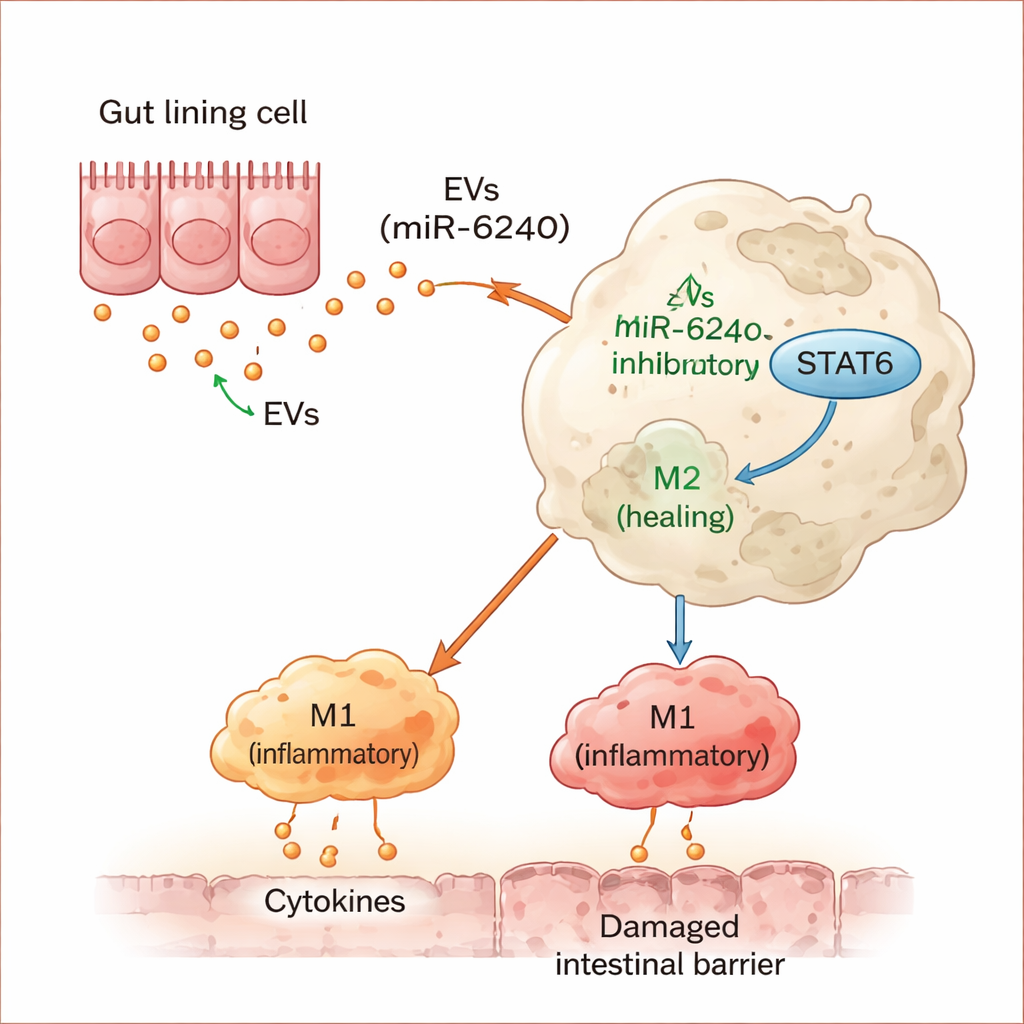
单一分子开关倾斜免疫平衡
进一步深入研究表明,miR-6240 直接靶向一种名为 STAT6 的蛋白,STAT6 通常有助于引导巨噬细胞——关键免疫细胞——走向修复与“清理”模式。通过抑制 STAT6,miR-6240 阻断了这一缓和通路,使巨噬细胞转向更具破坏性的组织损伤状态。给予小鼠合成形式的 miR-6240 可再现结肠中许多与纤维缺乏相关的特征,包括炎症、黏液丧失和屏障削弱。相反,在免疫细胞中阻断 miR-6240 可减轻来自缺纤维肠道囊泡的有害效应。当携带 miR-6240 的巨噬细胞被转移到健康小鼠体内时,受体也发生了肠道炎症,强调了这一单一信号的强大作用。
这对日常饮食意味着什么
对非专业读者来说,结论很直接:不吃纤维不仅改变肠道中哪些细菌生存,还改变你自身肠细胞与免疫系统的对话方式。低纤维饮食重塑微生物组,并促使肠上皮细胞释放富含 miR-6240 的囊泡,而这些囊泡则在免疫细胞中关掉保护性开关(STAT6),加剧炎症。尽管这种特定的 RNA 可能以小鼠为主,但这一普遍原理很可能更广泛地适用——我们吃的东西可以改写肠内的分子信息,决定肠道是保持平静还是走向炎症。恢复纤维摄入或针对类似分子通路的干预,或许有朝一日能帮助预防或治疗与饮食相关的肠道疾病。
引用: Song, M., Zhou, W., Fan, J. et al. Dietary fiber deficiency exacerbates intestinal inflammation via miR-6240-enriched gut extracellular vesicles. npj Biofilms Microbiomes 12, 53 (2026). https://doi.org/10.1038/s41522-026-00918-8
关键词: 膳食纤维, 肠道微生物组, 肠道炎症, 细胞外囊泡, 微小RNA