Clear Sky Science · zh
口腔微生物驱动的免疫调节沿口腔—肠道轴:从局部信号到全身性炎症
为什么你的口腔与全身健康息息相关
生活在你口腔中的细菌不仅仅会导致蛀牙或口臭。本文综述解释了口腔微生物如何进入肠道,扰乱其脆弱的防御,并促发可波及肝脏和大脑等器官的炎症。理解这一隐秘的“口腔—肠道轴”为从脂肪肝疾病到阿尔茨海默病等常见问题提供了新线索,也指向一些出乎意料但简单的措施——例如更好的口腔护理和饮食——可能有助于保护我们的整体健康。
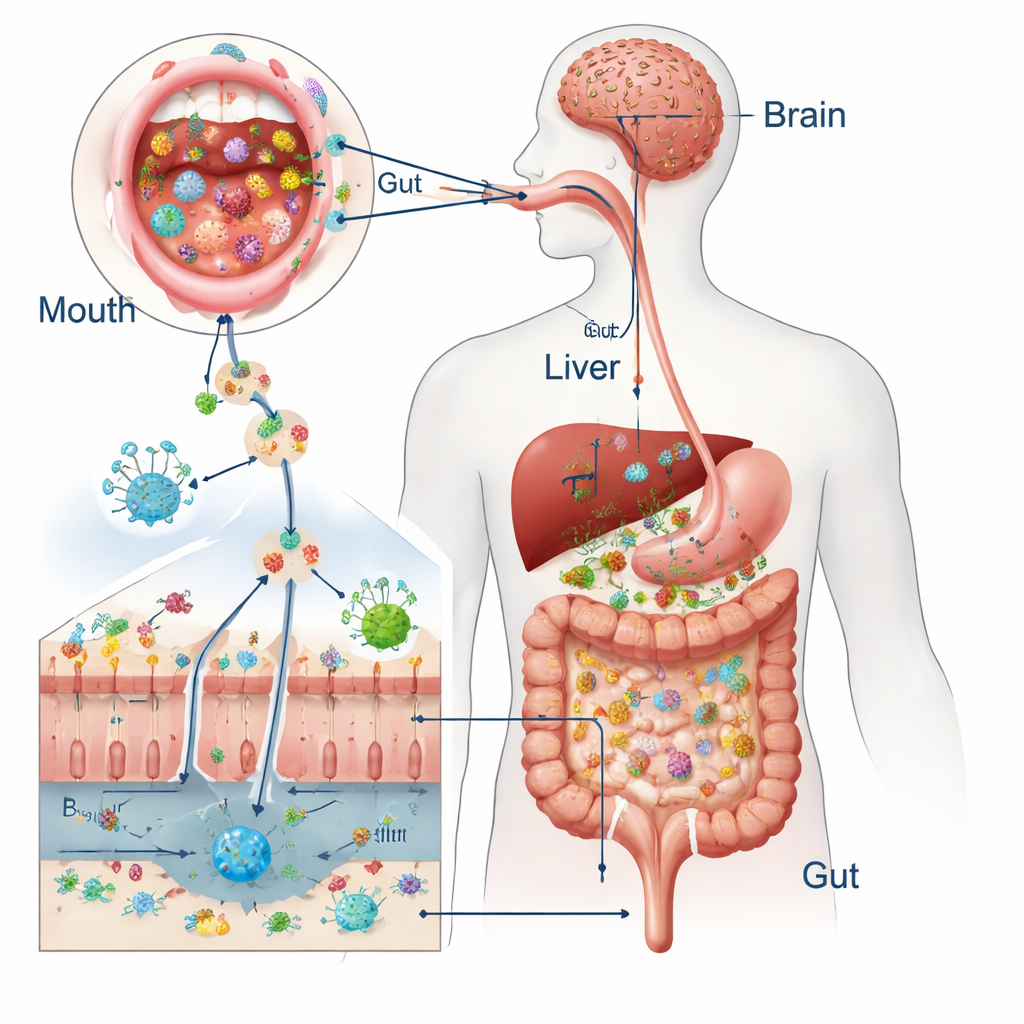
从吞咽到全身性效应
我们每天会吞下大约一到一点五升唾液,里面装着数十亿的口腔微生物。在健康人群中,强有力的防御机制——唾液的天然抗微生物成分、胃酸、胆汁、粘稠的黏液以及紧密连接的肠上皮细胞——阻止大多数这些“访客”在肠道定居。比较口腔与粪便中微生物的研究显示,在一切运作良好时,来自口腔的微生物仅占肠道微生物群的一小部分。但两者生态系统有一定重叠,像链球菌(Streptococcus)和维氏菌属(Veillonella)等口腔种类有时可在肠道中被检测到,引发了它们何时从无害过客变为长期定居者的问题。
当屏障失效时
在压力下,情形会发生改变。衰老、口干、口腔卫生差以及慢性牙龈病会使有害菌在口腔中过度繁殖。抗生素和抑酸药等药物通过使黏液变薄、松动细胞间连接并让更多微生物在穿过胃时存活,从而削弱肠道防御。口腔感染和牙科手术甚至可能将细菌推入血流。综述还强调了细菌胞外囊泡——微生物释放的纳米级“包裹”——它们能穿透组织并携带炎性信号远离源头。一些口腔细菌,如牙龈卟啉单胞菌(Porphyromonas gingivalis)和核梭杆菌(Fusobacterium nucleatum),甚至能藏匿在免疫细胞内,像微生物“特洛伊木马”一样随细胞巡游全身。
口腔细菌如何学会在肠道生存
并非所有到达肠道的口腔微生物都能在那里停留。能够定居的往往拥有特殊的生存技巧。某些菌株会改造其细胞膜以耐受强酸或胆汁;另一些以覆盖肠壁的黏液中的糖类为食,或与定居肠道细菌联手形成黏附性生物膜。同时,它们学会规避免疫监视。有些能够抑制自然杀伤细胞和T细胞的杀伤能力;另一些干扰通常检测微生物成分并触发保护性反应的早期警报感测器。通过推动免疫细胞向更具炎性表型而减少调节性“刹车”的平衡,它们创造出一个有利于长期、低水平定殖的生态位。
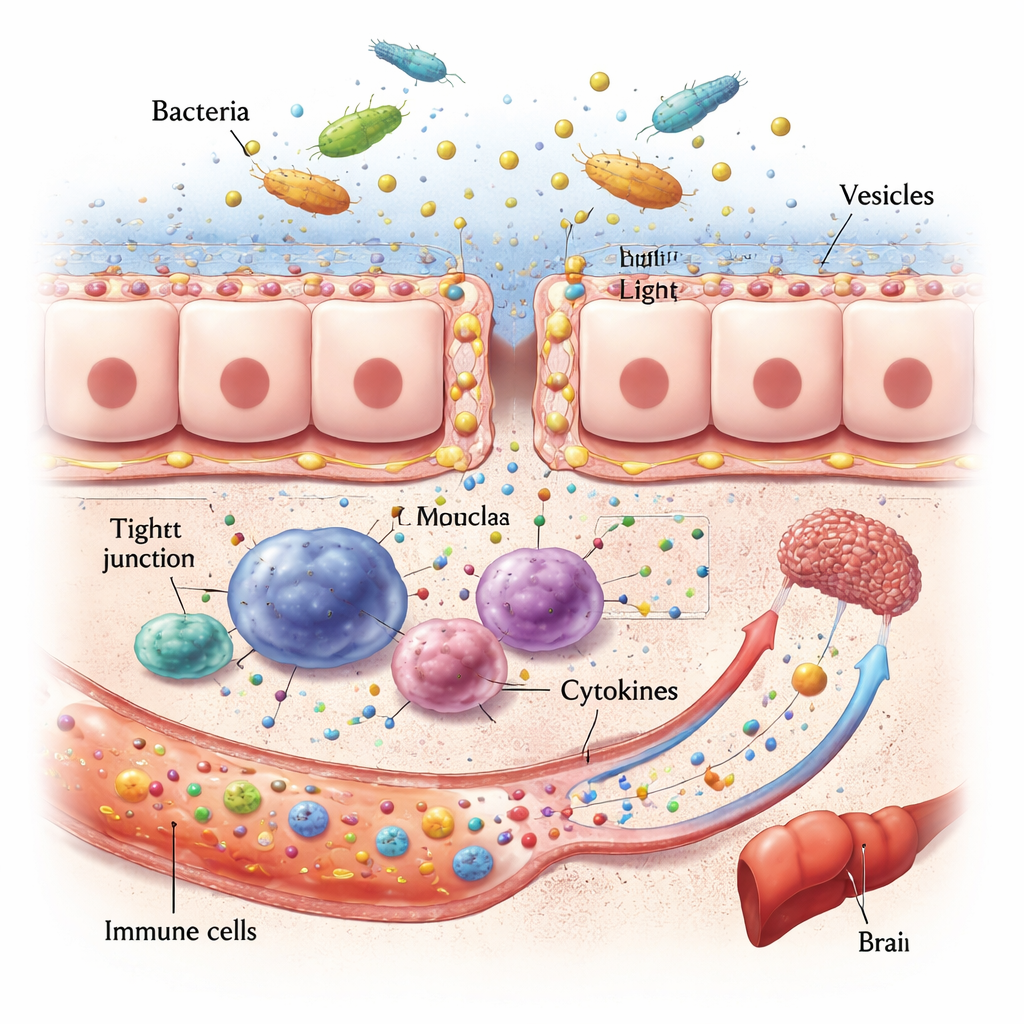
从肠道通透性到器官受损
一旦定植,侵袭性的口腔微生物及其囊泡可以破坏肠道的一线防线。它们会分解将相邻细胞封接在一起的蛋白,削薄黏液层,甚至直接杀死肠上皮细胞。这使肠壁更具通透性,细菌碎片和毒素得以渗入血流。在那里,它们激活免疫细胞并引发称为细胞因子的信号爆发。由于来自肠道的血液直接流向肝脏,该器官尤为容易受到影响:动物和人类数据都将口腔病原体与脂肪性肝病、纤维化和加剧的炎症联系起来。类似通路将口腔失衡和肠道破坏与大脑相连,在那里慢性炎症和改变的微生物代谢产物似乎会加剧与阿尔茨海默病相关蛋白的沉积并扰乱情绪与认知。
新的干预途径
认识到口腔—肠道轴为预防和治疗提供了多层策略。在口腔方面,常规牙周治疗、光疗和天然抗微生物肽可以降低有害细菌并减少进入肠道的数量。在肠道方面,益生菌、高纤维饮食以及恢复短链脂肪酸的补充剂有助于重建肠道屏障并平抑过度活跃的免疫反应。展望未来,将微型口腔、肠道、肝脏和大脑组织连接起来的复杂“器官芯片”装置,结合哪些微生物诱发哪些免疫反应的大数据图谱,或可实现个性化的慢性炎症性疾病预防方法。
这对你的意义
对普通读者而言,核心信息是:口腔并非法外之地——其微生物能够塑造肠道健康,并通过肠道影响全身。当口腔细菌绕过或侵蚀自然屏障时,它们可能助推对肝脏和大脑等远端器官的长期炎症。文章的结论是,保护口腔健康、维护肠道屏障,并通过有针对性的干预温和引导我们的微生物群,可能成为对抗现代慢性疾病的重要工具。
引用: Li, C., Fan, Y. & Chen, X. Oral microbiota–driven immune modulation along the oral–gut axis: from local signals to systemic inflammation. npj Biofilms Microbiomes 12, 46 (2026). https://doi.org/10.1038/s41522-026-00912-0
关键词: 口腔微生物组, 肠道屏障, 全身性炎症, 肝脏疾病, 大脑健康