Clear Sky Science · zh
酶增强抗生素治疗在一种植入物相关感染模型中将生物膜降低到不可检测水平
顽固植入物感染为何重要
髋关节和膝关节置换能改变生活质量,但当细菌在这些金属植入物上定植时,会形成称为生物膜的黏性群落。这些生物膜就像有装甲的城市,保护病原体免受免疫系统和抗生素的攻击,导致疼痛且长期难治的感染。本研究探讨了一种新的双管齐下治疗策略:先削弱生物膜的防御,然后用高剂量抗生素进行局部冲击——这种方法将来有望帮助更多保留原有植入物,而不是更换它们。
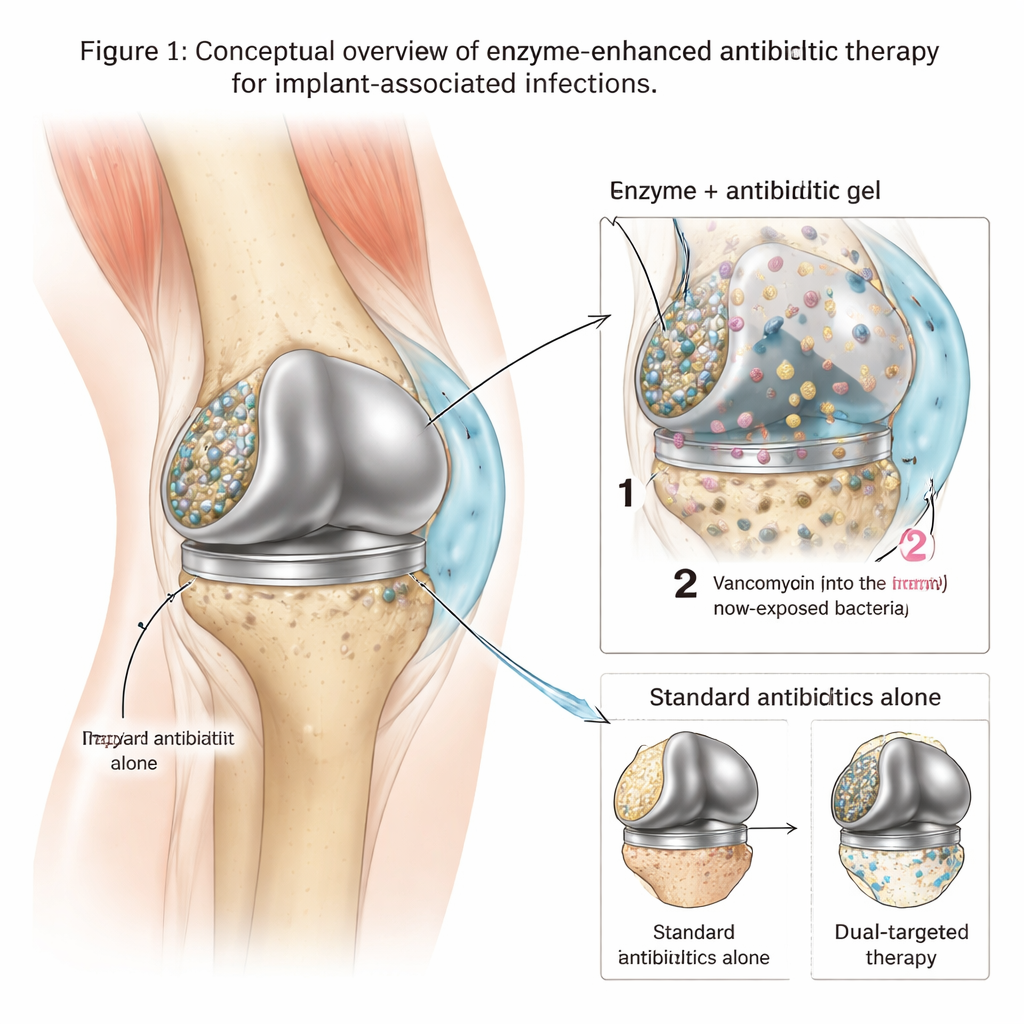
金属植入物上的隐蔽据点
当甲氧西林耐药金黄色葡萄球菌(MRSA)等细菌附着在人工关节上时,它们迅速在金属表面构建由DNA、糖类和其他分子组成的黏性基质。在这个受保护的生物膜内部,细菌生长缓慢、行为改变,并能耐受比游离细菌高出数百甚至数千倍的抗生素浓度。因此,标准治疗——即使是像万古霉素这样强效的药物——常常无法完全清除感染,迫使患者接受反复手术或彻底更换植入物。临床上需要的不仅是杀死细菌的工具,还需要能打破其保护堡垒、让药物到达目标的策略。
一种能递送酶和抗生素的智能凝胶
研究者设计了一种基于热敏水凝胶的局部治疗,所用材料为聚氧化烷-407(poloxamer 407)。该凝胶在低温下为液体,便于注射到植入物周围,但在体温下迅速凝固成柔软固体,有助于固定位置。研究团队在凝胶中装载了两种关键成分:一种强效抗生素(万古霉素)和由三种酶组成的混合物,这些酶能分解生物膜基质的主要成分。在体外测试中,他们调控凝胶使酶优先释放——松动并稀释生物膜——而万古霉素则缓慢释放,持续数天,在细菌所在的局部维持极高的药物浓度。
从实验皿到豚鼠模型
为检验该策略是否有效,研究团队先在实验室对钛片上生长的生物膜进行了测试,随后在模拟植入物感染的豚鼠模型中进行了验证。在体外实验中,间隔48小时进行两次酶-抗生素凝胶应用,可使金属表面活菌数降低超过10万倍,并几乎消除生物膜总量。在动物实验中,研究者在皮下外科植入带孔的笼子,内含钛珠,并用MRSA感染,然后用不同组合的全身抗生素和局部凝胶进行处理。最有效的方案包括:(1)局部凝胶同时含酶与万古霉素,给予两次;以及(2)全身给药的万古霉素加第二种抗生素利福平,后者对穿透生物膜特别有效。
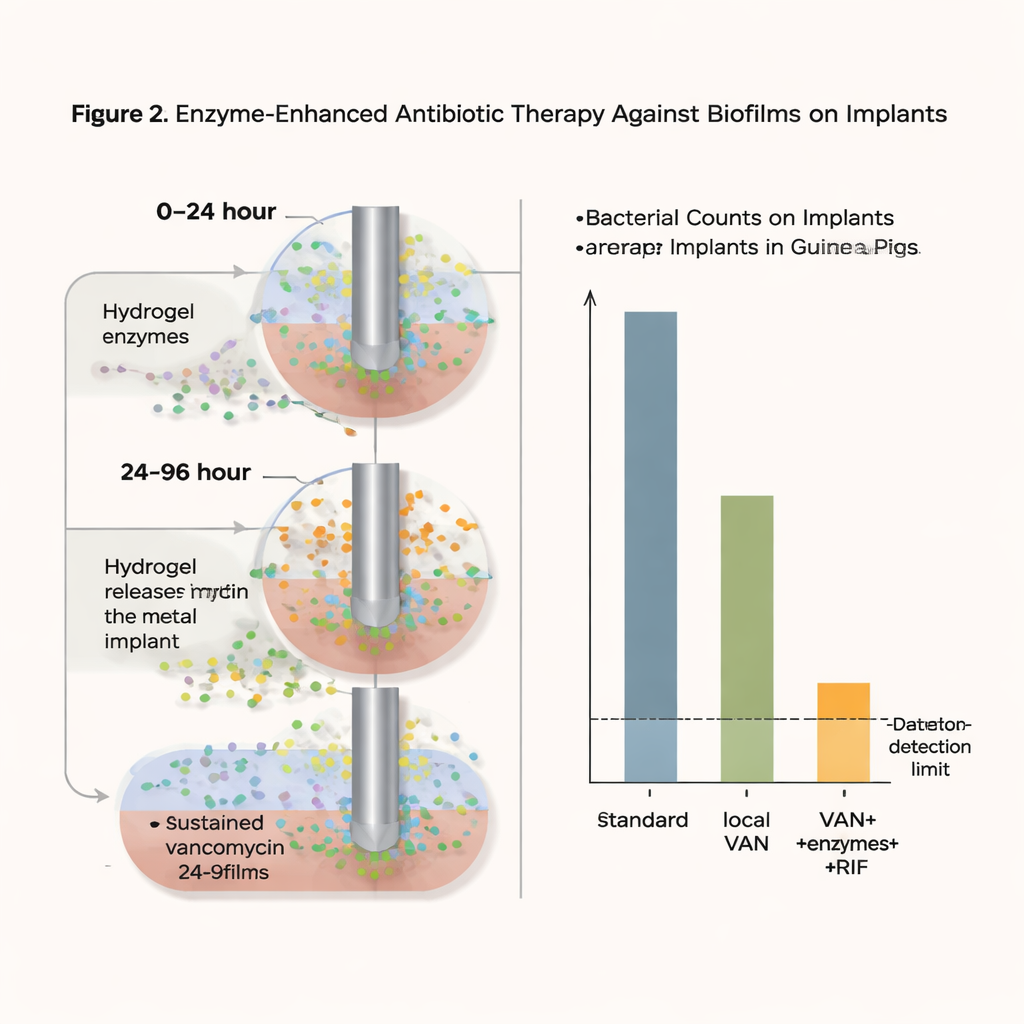
该新方法取得的成果
通过这种强效但局部化的策略,植入材料上的细菌计数降至检测下限——在该模型中实际上为“无可回收细菌”——治疗结束后一日,75%的处理笼子达到该水平;即使在五天后,仍有37.5%的笼子无可检测细菌。重要的是,未观察到万古霉素抗性增加,高局部万古霉素浓度似乎也阻止了利福平耐药菌株的出现。使用培养细胞和重建人皮模型进行的安全性测试未发现凝胶配方导致毒性或刺激的迹象。尽管在某些情况下仍出现轻微的细菌再生长,且治疗周期短于临床常规,但结果表明,将破坏生物膜的酶与持续的局部抗生素释放结合,能显著缩小 otherwise 顽固的感染规模。
这对患者可能意味着什么
对于面临植入物相关感染的患者,这项工作指向了一个未来:外科医生或许可以向被感染的关节周围注入一种智能凝胶,而不是立即拆除或更换植入物。先削弱生物膜屏障,再以高且持续的局部抗生素剂量冲击该区域——并辅以全身治疗——这种双重靶向策略旨在将细菌数量压低到不可检测水平并降低耐药风险。尽管仍需更多研究、更长的疗程和人体试验,但该方法为将一些最顽固的骨科感染转变为更可控乃至可治的病症提供了有希望的蓝图。
引用: Buzisa Mbuku, R., Poilvache, H., Maigret, L. et al. Enzymes-enhanced antibiotic therapy reduces biofilms to undetectable levels in an implant-associated infection model. npj Biofilms Microbiomes 12, 44 (2026). https://doi.org/10.1038/s41522-026-00910-2
关键词: 生物膜感染, 骨科植入物, 万古霉素, 酶治疗, 利福平