Clear Sky Science · zh
多层分子分析为硬化性小圆细胞瘤的诊断与靶向治疗提供信息
一种亟需更好答案的罕见癌症
硬化性小圆细胞瘤(DSRCT)是一种极为罕见且侵袭性的癌症,主要影响儿童、青少年和年轻成人。由于其发生率极低且在显微镜下可与其他肿瘤相似,医生常常难以做出准确诊断并选择有效治疗。本研究提出了一个简单但具有重要意义的问题:如果我们在多个分子层面上深入分析DSRCT肿瘤——不仅是DNA,还包括RNA、蛋白质模式和DNA上的化学标记(甲基化)——是否能同时提升诊断准确性并为已无标准疗法可用的患者发现新的、更精准的治疗选择?
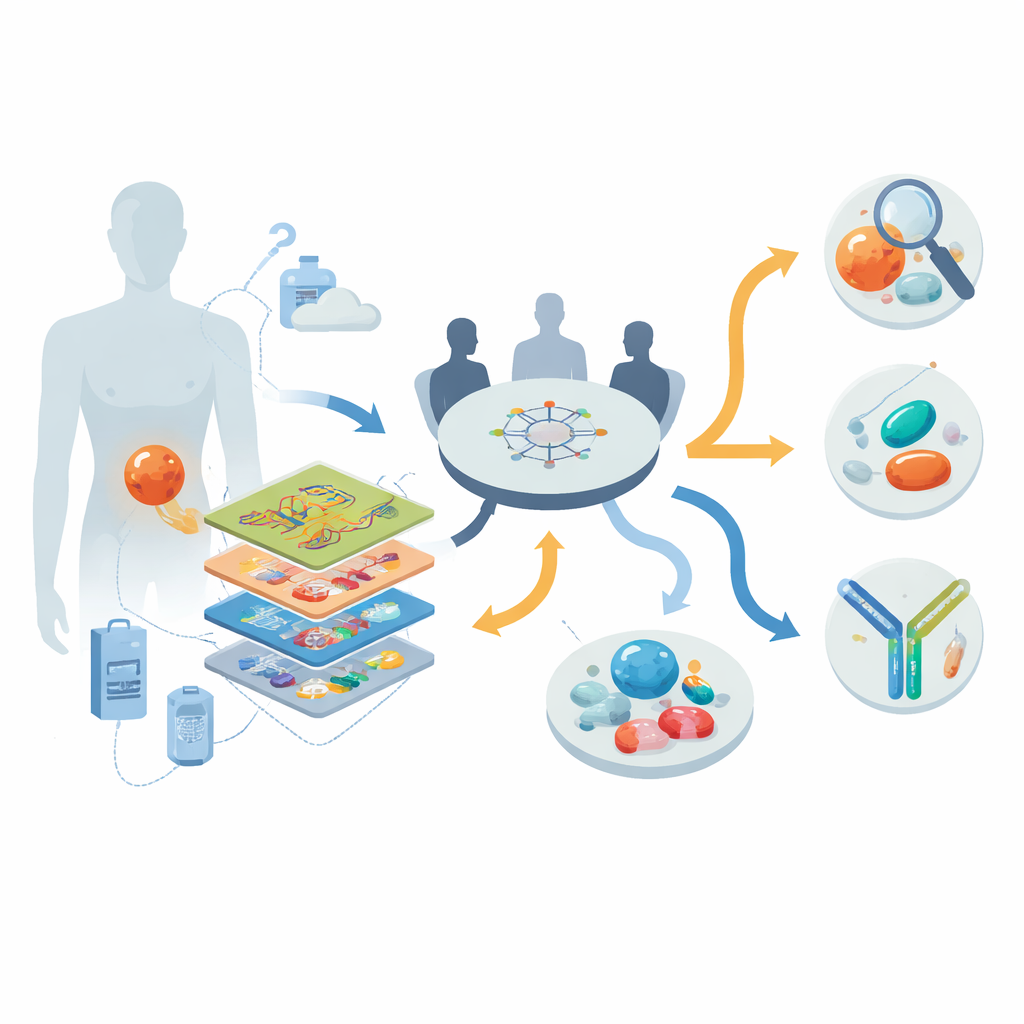
逐层剖析肿瘤内部
研究者在德国全国性的精准肿瘤学项目框架下开展工作,于2013年至2022年间招募了30例晚期、主要为耐药的DSRCT患者。对每位患者,他们应用了一套“多组学”工具包:全基因组或外显子测序用于研究DNA;RNA测序用于观察哪些基因处于活跃状态;DNA甲基化谱用于捕捉表观遗传指纹;在9名患者中,还进行了蛋白质与磷酸化蛋白的详细测定,以揭示哪些信号通路真正处于活跃状态。随后,多学科肿瘤委员会将这些数据与每位患者的临床病史共同审阅,以生成个体化的诊断澄清、靶向药物和临床试验建议。
纠正误诊并揭示隐藏的靶点
一个显著发现是深度分析在多大程度上纠正了原始诊断。在30例患者中,有8例最初被标注为其他实体——例如来源不明的癌症或定义模糊的肉瘤——在发现一个标志性基因融合(EWSR1::WT1)和特征性的甲基化模式后,被重新归类为DSRCT。与此同时,这些肿瘤的DNA相对“安静”:突变很少,拷贝数变化也偶见,因此经典的“突变基因=药物靶点”方法收效甚微。相反,最丰富的线索来自RNA和蛋白层面。通过将DSRCT的基因活性与数百例其他肉瘤比较,研究团队反复发现若干表面分子和信号酶的过度表达,这些分子在原则上可被现有或新兴药物所针对。
从分子信号到定制治疗
基于这些模式,肿瘤委员会为30例患者中的28例提出了107条基于分子信息的管理建议。大多数建议涉及阻断酪氨酸激酶的药物——这类关键酶驱动细胞生长和血管生成——或是针对高表达表面蛋白的新策略。例如小分子激酶抑制剂如帕唑帕尼(pazopanib);针对生长抑素受体的肽放射治疗;针对黏附分子CLDN6的实验性CAR-T细胞;以及将毒素递送至表达ERBB2(HER2)受体细胞的抗体-药物偶联物。17例患者被认为符合生物标志物匹配的临床试验入组条件,强调了详尽分子数据如何为罕见疾病患者打开原本难以获得的研究通道。
对经多线治疗患者的真实世界影响
在所有建议的个体化疗法中,16项实际用于13名患者,全部基于RNA层面的信号,并在有时结合磷酸蛋白数据进一步细化。尽管这些患者已接受多轮化疗和局部治疗,13名患者中仍有8名实现了疾病控制——5名出现部分肿瘤缩小,3名为疾病稳定。多靶点酪氨酸激酶抑制剂(最常为帕唑帕尼)在若干患者中带来了显著且有时持久的益处,尤其是在肿瘤中该药已知靶点明显过度活跃时。或许最值得注意的是两名高ERBB2表达的患者接受了抗体-药物偶联物曲妥珠单抗德鲁昔单抗(trastuzumab deruxtecan,T-DXd),两人均获得长达两年或更久的持久反应,尽管他们之前已耗尽多种疗法,且ERBB2受体并未显示出传统ERBB2阻断药通常要求的那种强激活模式。
这对患者及未来护理意味着什么
对于DSRCT患者,这项研究传递了一个审慎的乐观信息。尽管这种癌症缺乏明显可利用的DNA突变,但跨多个分子层面的分析既能纠正误诊,又能揭示常规检测看不到的可攻弱点。该研究表明,即便在一种罕见且侵袭性的疾病中,以生物学为导向的方法也能带来真实的临床获益,包括对帕唑帕尼和曲妥珠单抗德鲁昔单抗等药物的耐久反应。更广泛地讲,研究主张让DSRCT患者——以及由此类推其他超罕见癌症患者——常规获得全面分子谱分析与专家评审,这将为未来按个体肿瘤独特分子指纹而非仅按肿瘤类型选择治疗的试验铺平道路。
引用: Renner, M., Oleś, M., Paramasivam, N. et al. Multi-layered molecular profiling informs the diagnosis and targeted therapy of desmoplastic small round cell tumor. Nat Commun 17, 3397 (2026). https://doi.org/10.1038/s41467-026-71636-0
关键词: 硬化性小圆细胞瘤, 精准肿瘤学, 多组学分析, 靶向治疗, 抗体药物偶联物