Clear Sky Science · zh
依赖于 SLC33A1 与非依赖性 Golgi 神经氨酸 O-乙酰化在 CASD1 催化中的相互作用
微小糖修饰如何影响健康与疾病
我们的细胞表面覆盖着复杂的糖链,像分子身份证一样,引导免疫反应、发育过程,甚至决定病毒如何附着。该研究探讨了一种微妙但影响深远的糖修饰——在名为唾液酸的末端糖上添加小的化学“帽子”即乙酰基——并揭示了在细胞高尔基体内控制这一过程的意想不到的双重分子机制。理解这一潜在体系有助于解释某些严重的神经系统疾病,并为细胞如何在健康与疾病状态下精细调节其表面提供线索。 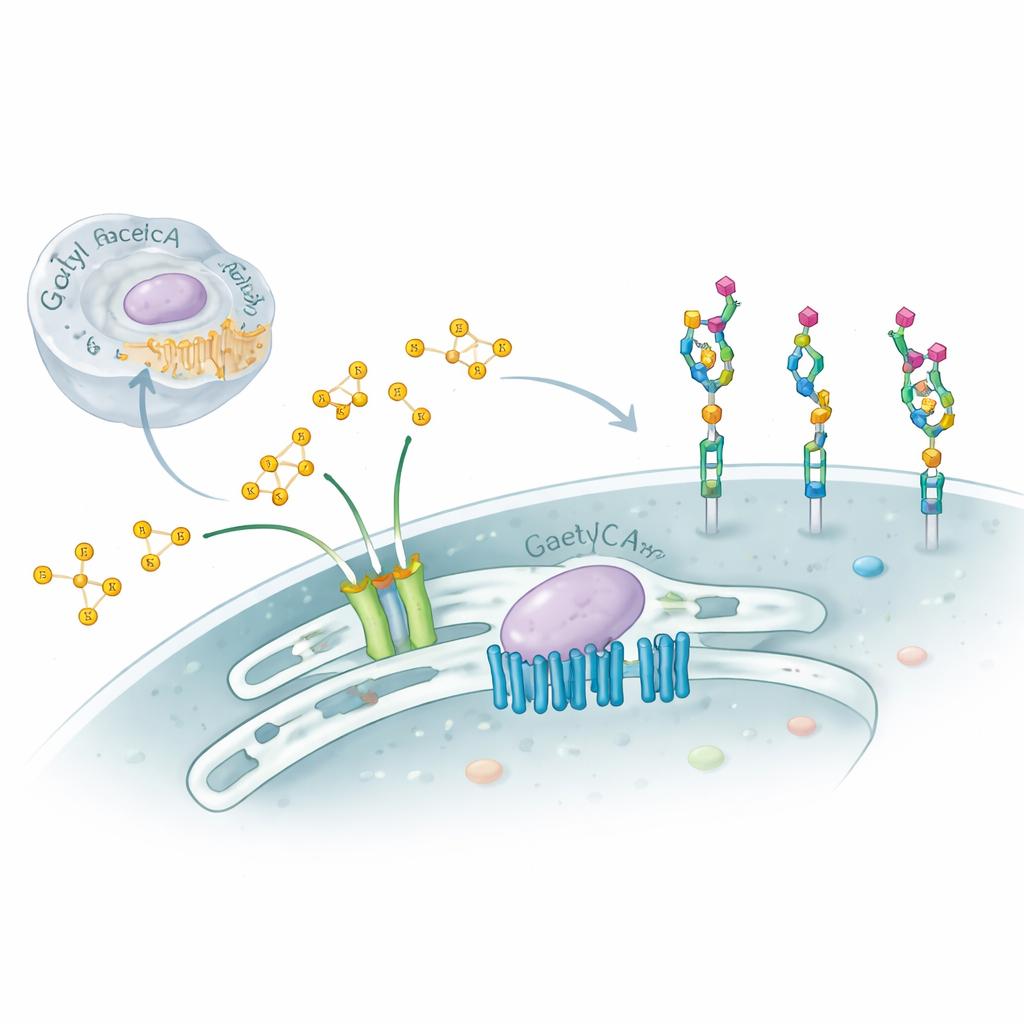
细胞表面的特殊糖
唾液酸位于许多细胞表面糖类(附着在蛋白质和脂质上)的外端,尤其是在大脑中的神经节苷脂上。通过对唾液酸进行微小修饰——例如在特定位置添加一到两个乙酰基——细胞可以掩盖现有的识别位点或创造新的位点。流感 C 型病毒和一些冠状病毒等会特异性识别这些被修饰的糖,而乙酰化的神经节苷脂会影响神经细胞的生存或死亡,以及肿瘤的生长。尽管重要性显著,但将这些乙酰基置入高尔基体的细胞机器的内部工作机制长期以来仍知之甚少。
一个转运蛋白与一个酶通力合作
研究人员聚焦于两个定位于高尔基体或其周围的蛋白:SLC33A1,一种将乙酰‑CoA(细胞主要的乙酰供体)跨膜运输的转运蛋白;以及 CASD1,一种已知能将乙酰基转移到唾液酸上的酶。通过在人类和仓鼠细胞系中进行基因编辑,他们敲除了 SLC33A1 并观察特定神经节苷脂的变化。缺失 SLC33A1 的细胞仍能合成基础的神经节苷脂 GD3 和 GD2,但完全丧失了其 9‑O‑乙酰化形式——这种修饰与癌症和神经功能相关。重新引入人源 SLC33A1 可恢复这些乙酰化神经节苷脂,表明 SLC33A1 是该通路乙酰‑CoA 的关键供应者。 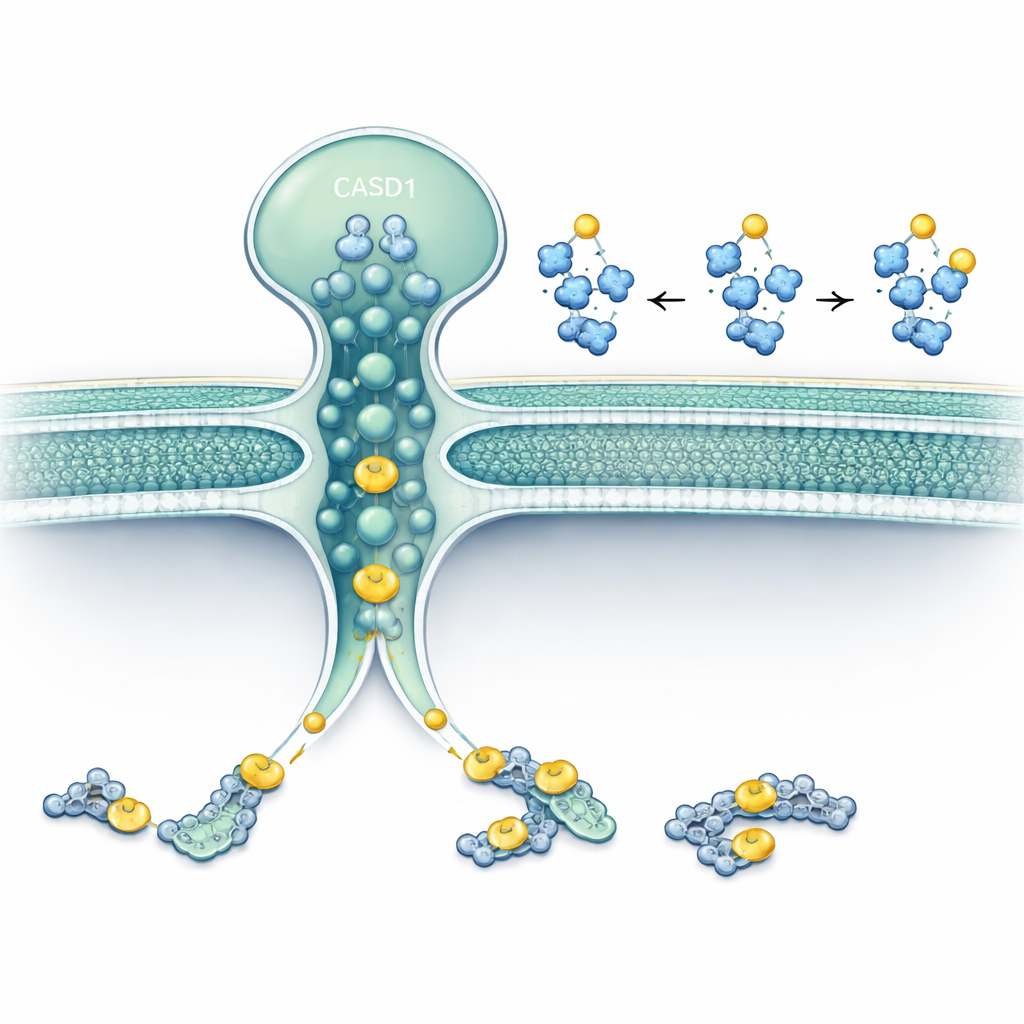
患者突变揭示医学相关性
SLC33A1 与若干罕见神经系统疾病有关,包括一类严重的儿童疾病(Huppke–Brendel 综合征)、一种遗传性痉挛性截瘫形式以及晚发性小脑共济失调。研究团队在缺失正常转运蛋白的细胞中重建了四种来源于患者的 SLC33A1 变体,并测试这些突变蛋白是否能挽救神经节苷脂的乙酰化。四种变体均显示功能下降,其中儿童发病的最严重突变几乎无法恢复任何乙酰化。基于最近解析的 SLC33A1 三维结构,作者将这些突变映射到蛋白上,展示了它们很可能如何扰乱蛋白构象或其结合乙酰‑CoA 的能力。这强烈提示受损的神经节苷脂乙酰化可能促成患者出现的神经症状。
CASD1 中隐藏的第二个活性位点
研究还揭示了一个意外转折:CASD1 本身似乎是一个具有双重功能的酶。其已知的位于高尔基体腔内的结构使用由 SLC33A1 递送的乙酰‑CoA。但在敲除 SLC33A1 时,细胞在某些条件下仍能在某些唾液酸上放置单个乙酰基,尽管它们无法添加形成更复杂修饰模式所需的第二个乙酰基。利用先进的结构预测和分子模拟,作者显示 CASD1 的跨膜部分与来自溶酶体的已知跨膜乙酰转移酶高度相似。他们定位了该区域中与乙酰‑CoA 在胞质侧结合并直接将乙酰基穿膜传递到唾液酸的关键氨基酸残基。当这些残基被突变时,CASD1 在体外测定和活细胞中均丧失了这一第二项活性。
两条途径,构成精细调控的糖编码
综上数据支持“两个催化位点”模型。一条路径依赖于 SLC33A1 将乙酰‑CoA 运入高尔基体腔内,在那里 CASD1 的腔内结构域向唾液酸添加乙酰基,从而实现单乙酰或双乙酰的修饰模式。另一条路径内嵌于 CASD1 的跨膜核心,可以直接利用胞质侧的乙酰‑CoA 并在 SLC33A1 缺失时仍提供基础水平的乙酰化。通俗地说,这意味着单一酶借助两种不同的乙酰来源,在细胞表面糖类上写下微妙的“标点”。当该转运蛋白或酶的任一部分功能异常时,这些标记会错位或消失,这或可解释某些神经发育和神经退行性疾病,并凸显了细胞如何塑造其外部身份的一个新型调控层面。
引用: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
关键词: 唾液酸, 高尔基体乙酰化, 神经节苷脂, SLC33A1, CASD1