Clear Sky Science · zh
在泛素非依赖底物周转过程中中脑蛋白-蛋白酶体的结构动力学
细胞如何迅速清理“垃圾”
在每个细胞内,蛋白质不断被合成与降解。许多蛋白质在进入细胞的主要回收机器——蛋白酶体之前,会被小分子泛素标记。但有些核内蛋白必须被极为迅速地清除,以至于没有时间进行标记。本研究揭示了一种鲜为人知的辅助蛋白midnolin如何直接插入蛋白酶体以清除这些紧急靶标,提供了细胞如何对基因活性进行快速而精确控制的线索。
通往细胞“粉碎机”的捷径
26S蛋白酶体是一个桶状复合体,将蛋白质分解为小片段。传统观点认为它通过识别附着在靶标上的泛素链来识别降解对象。近期研究发现了一条替代路径:一种“捷径”途径,其中midnolin将某些核内蛋白——尤其是那些快速开启或关闭基因表达的即刻早期基因产物——直接护送到蛋白酶体,且无需任何泛素标记。这类蛋白,例如参与应激反应和炎症的转录因子,必须在数分钟内出现又消失。新论文结合高分辨率冷冻电镜与生化实验,几乎以逐帧方式描绘了midnolin如何锁定蛋白酶体并将其货物定位以便被降解。
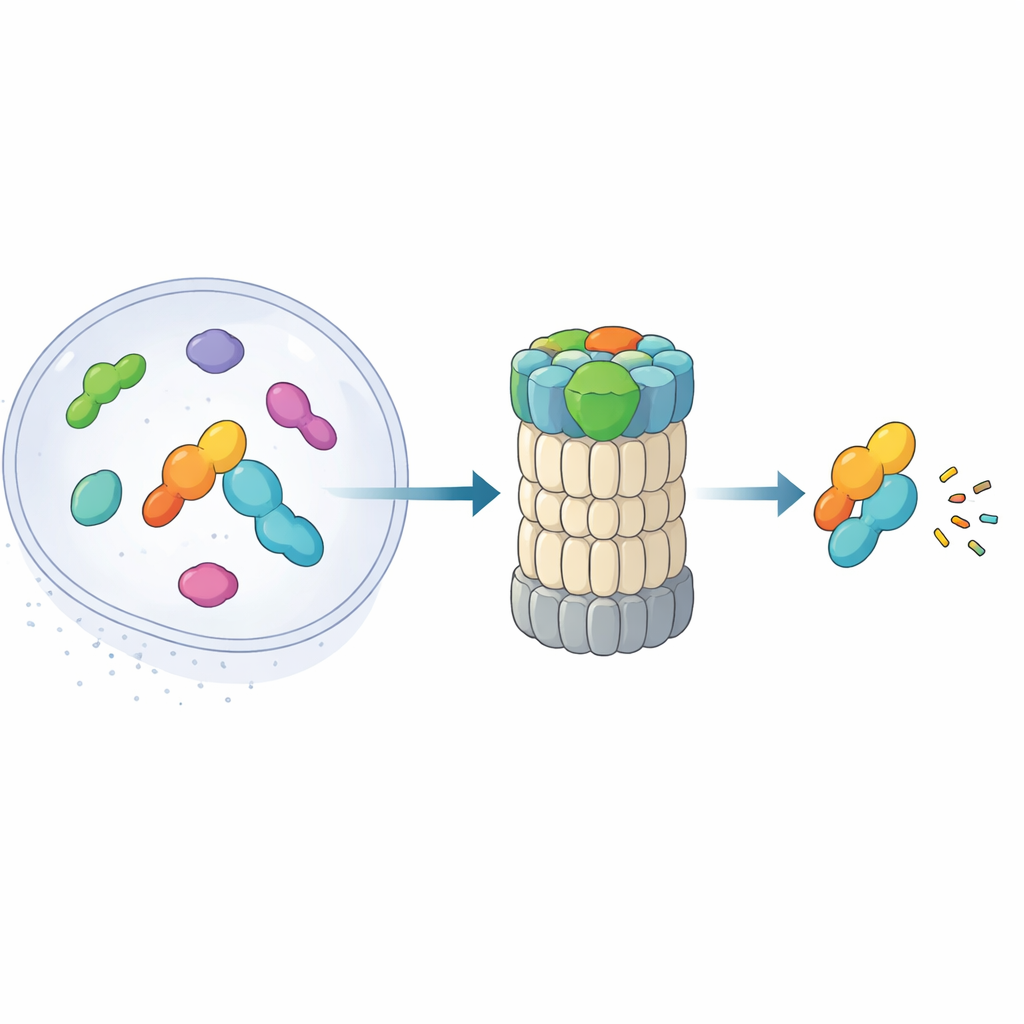
抓取并瞄准靶标的三段式助力器
Midnolin像一个具有三个关键模块的多功能工具。一端的C端螺旋插入蛋白酶体组分RPN1上的一个对接位点,将midnolin锚定在回收机器上。中间的“Catch”区域识别并紧握靶蛋白上的特定链状特征(degron)。在另一端是一个类泛素结构域。出人意料的是,这个结构域并不像其他运输蛋白中的类似结构那样主要用于结合蛋白酶体。作者显示,它贴靠在RPN11上——一种通常负责从底物上切除泛素的酶。在这里,RPN11更像一个支架:通过拥抱midnolin的类泛素段,它有助于将Catch结构域及其结合的货物直接保持在蛋白酶体狭窄入口孔的正上方。
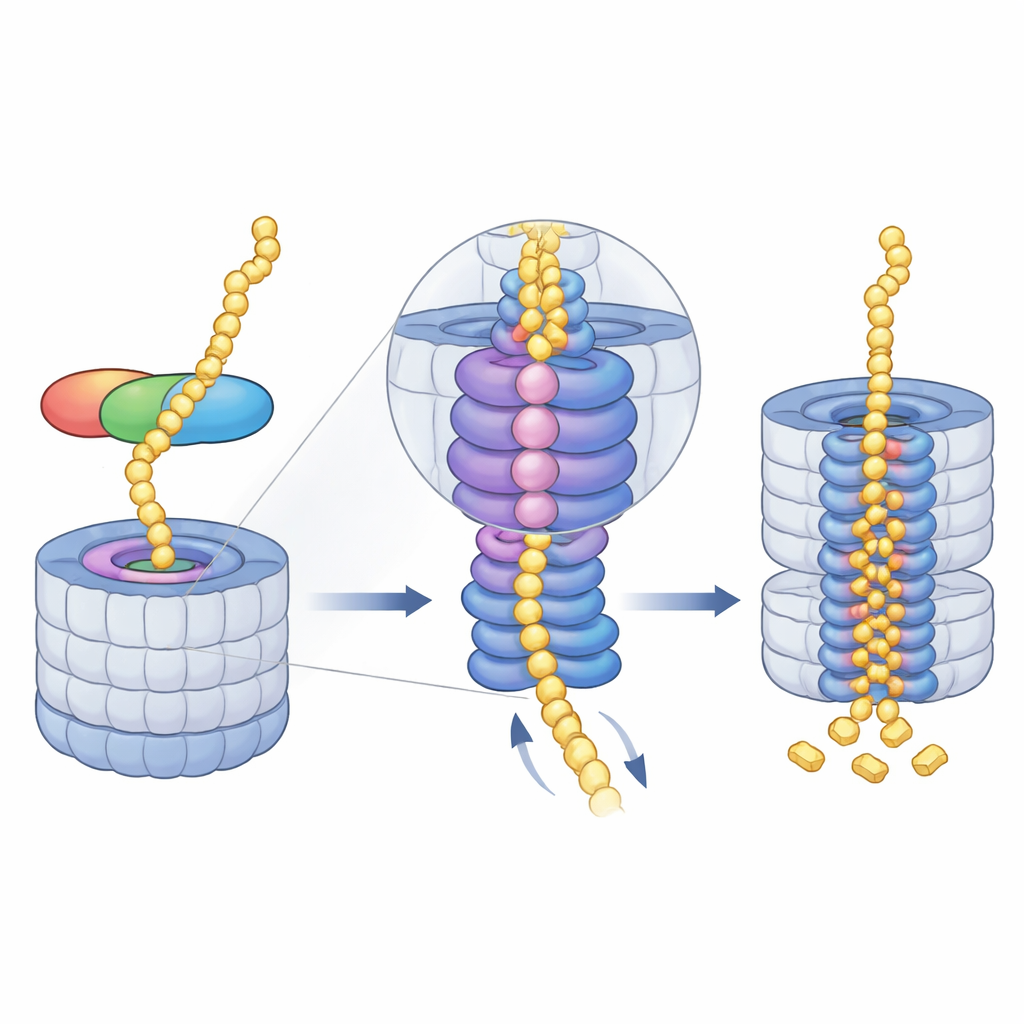
将蛋白引导入研磨核心
一旦midnolin完成对接,蛋白酶体耗能的马达——AAA+ ATP酶环接管任务。该环位于入口孔下方,通过一步步拉动未折叠的蛋白链进入核心。冷冻电镜快照显示了马达六个亚基采用的一系列“螺旋楼梯”式位置,它们在中央通道中抓住并交接底物。作者捕捉到了该循环的四个连续阶段,均显示midnolin结合的物质穿过孔道,甚至观察到一个亚基中镁离子的释放与整个环的向下位移同时发生。这提示协调的ATP利用与镁离子释放有助于把蛋白更深地棘轮式推进到含有切割位点的腔室中。
为何定位与共表达至关重要
团队测试了每个midnolin模块对效率的贡献。单独的锚定螺旋可以结合RPN1,但不能显著提升蛋白酶体活性。移除Catch结构域会导致许多蛋白酶体停留在无底物的空闲状态,即便midnolin仍能附着;将Catch替换为永久融合的底物也无法恢复完全活性。这些发现表明Catch不仅仅是抓取靶标——它还必须将蛋白精确定位在孔口入口处。生化实验和肿瘤转录组数据进一步显示,midnolin往往与其底物共表达。共表达时,midnolin折叠更好并形成稳定复合体,创造了一个现成的“降解我”包裹,可在细胞需要重置基因表达时迅速递送到蛋白酶体。
自我清理与未来的医学可能性
在靶蛋白被拉入并切碎之后,midnolin本身也未被豁免。它自身的无结构区可以被穿入马达并送入相同的破坏腔室,确保该辅助因子不会不必要地积累。通过阐明这一路径——无需泛素便可通向蛋白酶体——这项研究扩展了我们对细胞在极短时间内管理蛋白半衰期的理解。它还暗示了新的治疗策略:通过设计基于midnolin的分子,将致病的核内蛋白直接系到蛋白酶体,研究人员或许有朝一日能够更快速、更选择性地消除某些“不可成药”的靶点,包括某些癌症驱动因子。
引用: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
关键词: 蛋白酶体, midnolin, 蛋白降解, 泛素非依赖途径, 即刻早期基因