Clear Sky Science · zh
ANXA1-FPRs 信号介导的 MDSCs 空间异质性驱动口腔鳞状细胞癌进展中的免疫抑制
为何机体防御在某些口腔癌面前束手无策
口腔鳞状细胞癌是常见的口腔癌类型,常常对当下最令人振奋的癌症疗法——激发机体自身免疫的免疫疗法——表现出耐受性。本文提出了一个基础但关键的问题:原本应识别并清除癌细胞的强大免疫细胞,为何在这些肿瘤中屡屡失效?通过绘制不同细胞在肿瘤内的空间分布并解析它们之间的相互通信,研究者揭示出癌细胞、免疫抑制细胞与杀伤性 T 细胞之间随时间演变的“猫捉老鼠”式博弈,这有助于解释治疗失败的原因——并指示出可能的修正路径。 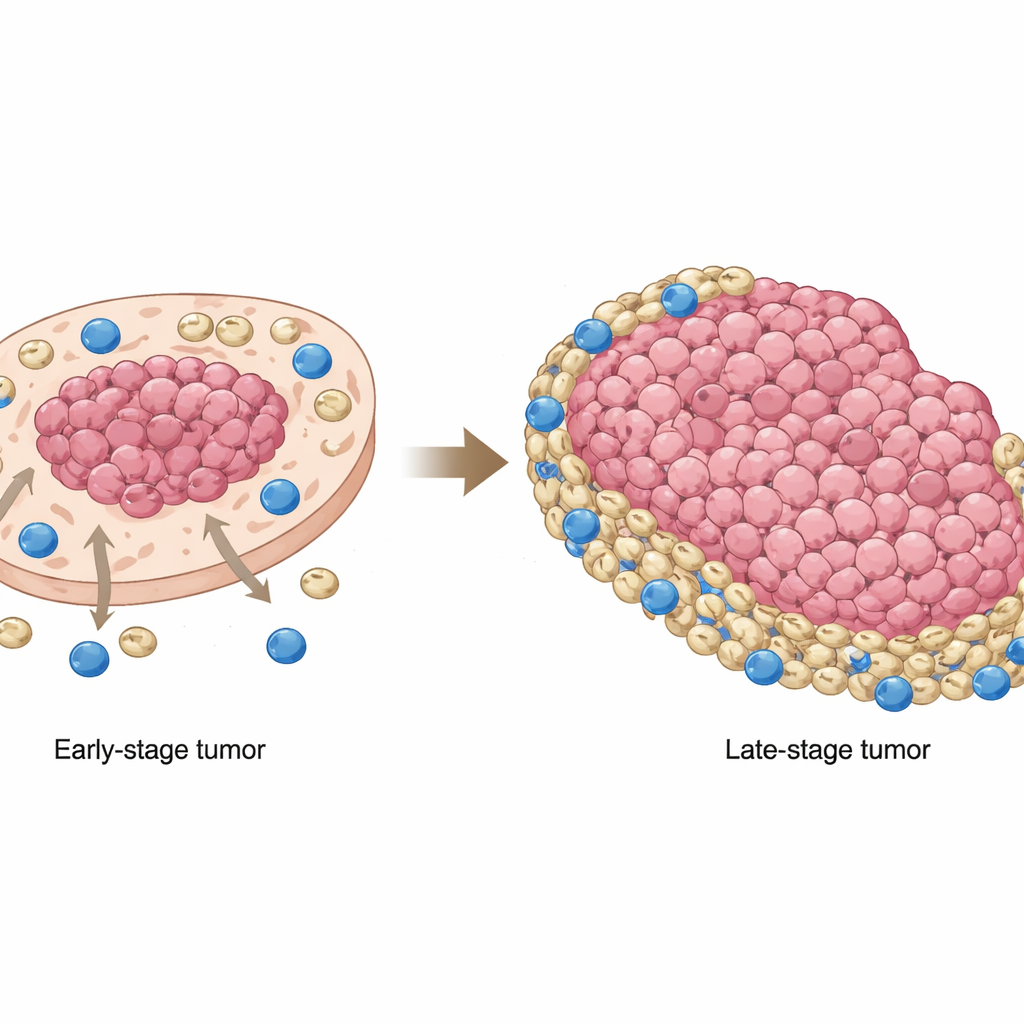
肿瘤内部的隐秘地形
作者将两种前沿方法结合:单细胞 RNA 测序,用以读取单个细胞的活性状况;以及空间转录组学,显示这些细胞在实际肿瘤组织切片中的位点。对早期与晚期口腔癌患者的肿瘤进行分析后,他们鉴定出主要细胞角色:癌性上皮细胞、CD8 “杀手” T 细胞、其他 T 与 B 细胞、构成结构支撑的成纤维细胞,以及一种名为髓源性抑制细胞(MDSCs)的特殊免疫细胞。早期肿瘤中活跃的 CD8 T 细胞更多,而晚期肿瘤则显示出较弱的 T 细胞信号和来自髓系细胞增强的免疫抑制信号,指向一个随时间推移对抗癌免疫愈发不利的环境。
抑制细胞的迁移
最引人注目的发现之一是随着肿瘤进展,MDSCs 的位置发生了变化。在早期癌症中,这些抑制细胞倾向于聚集在肿瘤细胞丰富的区域,靠近癌灶核心。到晚期,它们向外移动,积聚在肿瘤贫乏区和边缘,而这些区域 CD8 T 细胞更为常见。这意味着在晚期肿瘤中,杀手 T 细胞大多被推到边缘,随后遇到一圈 MDSCs,后者削弱了它们攻击癌细胞的能力。患者样本与小鼠模型证实,这种再分布并非偶发现象:当 MDSCs 与癌细胞的重叠减少、而在非肿瘤区域聚集时,患者的总体生存率更差。 
癌细胞与抑制细胞之间的信号开关
研究聚焦于癌细胞与 MDSCs 之间的一段分子“对话”,牵涉到肿瘤细胞表面的蛋白 annexin A1(ANXA1)与髓系细胞上的一类受体 FPRs。在疾病早期,癌细胞表面的 ANXA1 强烈作用于 FPR1 和 FPR3,尤其是位于 MDSCs 与肿瘤相关巨噬细胞上的那些受体,帮助招募并维持这些抑制细胞在肿瘤核心。一旦癌症进展,肿瘤细胞的 ANXA1 水平下降,削弱了这些原有的联结。与此同时,越来越多的 MDSCs 开始表达另一种受体 FPR2,ANXA1–FPR2 信号作为一种代偿性通路出现以继续维系 MDSCs。具有高 ANXA1 的一小部分肿瘤细胞并显示类干性特征,似乎像“诱饵”一样在早期吸引 MDSCs;当 ANXA1 下降后,MDSCs 不再被锚定在核心,反而转向富含 CD8 T 细胞的区域。
关闭护盾以助力免疫疗法
为检验阻断这段通信是否能改善治疗,研究者在口腔癌小鼠模型中用一种名为 WRW4 的小分子抑制剂阻断了 FPR2。单独抑制 FPR2 可减少肿瘤微环境中 MDSCs 的存在并增加 CD8 T 细胞,但并不足以显著放慢肿瘤生长。同样,单用抗 PD-1 免疫检查点抗体也仅带来温和益处,因为 MDSCs 仍然形成抑制性屏障。然而,当两种药物联合使用时,肿瘤生长被显著抑制,小鼠存活期延长。在这些动物体内,MDSCs 浸润显著下降,而 CD8 T 细胞更深入地侵入肿瘤细胞丰富的区域,这表明阻断 FPR2 可移除通常保护癌细胞免受免疫攻击的一道关键屏障。
这对未来癌症治疗的意义
总体而言,这项工作表明,决定免疫疗法在口腔癌中能否成功的,不仅是细胞的类型,还包括它们的空间排列与信号联盟。随着肿瘤进展,MDSCs 从中心迁移到边缘,在那里它们拦截杀手 T 细胞,而 ANXA1–FPR2 信号有助于维持这种抑制性布局。通过破坏这一路径——尤其是与现有检查点抑制剂联合使用——临床上可能重塑肿瘤微环境,使机体的免疫细胞能够重新识别并摧毁癌细胞。这提示了一个具体策略:将 FPR2 阻断剂与免疫疗法配合使用,可能改善那些目前对最佳可用治疗耐受的口腔癌患者的结局。
引用: Li, F., Han, Y., Ou, F. et al. Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression. Nat Commun 17, 2535 (2026). https://doi.org/10.1038/s41467-026-70861-x
关键词: 口腔鳞状细胞癌, 肿瘤微环境, 髓源性抑制细胞, 空间转录组学, 癌症免疫治疗