Clear Sky Science · zh
合成适配体机械受体通过DNA电路实现细胞特异性力传感与时间控制
通过轻微牵拉倾听细胞
我们的身体充满了不断对周围环境施加推拉力的细胞,这些微小的力决定了细胞何时生长、移动或分化。该研究描述了一种新方法,利用可调节到特定细胞类型并可随时间开启或关闭的DNA器件来窃听这些力。这样的技术未来可帮助工程师引导组织生长、理解肿瘤行为,或设计能实时响应活细胞的智能材料。
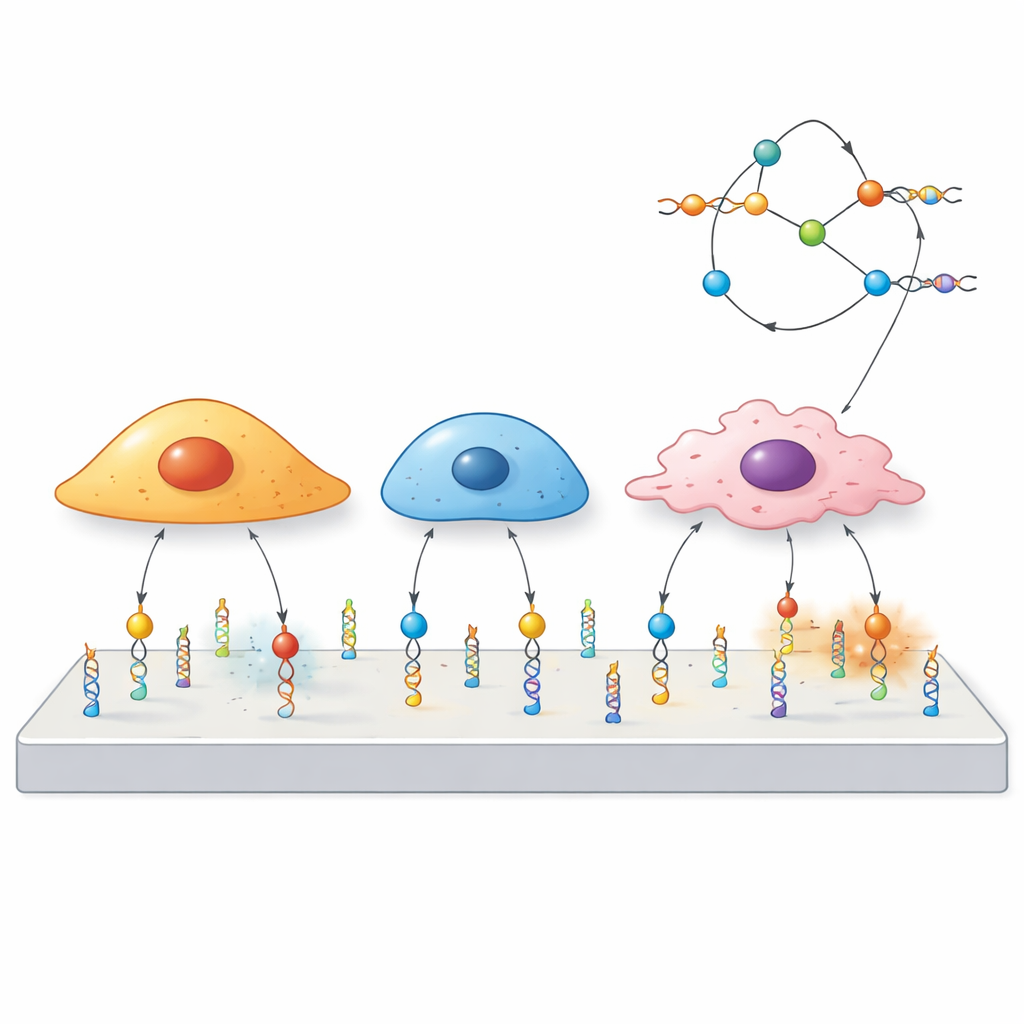
将DNA作为微小的机械开关
研究人员用DNA构建了“机械探针”,DNA本身即携带遗传信息的分子。每个探针由三部分组成:一个称为适配体的短DNA序列,可粘附在选定的细胞表面蛋白上;一段配对的DNA片段,像弹簧一样设定在特定力下断开;以及一个在该弹簧断裂时发光的荧光染料。当细胞对适配体结合的受体施加足够大的拉力时,DNA双链打开,信号被触发。由于不同适配体能结合不同受体,团队可以预先决定哪些细胞或蛋白能激活探针。
在细胞表面发现隐蔽的力传递通路
大多数现有的力传感器集中在整合素上——这种帮助细胞抓住基质的知名蛋白存在于多种细胞类型中,限制了选择性。在这里,团队将目标转向那些通常不被视为机械受体的“非常规”受体。他们展示了名为AS1411的适配体(可结合肿瘤细胞常见的核蛋白nucleolin)仅在能够特异识别其靶点时才产生信号。通过设计需要较弱或较强力才能打开的探针,他们发现nucleolin传递的力相比整合素较为温和,且本身并不帮助细胞在表面展开。相比之下,另一种识别受体PTK7的适配体Sgc8即便在细胞仅略微粘附时也能报告力,形成环状图案,提示了不同的运动来源。
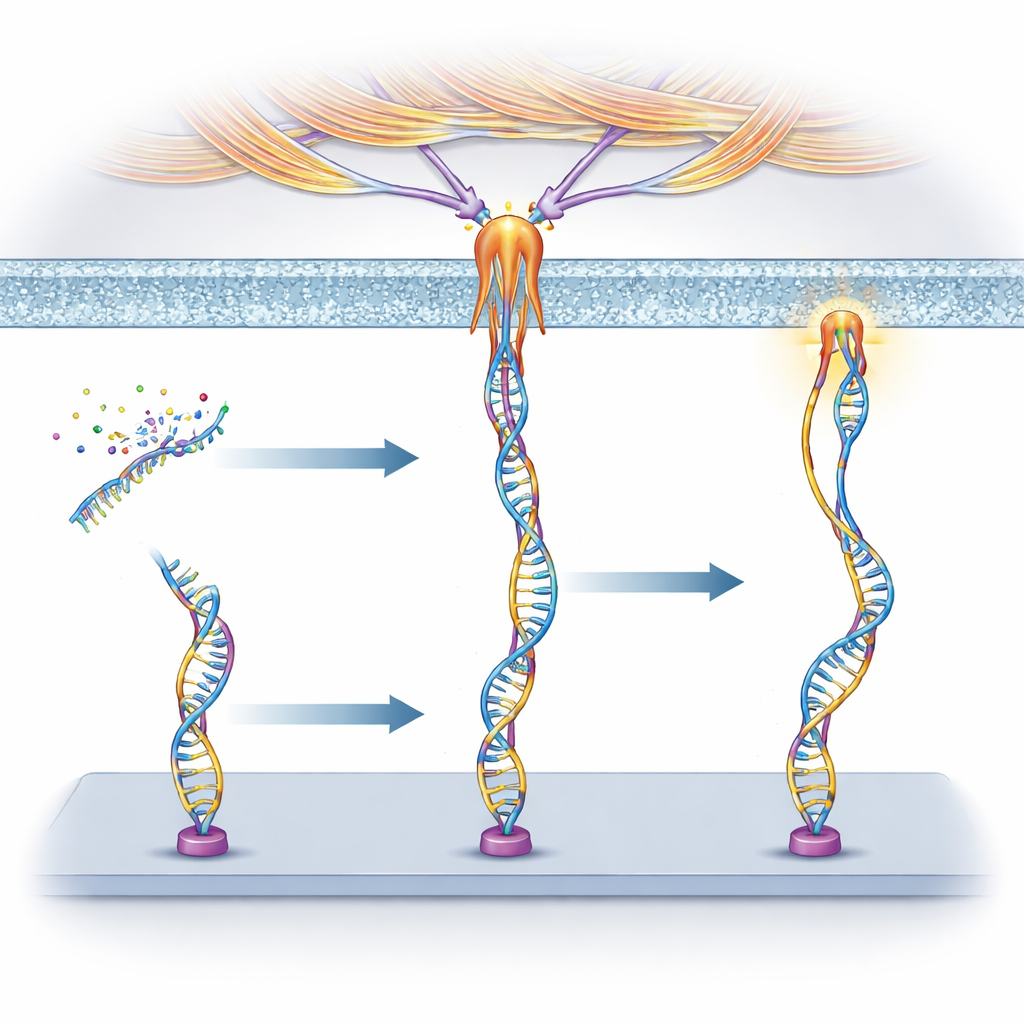
追踪力的来源
为了解是什么在拉动这些DNA器件,研究人员使用了可选择性阻断不同细胞过程的药物。对于nucleolin,他们发现其所承受的力高度依赖于肌球蛋白——即帮助肌肉收缩的那种马达蛋白——并出现在细胞形成粘着斑的位置——这些是用于抓握和感知刚度的特殊接触点。这表明nucleolin间接与细胞内部的肌动蛋白-肌球蛋白机器相连,并能分享其收缩力。而对于PTK7,阻断一种称为巨胞吞(macropinocytosis)的过程——细胞使膜起皱并吞入液体——则显著减少了信号。产生的力主要来自由肌动蛋白驱动的早期膜皱褶,而非随后囊泡封闭的步骤,揭示了不同的机械通路。
以分子精度调节细胞选择性
由于每个适配体识别特定的表面受体,相同的DNA支架只需替换适配体即可重新编程。团队用针对三种不同靶点(PTK7、黏蛋白1(mucin-1)和EpCAM)的探针进行了演示,横向测试了一组在这些蛋白上高表达或低表达的癌细胞系。富含某一受体的细胞会产生强信号,而受体含量少的细胞几乎不响应,即便它们混合在同一培养皿中。值得注意的是,即使是共享相同受体的细胞也可能显示不同的力空间分布,强调了力通过受体传输不仅取决于受体的存在,还取决于每种细胞类型的内部连线。
编程控制细胞何时被允许牵拉
利用适配体由DNA构成的特性,研究人员将探针连接到控制适配体是否能结合的DNA反应网络。互补的“阻断”链可以暂时掩盖适配体,而“激活”链随后通过链置换反应移除阻断链,恢复力敏感性。他们还设计了一种可被酶RNase H切割的RNA阻断链,并通过与酶竞争的诱饵分子进一步减缓该切割。通过这种方式,他们将机械感测转变为一个定时程序:细胞只有在内置延迟之后或在选定的时间窗口内才能产生信号。
这对未来活体材料的意义
通俗地说,这项工作把DNA变成了一个智能机械锁——仅对特定细胞、在特定力下并在特定时间开启。通过揭示诸如nucleolin和PTK7等不那么显眼的受体也能通过细胞内部截然不同的途径传递机械信息,它拓宽了我们对细胞如何“感知”环境的认识。由于整个系统由核酸构建,它可以直接接入迅速扩展的DNA电路和纳米装置工具箱。这为构建不仅能感测细胞何时施力或拉动、还能以精确编程的时序做出生化响应的材料和工程化组织奠定了基础,可能用于引导修复、成长或癌症治疗。
引用: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
关键词: 力转导, DNA适配体, 细胞力学, 合成生物学, DNA反应网络