Clear Sky Science · zh
Frazzled/DCC 指导空间性祖细胞整合以确保稳态肠道更新
肠道如何悄然自我更新
每天,覆盖在我们肠道表面的细胞都在磨损并需要被替换,但整个器官却以惊人的精确度维持其形状和体积。利用果蝇作为模型,这项研究揭示了一种隐藏的引导系统,它告诉新生肠细胞准确地移动到何处以填补上内壁的微小空隙。理解这种“细胞交通管制”不仅澄清了健康器官如何自我维护,也有助于说明类似的引导信号在癌症扩散过程中如何可能被劫持。
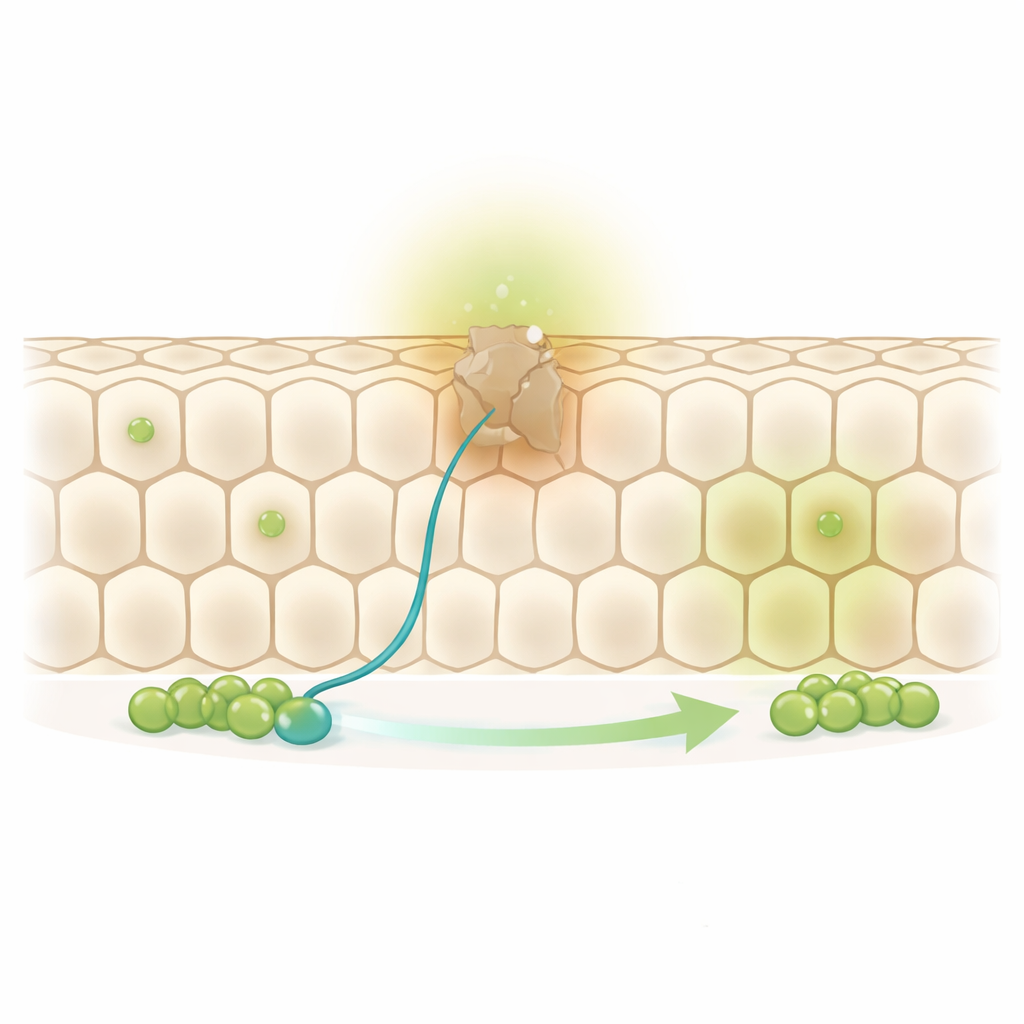
如蜂巢般持续运动的结构
果蝇中肠由一层排列如蜂巢的大型吸收细胞覆盖。在这层细胞片的基底,散布着干细胞及其直接的子代——称为祖细胞。当一个老的吸收细胞走到寿命尽头时,干细胞分裂,其祖细胞最终替代那邻近的衰老细胞。然而,作者注意到大约三分之一的蜂巢细胞并没有与之直接相邻的干细胞或祖细胞。这提出了一个难题:这些“触及不到”的细胞是如何在不留下屏障空洞的情况下被更新的?
新细胞在移动
通过在一周内追踪单个替换事件,研究者发现这些远端细胞和紧邻干细胞的细胞一样经常被更新。这意味着祖细胞必须移动。确实,团队观察到祖细胞会伸展出长而细的突出物——类似细胞的触手——其频率和长度都超过干细胞本身。这些突出物并非随机:在正常情况下,它们主要指向那些更老、尚未被替换的邻居,而不是刚更新过的细胞,暗示了一种主动的搜索与救援行为,目标是那些最需要被替换的细胞。
神经引导信号被重新用于肠道
为了解这些突出物如何被定向,作者转向了一类在大脑布线中最为人所知的分子:网蛋白及其受体 Frazzled/DCC 和 Unc-5。在神经系统中,网蛋白像远程灯塔一样吸引或排斥生长的神经纤维。在果蝇肠道中,团队显示 Frazzled/DCC 和 Unc-5 受体特异性地存在于祖细胞上,并在其突出物中富集。衰老的吸收细胞则开始产生并释放一种称为 Netrin-B 的网蛋白。当研究者在特定细胞中增加 Netrin-B 时,邻近祖细胞伸出更长的突出物并朝向该信号源定向,随后迁移过去占据该位置。相反,阻断 Netrin-B 或使 Frazzled 失活会导致突出物缩短、远端细胞不再被高效替换,而且果蝇寿命缩短,凸显出该引导对肠道健康的重要性。
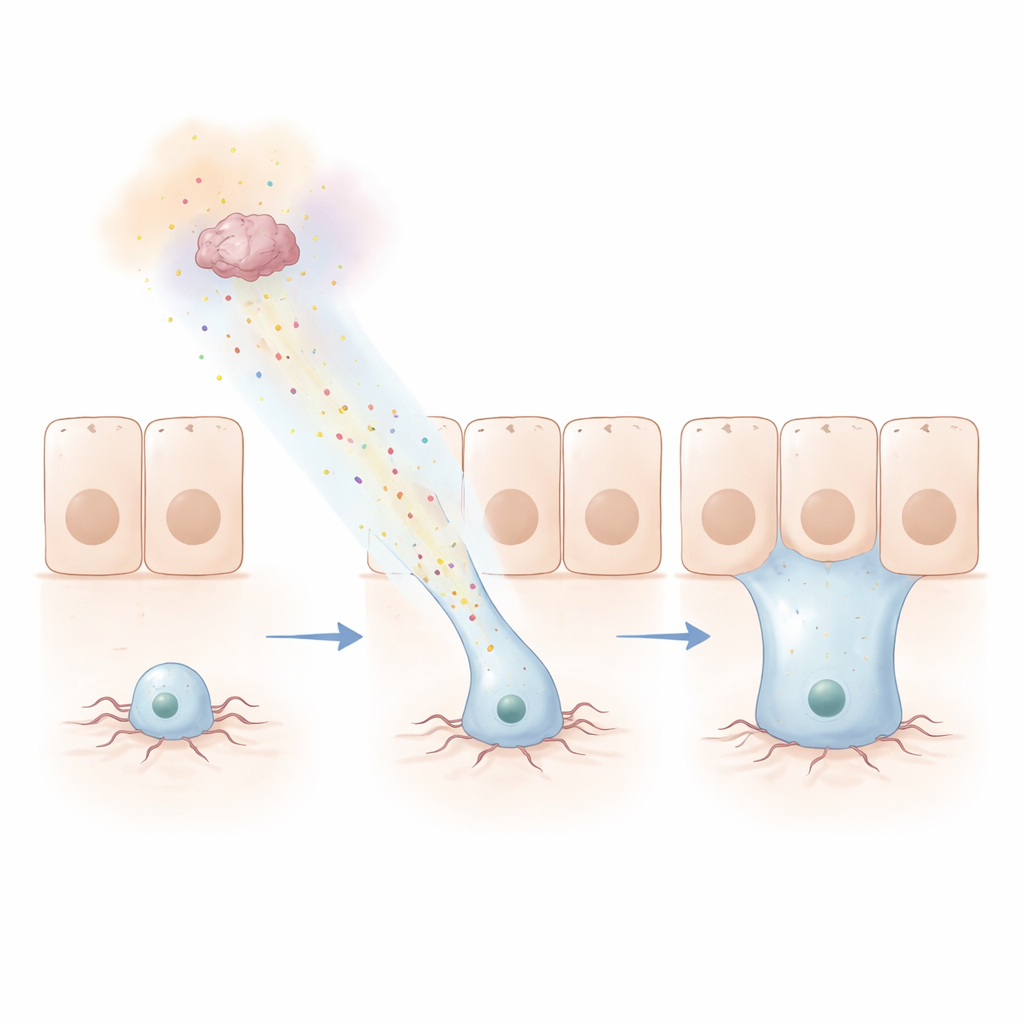
沿化学痕迹追踪
为了探查该信号的作用距离,团队设计了一个巧妙的“哈梅林”测定(以吹笛人命名)。他们在肠区交界处形成一环状细胞群分泌网蛋白,同时对远处的祖细胞进行荧光标记。数日内,祖细胞朝信号源迁移了数十微米,甚至跨越了一个清晰的边界进入不同的组织层并在那里整合。人类版的网蛋白和 DCC 受体可以替代果蝇对应物并仍然引导这些移动,表明该机制高度保守。推动细胞运动的同一套肌动蛋白机制也是必需的:当关键成分被去除时,突出物和远程更新均失败。
这对健康与疾病意味着什么
简而言之,这项工作表明肠道并不只依靠局部细胞增殖的压力来更新内壁。相反,垂死的细胞会发出一种化学“求助”信号 Netrin-B,吸引带有 Frazzled/DCC 受体的特定祖细胞。这些祖细胞沿着梯度伸出触手,朝老化细胞爬行,并嵌入到位以维持屏障完整。由于相同的 Netrin–DCC 系统在哺乳动物中也很活跃,且与癌细胞侵袭和转移有关,果蝇的发现为将这些分子视为双刃剑提供了具体的机制性支持:它们对健康组织的有序修复至关重要,但在肿瘤误调控时也可能变得危险,使肿瘤细胞学会移动并在新器官定植。}
引用: Zipper, L., Ramon-Cañellas, P., Akkas-Gazzoni, F. et al. Frazzled/DCC directs spatial progenitor integration ensuring steady-state intestinal turnover. Nat Commun 17, 2491 (2026). https://doi.org/10.1038/s41467-026-70704-9
关键词: 肠道干细胞, 细胞迁移, 网蛋白信号, 组织稳态, 癌症转移