Clear Sky Science · zh
血管侵犯相关的基因表达可在 I 期肺腺癌术前活检中检测到
这对早期肺癌患者意味着什么
如今许多人被诊断出可通过手术切除的小型肺肿瘤。但其中一些早期癌症会在体内悄然扩散并复发,而另一些则不会。医生知道一个危险信号是癌细胞侵入邻近血管,这种变化称为血管侵犯,但在术前或术中通过显微镜看到它非常困难。本研究表明,肺肿瘤的微小样本中已携带能揭示癌症是否很可能侵入血管并更易复发的基因活动模式,这为更个体化的手术与随访提供了可能。
早期肺肿瘤中隐匿的高风险亚群
研究人员聚焦于 I 期肺腺癌,这是一种常见的肺癌亚型,常在体积较小且表面上被限制在肺内时被发现。在这类患者中,一大威胁是显微镜下的血管侵犯:肿瘤细胞群侵入小静脉或小动脉,为远处器官提供了直接通路。现有的分级系统并不能完全捕捉到这一风险,而且病理学家在常规切片或术前获取的细针活检样本中很容易漏诊这些微小灶。因此,一些本可从更广泛手术或辅助药物治疗中获益的患者未能及时被识别。该团队试图寻找一种可在非常少量组织中可靠检测到的血管侵犯分子指纹。
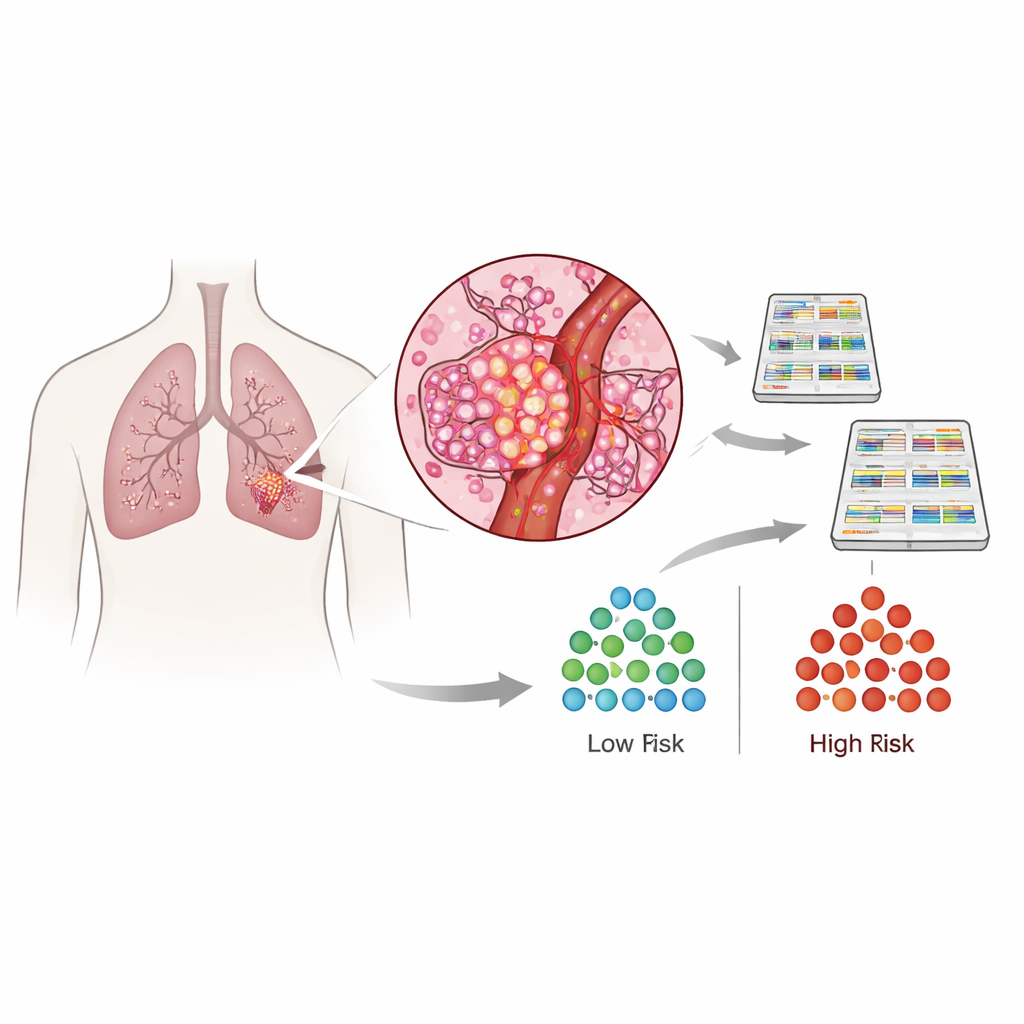
从肿瘤基因活动解读血管侵犯
研究者对 162 例术后切除的肿瘤进行了 RNA 测序,测量每个癌组织中哪些基因被激活或抑制。他们鉴定出 474 个在有血管侵犯的肿瘤与较为良性生长模式的肿瘤之间差异明显的基因。这些基因分为四个簇。三个簇在侵入血管的肿瘤中更为活跃,且与细胞快速分裂、细胞松解并穿行组织的能力、新血管形成以及对缺氧环境的适应相关。剩下的一个簇在这些侵袭性肿瘤中活性较低,与细胞粘附、增殖控制和免疫监视有关——这些特征通常有助于抑制癌症。这表明血管侵犯不仅仅是一个局部的微小事件,而是反映了肿瘤整体生物学的广泛转变。
在肿瘤全景中绘制风险信号分布
为了查看这些基因模式在肿瘤内部的位置,团队使用了空间转录组学,这项技术在保留组织显微图像的同时记录组织切片上成千上万个微小点的基因活性。他们分析了 15 例肺癌(包括有无血管侵犯的样本),并将基因活动图与详细的病理学注释叠加。高风险基因簇不仅在癌细胞占满血管的部位强烈表达,还在邻近的高等级肿瘤区域和围绕侵袭巢形成的致密瘢痕样组织(称为基质增生性间质)中高度表达。与之相对的低侵袭性簇则在更有序的肿瘤结构和外观正常的肺组织中富集。这证实了血管侵犯特征延伸远超过被侵占的血管本身,且由癌细胞与周围支持细胞共同塑造,尤其是那些重塑组织的特化成纤维细胞。
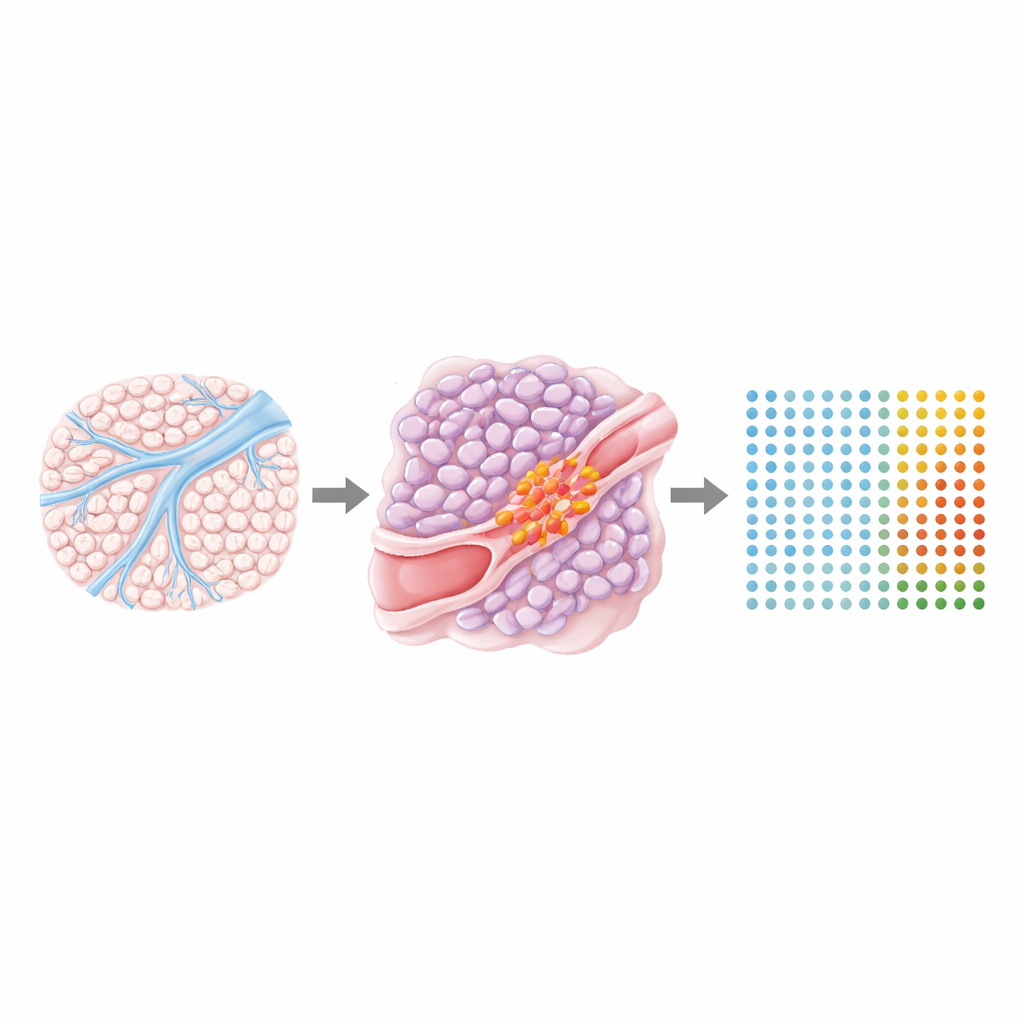
为临床医生构建实用的预测工具
从较大的基因集合中,研究者提炼出一组 48 基因的预测器,并训练了机器学习模型以区分有血管侵犯与无血管侵犯的肿瘤。在原始患者队列和独立验证集中,该预测器均以高准确度正确区分了两类肿瘤,并且与术后癌症复发的可能性相关。值得注意的是,该预测器并非简单反映现有的显微镜分级特征,与淋巴管入侵相关的改变重叠较少,强调了血管侵犯是一个独立的过程。通过检查同一肿瘤内的多个区域,团队发现预测器评分在已知的肿瘤异质性情况下仍相当稳定,这表明单次小样本即可提供有用信息。
从针吸活检到个体化手术
最具临床意义的测试是这种基因评分能否从常规术前活检中读取,而活检通常只取到肿瘤的一小片并且很少直接见到被侵入的血管。在 24 例患者的初步队列中,活检组织中的预测器评分与随后手术标本的评分高度一致,并且准确预测了切除时哪些肿瘤会显示血管侵犯。在考虑到 I 期疾病中血管侵犯的常见率后,活检中低预测器评分对应肿瘤确实缺乏血管侵犯的概率很高。这意味着,经过进一步验证后,此类检测可帮助识别适合进行保留更多肺组织的较小手术的患者,同时提示那些可能需要更广泛手术或附加治疗的患者,使肺癌治疗更接近真正的精准外科。
引用: Steiner, D., Sultan, L., Sullivan, T. et al. Vascular invasion-associated gene expression is detectable in pre-surgical biopsies of stage I lung adenocarcinoma. Nat Commun 17, 2581 (2026). https://doi.org/10.1038/s41467-026-70600-2
关键词: 肺腺癌, 血管侵犯, 基因表达特征, 空间转录组学, 基于活检的风险预测