Clear Sky Science · zh
使用以国际单位制为锚定校准物实现绝对转录组学的计量学基础
为何将 RNA 信号转换为真实数字至关重要
现代基因检测可以读出细胞中哪些基因被开启或关闭,但它们在一个基本问题上踟蹰:到底有多少分子存在?当今的 RNA 测序技术主要比较样本间的相对变化,而不能给出可靠的、硬性的计数。如果你要设定通用的疾病阈值、在医院间比较结果,或构建精确的细胞工作模型,这就是个问题。这项研究提出了一种新的方法,将 RNA 测序锚定到化学与物理中使用的相同国际单位,从而把模糊的相对信号转化为绝对且可比的数字。
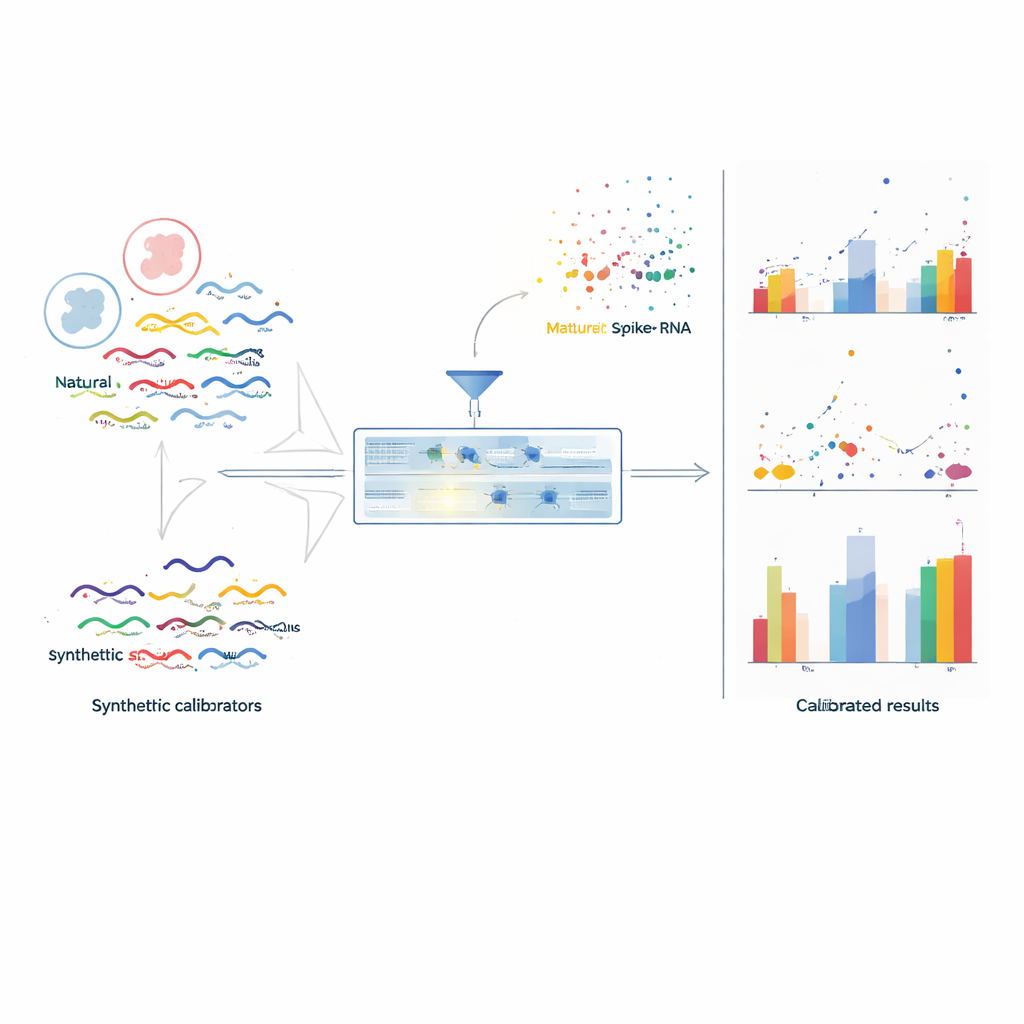
比较基因活性时的问题
RNA 测序通过将 RNA 分子切成片段并计数每个基因被代表的次数来工作。但有两类扭曲会出现。首先,实验之间的系统性差异——例如不同的实验室、仪器或样本制备方法——会产生“批次效应”,使得相同样本在重复测定时看起来不同。其次,序列依赖效应——具有某些长度或碱基组成的基因更容易或更难被捕获——意味着即便在同一样本内,也会有些基因被持续高估而有些被低估。因此,科学家在很大程度上被迫讨论条件之间的倍数变化而非真实的分子计数,而这些倍数变化本身在不同批次间也可能具有误导性。
用于 RNA 测量的一组新尺度
为了解决这个问题,作者创建了 TranScale——一套由 100 种合成 RNA 分子组成的面板,设计上既能像真实的人类转录本那样表现,又在序列上可计算地区分开来。这些标准覆盖了广泛的长度、序列特征以及临床相关变体(如剪接形式和基因融合),紧密反映了真实细胞 RNA 的多样性。关键在于,每种 TranScale 分子都使用一种称为同位素稀释质谱的主要测量技术被赋予了精确浓度,并且该测量可追溯到国际单位制(SI)。通过在测序前在每个 RNA 样本中混入已知微量的 TranScale,实验获得了一个内部尺子,该尺子会经历与天然 RNA 相同的实验步骤和扭曲。
将有噪声的测序读数转换为绝对计数
在每个文库中加入 TranScale 后,团队可以将每个外加分子(spike-in)的测序读数与其认证浓度进行比较。对于每个批次,他们挑选表现良好的外加分子并拟合一条直线校准曲线,将基于读数的单位与真实分子计数联系起来。这个简单模型同时捕捉了批次层面的偏差和与序列相关的偏差。随后将同一条曲线应用于样本中的所有基因,将它们的相对读数转换为每单位 RNA 的绝对拷贝数。在一项故意设计以产生强烈批次效应的大型多实验室、多平台研究中,这一校准将各中心间绝对测量的中位变异从超过 85% 降到 15–25% 以下,并恢复了被技术噪声掩盖的生物样本的正确聚类。
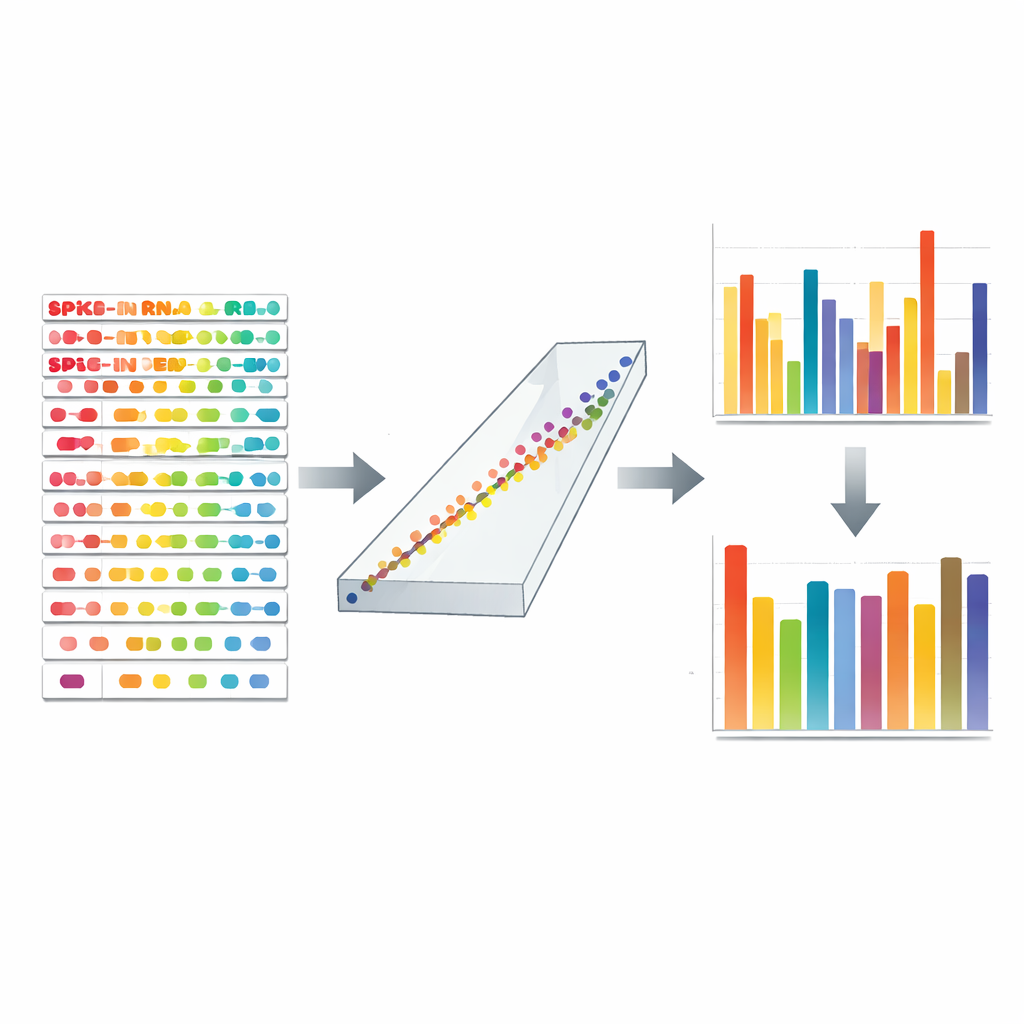
发现隐藏的错误并予以修正
TranScale 标准也可作为数据质量的诊断探针。通过将测得值与其认证真值比较,作者区分了两种误差:每个基因的绝对水平有多偏离,以及条件间比值有多偏离。他们发现了令人惊讶的例子:相对差异看起来一致但绝对数字严重失真,反之亦然。这意味着传统只关注倍数变化的检查可能会错过严重问题。经过校准后,外加分子和数千个真实人类基因的绝对水平与比值都与独立的数字 PCR 测量以及外部参考数据集高度一致。修正后的数据呈现出更清晰的定量格局,使得在相同绝对尺度上比较 housekeeping 基因与癌症驱动基因成为可能,并能将诸如共同扩增的癌基因这类 DNA 变化直接与其 RNA 输出连接起来。
从相对趋势走向临床阈值
最后,研究人员展示了绝对标定如何增强医疗决策的准确性。以乳腺癌中常测的一个癌基因为例,他们基于数字 PCR 定义了一个固定的截止值,并检验 RNA 测序能否在多个批次中可靠地将样本判定为正常或肿瘤。未经校正的数据由于批次效应给出了不一致的答案,而在 TranScale 校准后每个文库均与真实分类一致。通过通过仿生标准将 RNA 测序与 SI 单位相连,这项工作为转录组学奠定了计量学基础。它为通用诊断阈值、中心间的稳健数据共享,以及更精确的系统级基因表达模型的建立打开了大门。
引用: Zhang, Y., Yang, B., Yu, Y. et al. A metrological foundation for absolute transcriptomics using International System of Units-anchored calibrators. Nat Commun 17, 2747 (2026). https://doi.org/10.1038/s41467-026-70582-1
关键词: RNA 测序, 绝对定量, 计量学, 基因表达校准, 生物分子标准