Clear Sky Science · zh
蛋白酶体核心颗粒分步装配中的结构转变
细胞如何清理分子垃圾
在我们每个细胞内,废弃和受损的蛋白质必须被分解,否则会像垃圾一样堆积。一个称为蛋白酶体的巨大神经分子机器承担着大部分清理工作,它也已成为抗癌药物的靶点。这项研究探查了酵母细胞中蛋白酶体催化核心如何逐步构建的幕后过程,揭示了出人意料的捷径和安全检查,帮助确保最终机器能精确工作并且仅在准备就绪时才激活。
构建一个蛋白切割的桶状结构
蛋白酶体的“业务端”是由叠放的蛋白亚基环组成的桶状核心。这个桶包含了隐蔽的切割位点,用来把其他蛋白切成小片。因为过早激活这些切割器很危险,细胞会以一系列部分组装的中间体来搭建这个桶。作者着重研究了早期形式的核心,称为前体复合体,这些通常稀少且短暂。通过略微减慢装配的最后一步之一,他们得以从酵母中捕获并纯化这些早期形态,并使用高分辨率冷冻电子显微镜对其成像——该方法将分子“冻结”在活动状态并展示其三维形状。
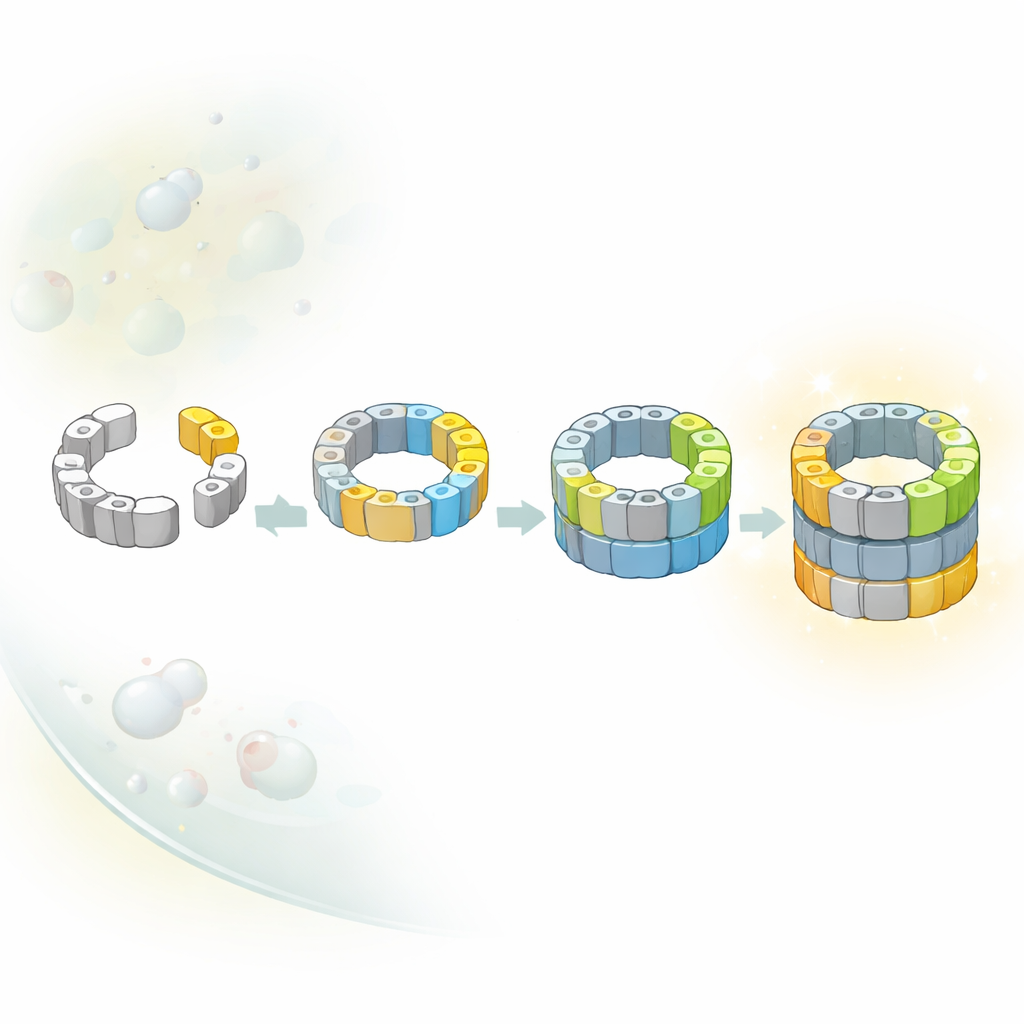
通向相同核心的多条路径
教科书式的经典图示常暗示细胞内复杂机器沿着单一固定路线构建。然而,研究人员发现蛋白酶体核心并非如此。他们鉴定出若干不同的中间体,这些中间体在半成品桶中加入了不同的催化亚基。通过将结构快照与开关单个亚基的遗传策略相结合,他们表明至少存在两条可选路径,从早期的半桶通向几乎完成的结构。在一条路径中,名为β5的特定亚基先到达;在另一条路径中,另一个亚基β1可以更早加入。这些路径之间的平衡很可能取决于细胞拥挤环境中哪些构件更为可用。
从松散部件到锁定的切割腔
这些结构还展示了随着装配进行,蛋白酶体的切割位点如何被谨慎地准备激活。在早期中间体中,包围埋藏切割残基的关键环区松散且无序,催化中心仍被短的“前肽”片段阻挡。随着更多亚基围绕环体依次就位,这些环逐渐采用更确定的构形,使得自我激活所需的关键氨基酸排成一条线。只有当两个半桶最终组合在一起,形成双环桶时,这些环才会完全锁定到其活性构象并触发阻挡片段的移除。这种几何与化学的耦合有助于确保强大的切割活性仅在封闭腔室内出现,从而保护细胞的其余部分。
伴侣蛋白引导然后放手
在此过程中,称为伴侣蛋白的专门辅助蛋白引导正在组装的桶并防止错误组合。一种伴侣蛋白Ump1起初大多无结构,但随着更多亚基将其包围,它逐步折叠,最终被困在中心腔内并在桶活化后被降解。另一对伴侣蛋白Pba1–Pba2以两种巧妙方式抓住外环表面。Pba1的一个柔性环像垫片一样楔入两个外环亚基之间,使它们略微分开,防止过早闭合。与此同时,一个外环亚基(α1)的末端帮助定位相邻片段,以便在最后阶段伴侣蛋白可以释放且环可以正确闭合。当研究者删除α1的末端时,桶停滞在一个后期、几乎完成但顽固地保持伴侣蛋白的状态,证实该小区域作为释放开关的一部分发挥作用。
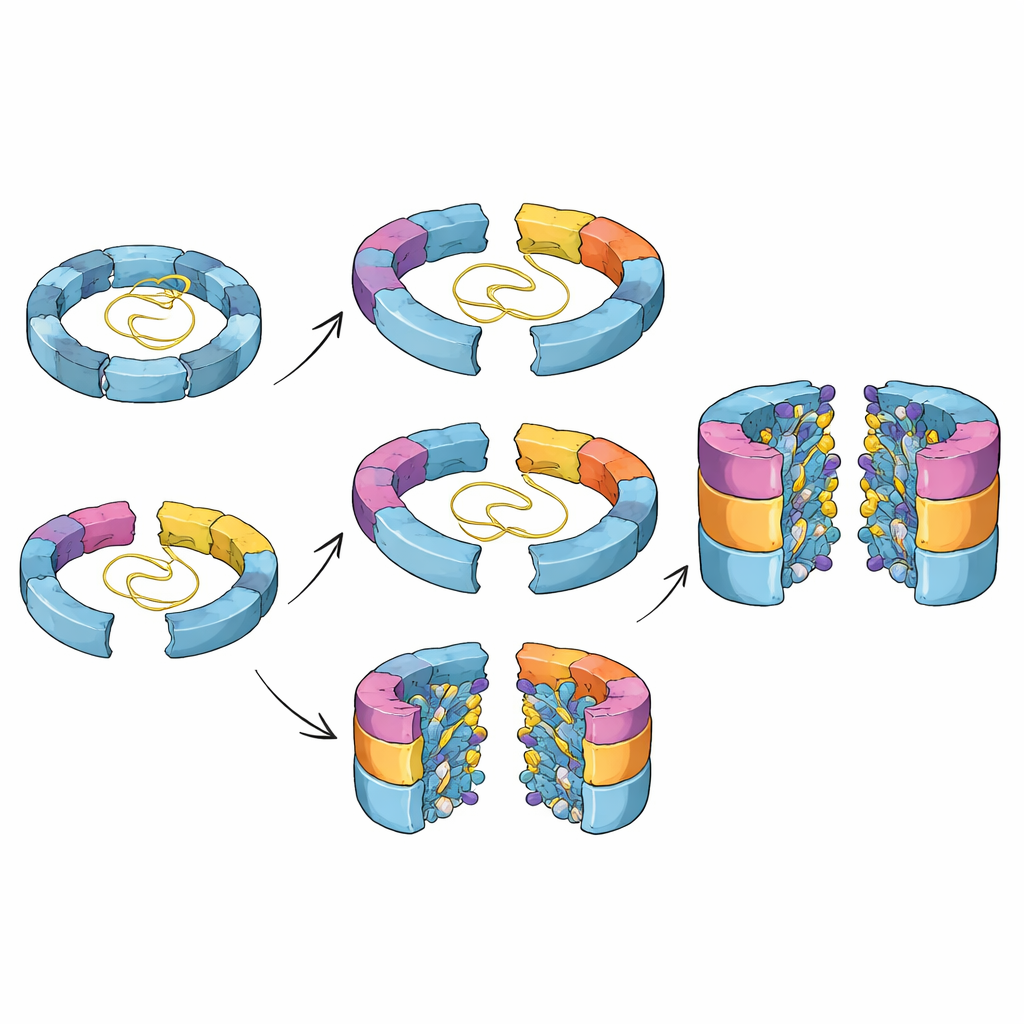
这些隐蔽步骤为何重要
综合来看,这些发现勾勒出细胞如何协调组装一个既危险又必需的蛋白切割器的详细图景。研究表明,蛋白酶体核心可以通过多条路线建成,其活性位点是逐步塑形就位的,伴侣蛋白不仅稳定早期中间体,而且被纳入一个计时回路,确保它们在恰当时刻离开。理解这些隐蔽步骤有助于解释装配因子中的微小遗传变化如何促成疾病,并可能有助于设计通过针对构建过程而非最终结构来微调蛋白酶体活性的药物,以用于癌症、免疫疾病或神经退行性疾病的治疗。
引用: Mark, E., Ramos, P.C., Nunes, M.M. et al. Structural transitions in the stepwise assembly of proteasome core particles. Nat Commun 17, 2582 (2026). https://doi.org/10.1038/s41467-026-70525-w
关键词: 蛋白酶体装配, 蛋白质降解, 分子伴侣, 冷冻电子显微镜, 细胞质量控制