Clear Sky Science · zh
一种致病Tau突变导致自噬-溶酶体功能障碍,限制Tau在额颞叶痴呆模型中的降解
当大脑的清理队伍跟不上时
为什么有些人在远未到老年时就出现毁灭性的记忆和行为问题?这项研究通过聚焦单一脑内蛋白Tau和那些通常负责控制它的小型细胞“回收中心”,来探讨这个问题。通过在超清显微镜下观察活体人类神经细胞,研究者展示了致病Tau突变如何堵塞细胞的废物处理系统,以及用小分子激活该系统如何有助于清除堆积。他们的发现可能为某些形式的痴呆症指明新的治疗策略。
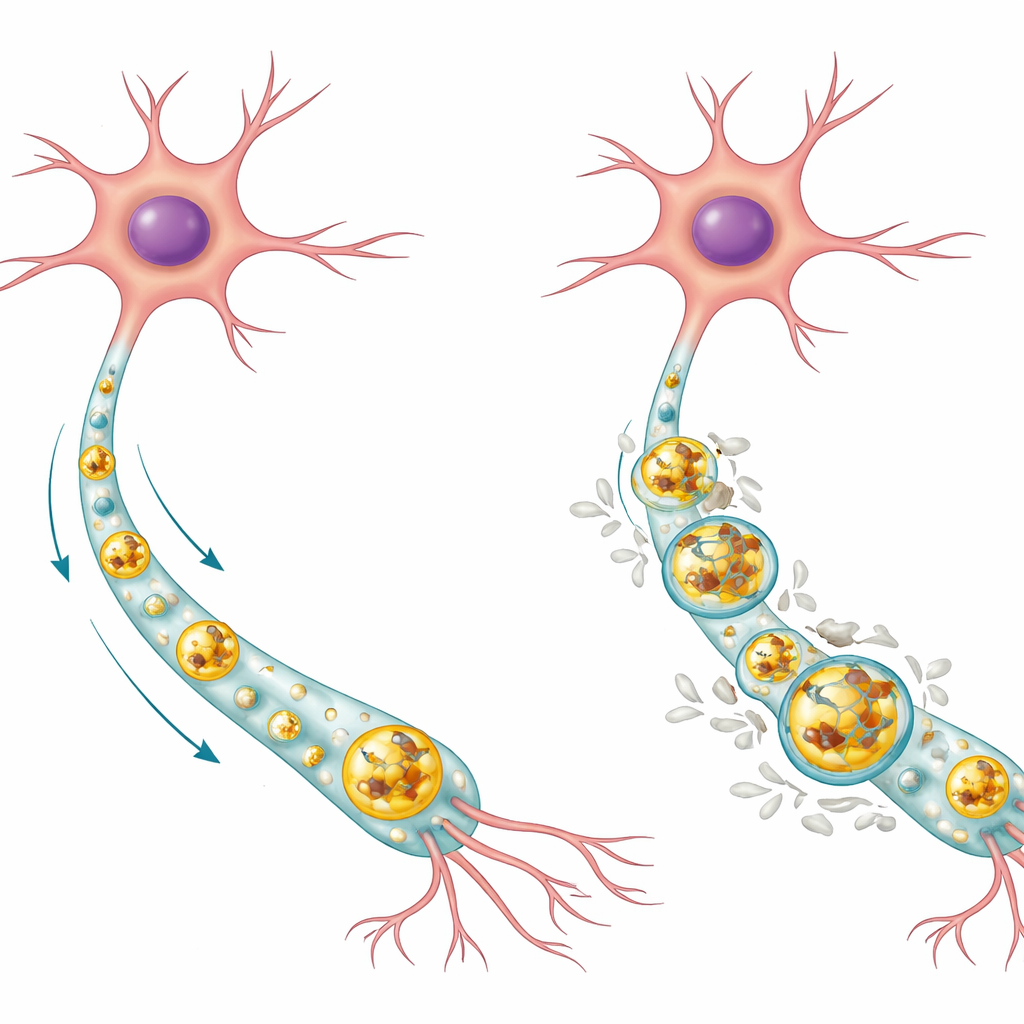
脑细胞通常如何清理垃圾
神经元是寿命很长的细胞,不能通过分裂来稀释损伤物质,因此高度依赖细胞内的清理系统。其中一个关键通路是自噬-溶酶体途径。在这个过程中,不需要的蛋白和老化的细胞器被包裹在称为自噬体的膜囊中,自噬体随后与充满酶的溶酶体融合,货物在其中被降解并回收。在健康的人类神经元中,作者发现正常的Tau蛋白倾向于在溶酶体的酸性核心内积累,在那里它可以被降解,而磷酸化的Tau(一种与疾病相关的化学修饰)更多地位于溶酶体的外膜上。健康细胞中大多数溶酶体完全不含Tau,这表明该系统通常能将Tau水平维持在较低且受控的状态。
遗传性痴呆中出了什么问题
研究团队聚焦于MAPT基因的一个突变,称为p.R406W,该突变会导致一种遗传性额颞叶痴呆,并能模拟类似阿尔茨海默病的记忆丧失。利用干细胞技术,他们将患者的皮肤细胞重编程为诱导多能干细胞,继而分化为大量携带该突变或经基因编辑恢复正常的人类神经元。在突变神经元中,总Tau和磷酸化Tau显著增高,这并非由于细胞产生更多Tau,而是因为它们清除得不够高效。超分辨率成像显示,突变细胞中几乎所有溶酶体都被Tau填满,尤其是磷酸化的Tau覆盖在溶酶体膜上。这种积聚表明细胞的主要蛋白质处置通路被堵塞了。
被堵塞的回收中心与迟缓的运输
更仔细观察回收机械,研究者发现突变神经元的溶酶体数量更多、体积更大,并且倾向于位于远离细胞体的位置。用荧光染料的活细胞成像显示,这些溶酶体移动更慢、在神经纤维上行驶的距离更短,尽管其所依赖的微管轨道看起来正常。突变神经元还含有更多自噬体、更多货物适配蛋白p62以及额外的脂滴——这些都是物质被标记为待处置但未被充分降解的迹象。使用pH敏感报告分子,他们发现突变细胞中的自噬体常常未能与溶酶体正确融合,导致“半成品”回收囊泡堆积以及广泛的清理缺陷,不仅影响Tau,也影响其他被运输的物质。
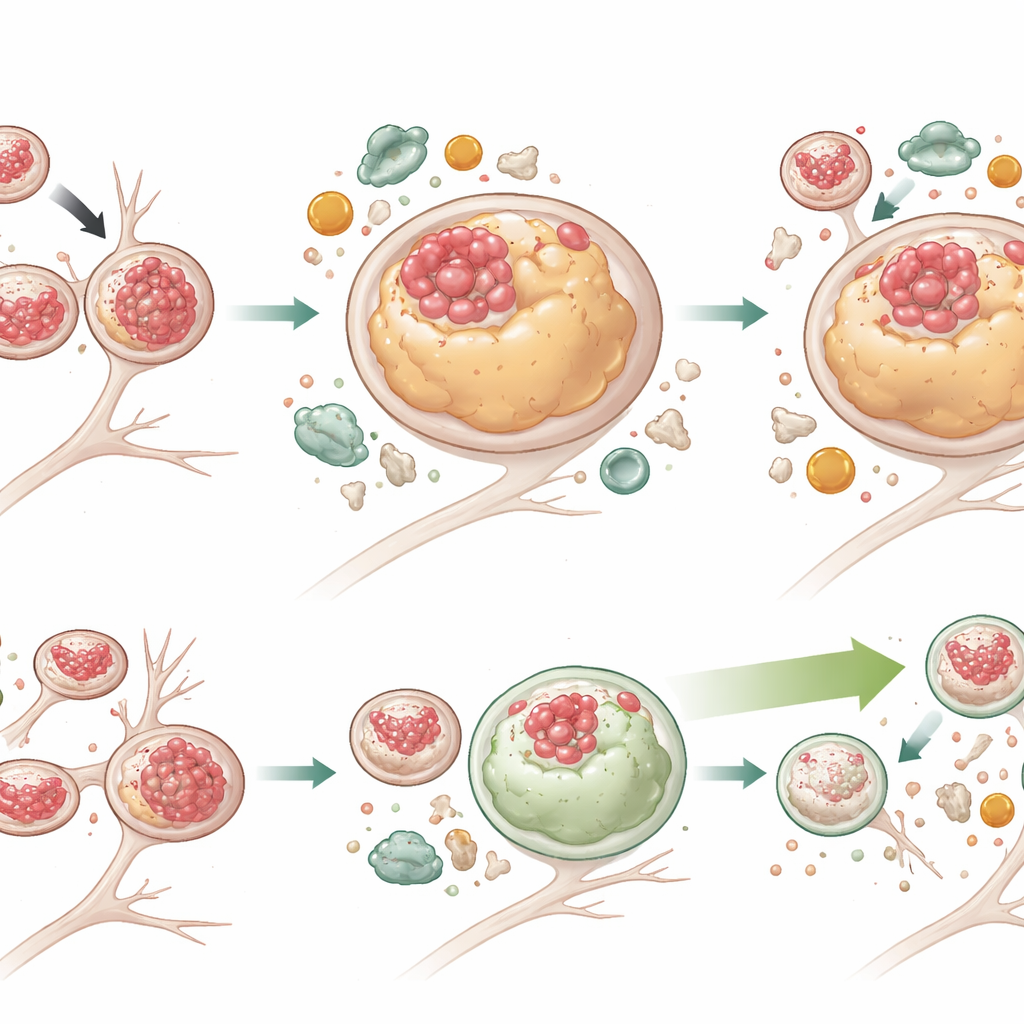
在未修复交通堵塞的情况下增强细胞清理
为测试增强自噬是否能克服这些问题,团队用G2-567处理神经元,这是一种先前被证明能刺激自噬-溶酶体系统的小分子。两周处理后,突变神经元的总Tau和磷酸化Tau水平均显著降低,许多溶酶体再次不含Tau,溶酶体体积也回缩到接近正常水平。活跃自噬的标志物增加,而p62——作为降解停滞的指标——在突变细胞中下降,表明货物被更有效地分解。有趣的是,G2-567并未纠正所有缺陷:突变神经元的溶酶体仍然倾向于位于远离细胞体的位置并且移动迟缓,与溶酶体运输相关的适配蛋白(JIP3)仍然偏高。这表明溶酶体的运动功能与其降解功能在一定程度上可被解耦,仅改善降解可能就足以减少有毒Tau的堆积。
这对未来痴呆治疗意味着什么
对非专家而言,关键结论是:在这种遗传性额颞叶痴呆模型中,问题并非仅仅是Tau变得异常,而是神经元的回收系统跟不上。p.R406W Tau突变直接干扰了自噬-溶酶体途径的多个步骤,导致Tau——尤其是其磷酸化形式——与其他未被降解的物质一起在溶酶体表面和内部积累。通过药理学手段促使细胞的清理机器更努力地工作,研究者得以降低Tau水平并使溶酶体大小恢复正常,尽管运输缺陷仍然存在。这些发现强化了这样一种观点:设计能够安全增强自噬和溶酶体功能的药物,可能有助于恢复Tau相关痴呆以及诸如阿尔茨海默病等更常见疾病中的蛋白质平衡。
引用: Mirfakhar, F.S., Marsh, J.A., Sato, C. et al. A pathogenic Tau mutation drives autophagy-lysosome dysfunction that limits Tau degradation in a model of frontotemporal dementia. Nat Commun 17, 2699 (2026). https://doi.org/10.1038/s41467-026-70473-5
关键词: Tau蛋白, 自噬, 溶酶体功能障碍, 额颞叶痴呆, 神经退行性疾病