Clear Sky Science · zh
表面疏水性与刚性决定口服纳米颗粒在结肠炎治疗中的蛋白冠
将药丸变得更“聪明”
患有结肠炎等炎性肠病的人常需服用强效抗炎药,但大量药物剂量被浪费或在体内其他部位产生副作用。本研究探索了一种让口服药物更像制导导弹的新方法:通过设计微小的载药颗粒,使其招募体内肠道蛋白作为天然靶向系统,帮助药物定位到驱动肠道炎症的免疫细胞。
肠道如何为纳米颗粒“着装”
任何纳米颗粒进入体内后,都会很快被一层薄薄的蛋白质包裹,形成科学家所称的“蛋白冠”。在患病的肠道中,这层冠与健康组织中的不同,因为局部的蛋白组成发生了变化。作者此前发现,结肠炎会产生一种特殊的肠道冠,能够在一定程度上将颗粒引导至称为巨噬细胞的免疫细胞——这些细胞既助长也解决炎症。在此基础上,他们旨在通过调整载药颗粒的两个基本特征——表面疏水性(排水性)和刚性(硬度)——来刻意塑造该蛋白冠,将疾病自发产生的温和效应转化为强效的靶向策略。
使颗粒对蛋白更具吸引力
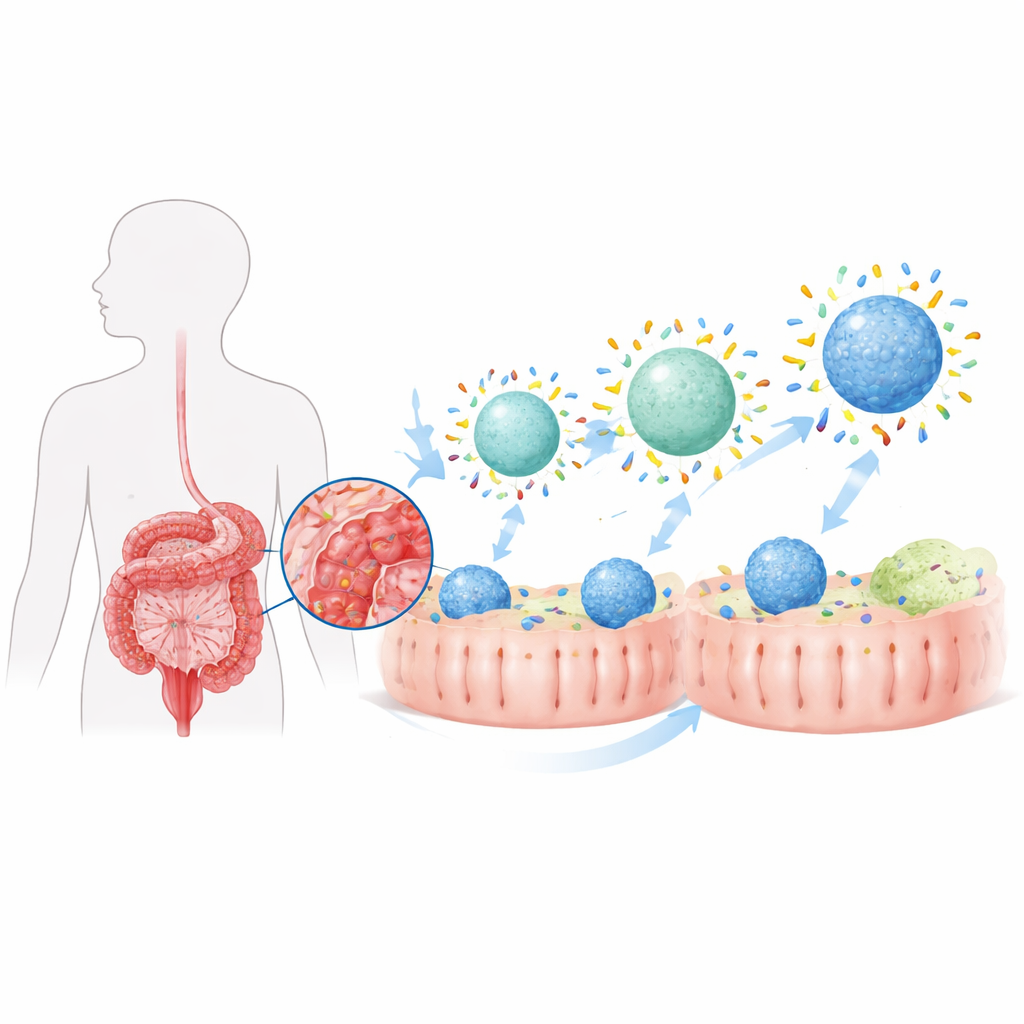
研究团队构建了类似微小脂质囊泡的脂质基纳米颗粒,并通过添加不同量的一种常用聚合物涂层来调节其表面的亲水或疏水特性。表面更疏水的颗粒在接触结肠炎相关液体时,无论在动物体内还是试管实验中,都结合了更多的肠道蛋白。当这些“疏水型”颗粒装载了类固醇布地奈德并口服给予结肠炎大鼠时,它们向结肠巨噬细胞递送了远多于亲水版本的药物。因此,被治疗的动物恢复了更多体重,结肠缩短和组织损伤更少,肠道内炎性分子水平也更低。然而,尽管炎症有所好转,但并未完全恢复到健康状态,这表明仅仅增加蛋白冠的总体量还不够。
通过增强刚性选择更合适的“伙伴”
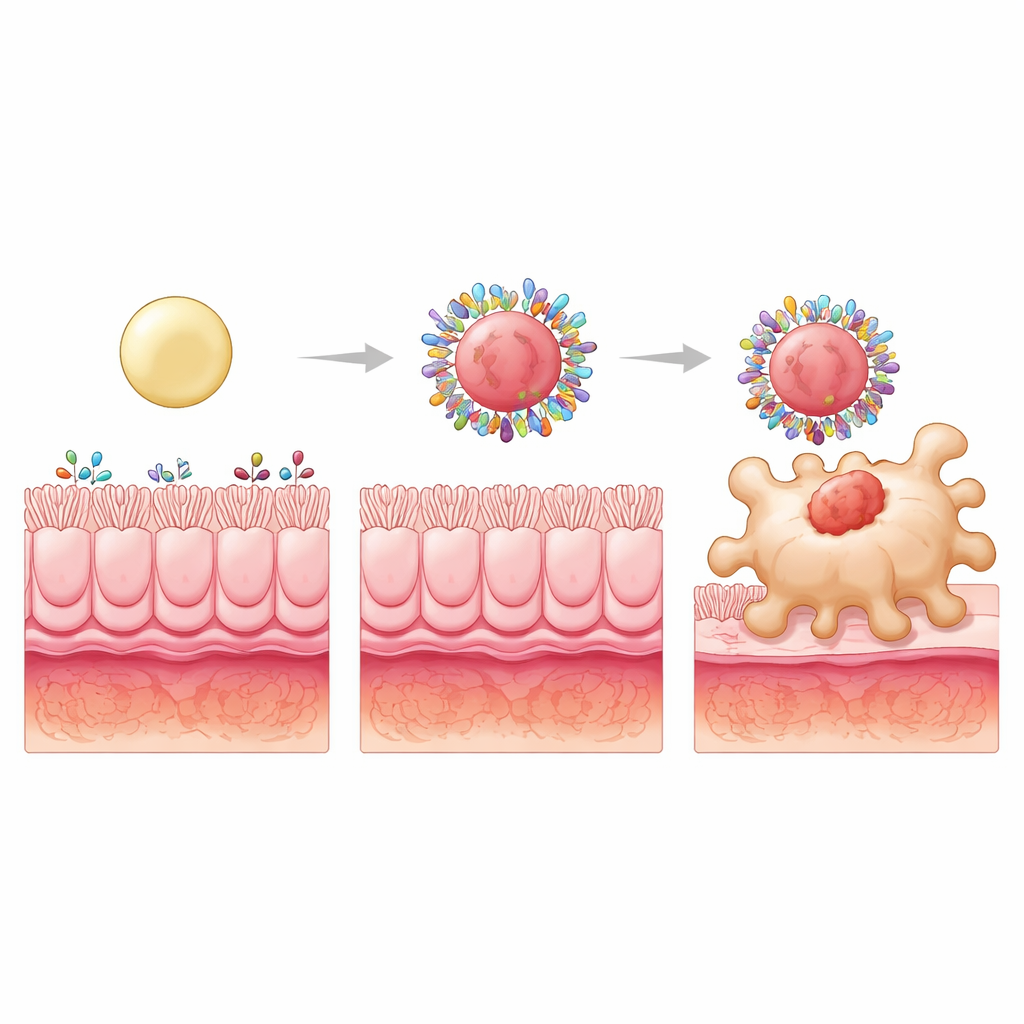
为进一步推进这一概念,研究者保持颗粒表面疏水性不变,但通过在核心填充不同尺寸的塑料微球改变内部结构,使颗粒呈现软、中等或高刚性。三种颗粒捕获的肠道蛋白总量相似,但蛋白组成发生了变化。刚性最高的颗粒形成的蛋白冠中富含能与巨噬细胞表面受体结合或携带巨噬细胞摄取的小分子营养物的蛋白质。其中一种蛋白S100A8在发炎肠道中含量丰富,能够与特定的巨噬细胞受体相互作用。在蛋白冠上阻断S100A8能显著减少巨噬细胞对高刚性颗粒的摄取,显示出它是由颗粒刚性选择出的关键靶向成分。
从更好靶向到更佳修复
当布地奈德被封装入这些高疏水、高刚性的颗粒并口服给予结肠炎大鼠时,其疗效显著。刚性较高的配方不仅减少了肠道损伤和氧化应激,还将多种炎性信号恢复到健康动物的水平。它恢复了“攻击型”和“镇静型”巨噬细胞之间更健康的平衡,并增强了有助于抑制免疫反应的调节性T细胞。重要的是,这些益处依赖于结肠炎中被改变的蛋白环境;相同设计在健康大鼠中未表现出特殊靶向性,这强调了蛋白冠是一个动态且疾病特异性的盟友。
这对未来药物的意义
这项工作表明,我们可以通过调节口服载体的表面和力学特性,引导体内自身蛋白充当智能、可自我更新的“标签”。研究者先通过疏水表面增加蛋白捕获,然后利用刚性偏好像S100A8这样的巨噬细胞归巢蛋白,创造出能够自然识别并定位驱动结肠炎的免疫细胞并将疗法送达其所需之处的纳米颗粒。同样的设计逻辑——操控颗粒在肠道表面的感觉和行为——可被应用于多种纳米医药和疾病,为无需添加人工靶向分子的更微妙靶向治疗提供了一条新途径。
引用: Wu, J., Ni, M., Xing, L. et al. Surface hydrophobicity and rigidity determines protein corona on orally delivered nanoparticles treating colitis. Nat Commun 17, 2497 (2026). https://doi.org/10.1038/s41467-026-70453-9
关键词: 纳米颗粒药物递送, 炎性肠病, 蛋白冠, 口服纳米药物, 巨噬细胞靶向