Clear Sky Science · zh
跨NS4B同源物的属级互作图谱鉴定出UFM化在正黄病毒复制中的保守作用
这项病毒研究为何重要
登革热、寨卡和西尼罗河病毒等病毒正在扩散到新的地区,可引起从发热到脑部感染和出生缺陷等多种疾病。然而,我们仍然缺乏广泛、可靠的治疗方法。本研究探索了这些病毒与一种鲜为人知的细胞标记系统——UFM化之间的隐秘协作如何帮助病原体增殖。通过跨多种相关病毒绘制这种关系,作者发现了一个共同的薄弱环节,可能被用于开发未来的抗病毒药物。
追踪一个关键的病毒内部因子
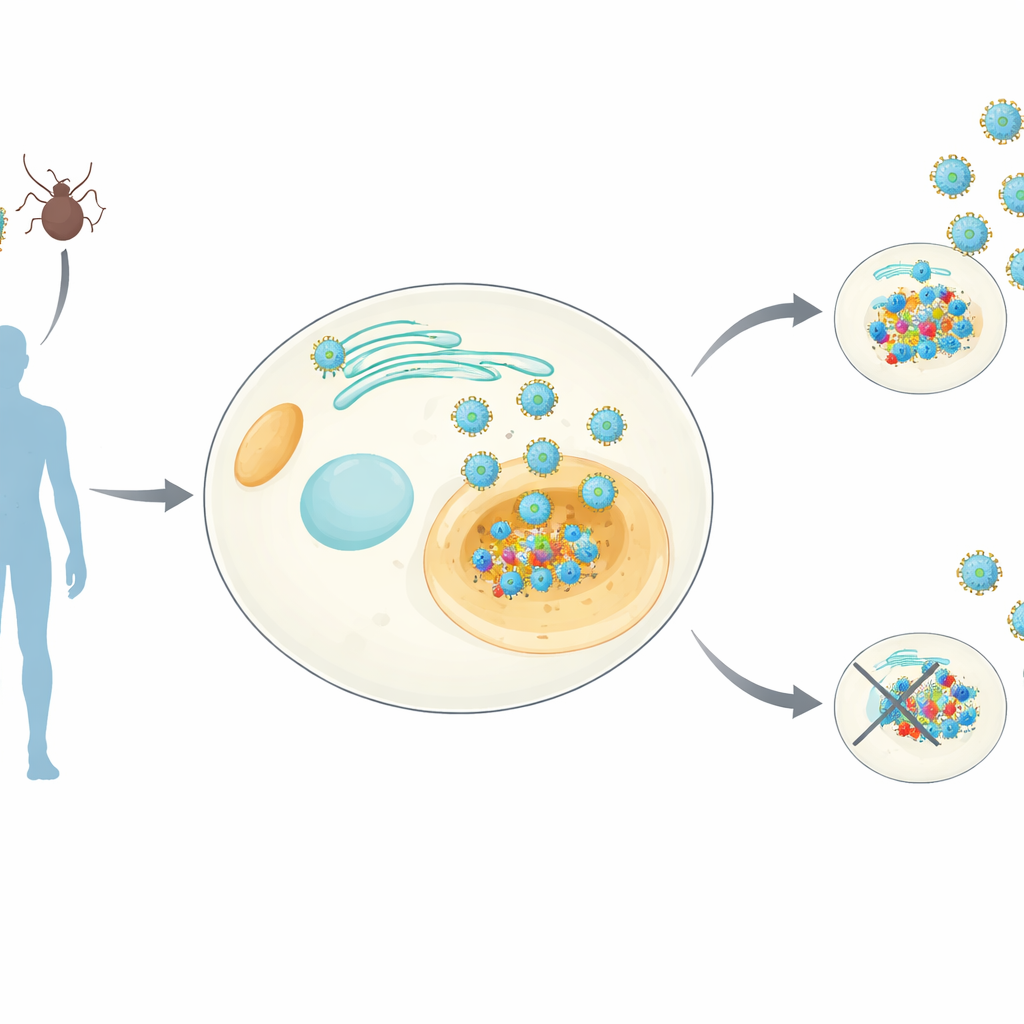
正黄病毒科(orthoflavivirus)包括登革热、寨卡、黄热等病毒——它们都携带一个名为NS4B的小蛋白,嵌入在我们细胞内部的膜中。已知NS4B对病毒复制至关重要,但其确切功能一直不明。研究人员构建了稳定表达来自八种不同正黄病毒的NS4B的人类细胞系,随后使用灵敏的质谱技术拉下NS4B及其结合的人类蛋白,并并行测量NS4B表达如何改变细胞内蛋白的整体组成。这产生了一个属级的“互作图谱”——他们称之为NS4Bome——显示出既有共同的也有病毒特异的宿主靶点。
共同策略与特有手段
该图谱揭示了538种与NS4B相互作用的人类蛋白,以及超过500种在NS4B存在时丰度发生变化的蛋白。许多蛋白集中在调控线粒体能量产生、内膜形态塑造以及新合成蛋白和脂类的运输等通路中。有些相互作用在大多数病毒中共享,暗示所有正黄病毒可能采用的进化保守策略。另一些则仅出现在某些物种或毒株中,或能解释为何部分病毒偏好蚊子而非蜱虫传播,或为何导致脑部疾病而非出血热。这一系统视角将以往零散的研究串联成一张连贯的病毒改造细胞的图谱。
一个意外的盟友:UFM化系统
在NS4B结合的众多伙伴中,尤为突出的一个是UBA5——UFM化途径的起始酶。UFM化是将一个小蛋白标签UFM1附加到选定靶标上的细胞系统,影响诸如蛋白质量控制和应激反应等过程。使用RNA干扰和基于CRISPR的基因敲除,研究团队证明缺失UBA5或无法执行UFM化的细胞其寨卡及若干相关病毒的复制显著降低。重新引入正常的UBA5可恢复病毒生长,而不能驱动UFM化的突变形式则不能恢复,证明了这一标记活性本身对感染至关重要。
标记如何支持病毒工厂
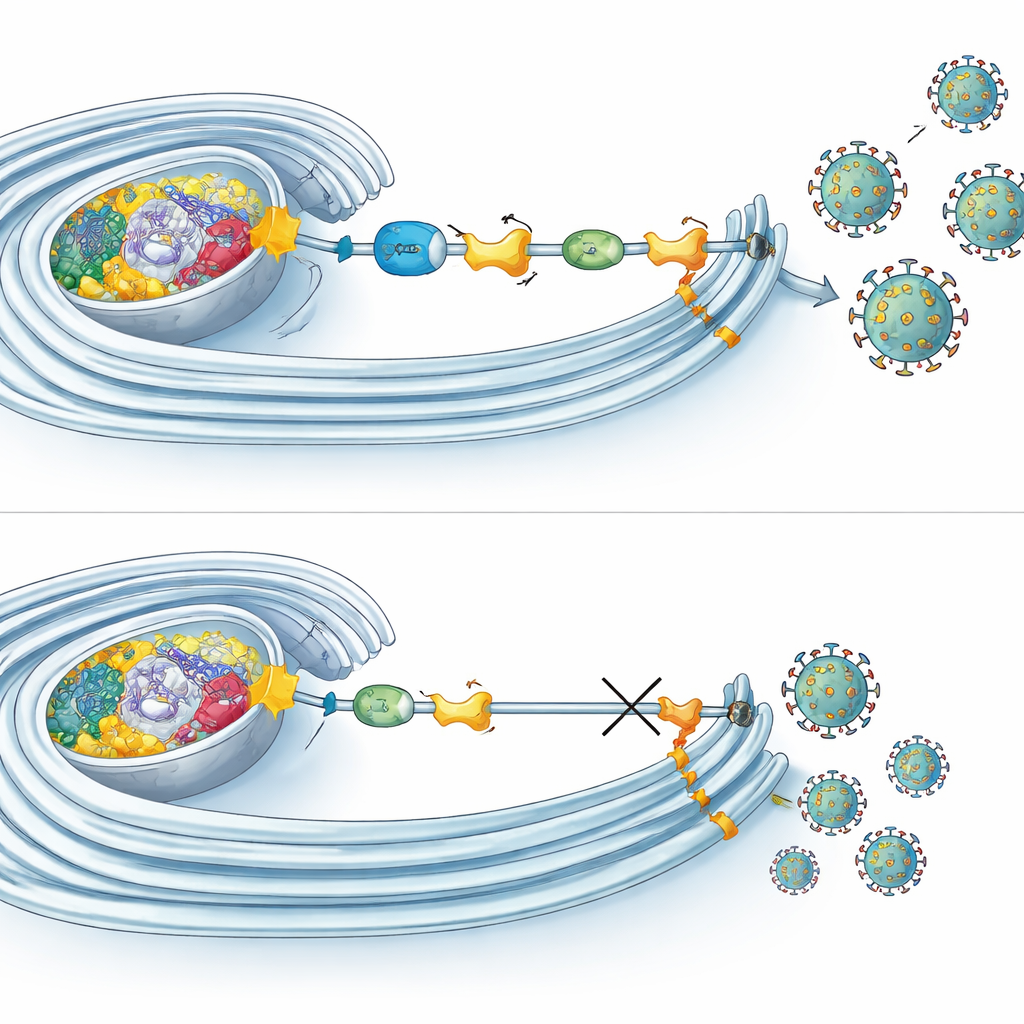
显微镜和生化实验显示,多种UFM化成分在病毒RNA在改造的膜内复制的位点聚集。在那里,它们不仅与NS4B结合,还与构建复制机械的其他病毒蛋白相关联。有趣的是,阻断UFM化并不阻止病毒入侵、RNA合成或蛋白质翻译。相反,它主要损害生命周期的晚期阶段,如感染性颗粒的组装或释放。与此同时,UFM化还影响线粒体的呼吸:当该途径被禁用时,细胞表现出耗氧量降低和线粒体形态改变。相比之下,在寨卡感染的早期,线粒体呼吸增强,这表明病毒可能在需要大量能量时借助UFM化来提升细胞的能量输出。
在细胞与小型鱼类中测试药物
随后作者转向一种小分子化合物DKM 2‑93,该化合物可阻断UBA5的活性位点。在培养的人类细胞中,该抑制剂在对细胞影响较小的剂量下将寨卡病毒产量大约降低了十倍,并在多种细胞类型中显示活性。为检验该策略在生物体内是否可行,他们采用了模拟发育中大脑关键疾病特征的寨卡感染斑马鱼模型。在早期脑发育阶段用DKM 2‑93处理受感染胚胎,显著降低了病毒RNA水平并减少了出现严重畸形的鱼的比例,表明在体内具有真实的抗病毒益处。
对未来治疗的意义
通过构建NS4B在多种正黄病毒中与人类蛋白互作的全面图谱,这项研究指出UFM化作为一个被病毒依赖的保守辅助通路,有助于生成感染性颗粒。由于相同的宿主系统似乎支持登革热、寨卡、西尼罗河等病毒,选择性抑制UFM化的药物可能成为广谱抗病毒剂,而非只针对单一病毒。尽管仍需进一步明确哪些蛋白被标记并确保安全性,但这些发现确定了一个有前景的基于宿主的靶点,未来有望用单一治疗策略在多种蚊媒与蜱媒疾病爆发时发挥作用。
引用: Rajasekharan, S., Barragan Torres, V.A., Pinheiro Gomes, Y.C. et al. A genus-wide interaction atlas across NS4B orthologues identifies a conserved role for UFMylation in orthoflavivirus replication. Nat Commun 17, 2489 (2026). https://doi.org/10.1038/s41467-026-70437-9
关键词: 寨卡病毒, 登革热, 宿主–病毒互作, UFM化, 广谱抗病毒药