Clear Sky Science · zh
3D 五细胞共培养模型揭示高级别浆液性卵巢癌中恶性细胞驱动的巨噬细胞极化
这项研究为何重要
卵巢癌常在晚期才被发现,并且经常对治疗产生顽固耐受性。其原因之一在于癌细胞生存在一个由免疫细胞和结缔组织细胞组成的支持性“邻里”中,这些细胞帮助肿瘤逃避药物和机体防御。该研究构建了一个复杂的实验室模型——在 3D 条件下使用五种人类细胞——以模拟这一邻里,并实时观察癌细胞如何将邻近的免疫细胞(称为巨噬细胞)推向帮助肿瘤而非对抗肿瘤的角色。
构建微型肿瘤“邻里”
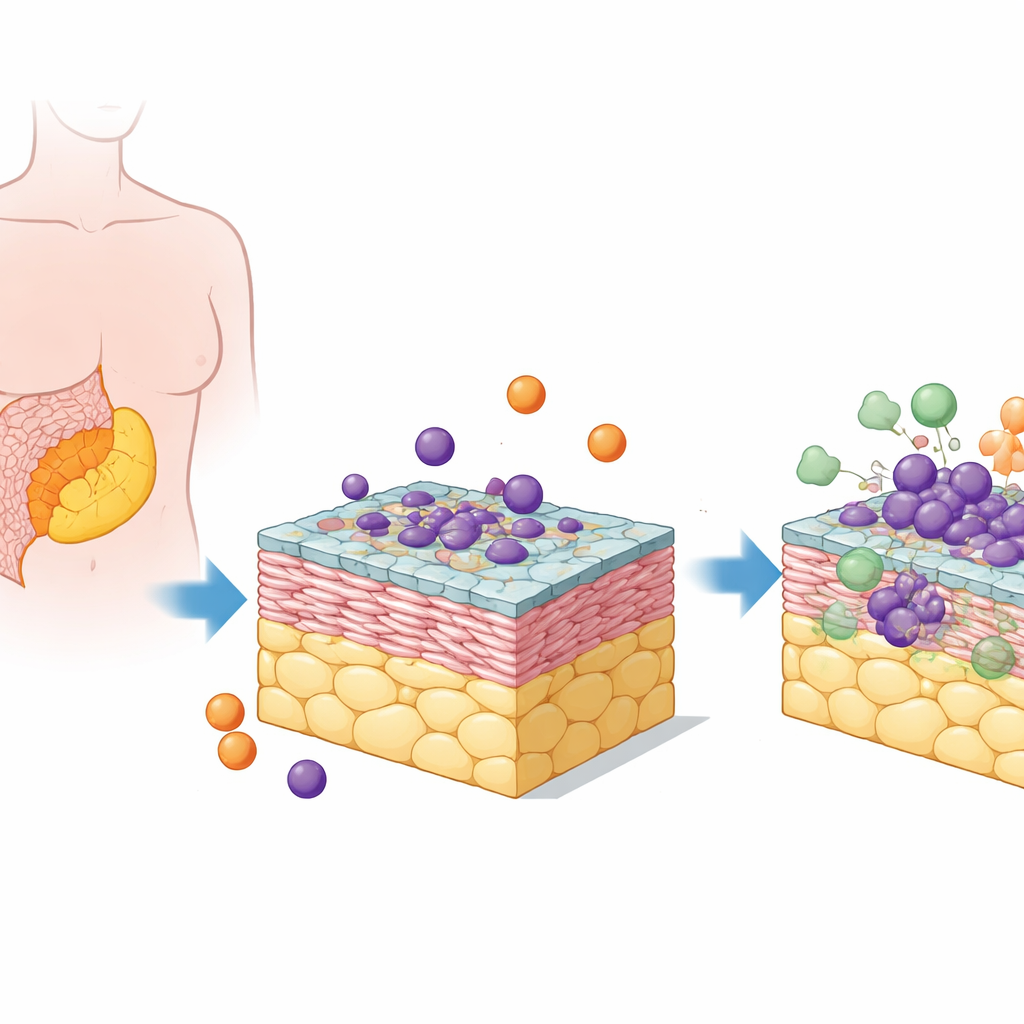
研究人员聚焦于高级别浆液性卵巢癌,这是该病最常见且致死率最高的类型。其转移灶常在腹腔内的一种脂肪组织——网膜中生长。为重现这一环境,研究团队将人类脂肪细胞、结缔组织细胞(成纤维细胞)、一层间皮细胞、卵巢癌细胞以及循环免疫细胞(单核细胞)结合起来。这五种细胞被组装成叠层的 3D “五细胞共培养”体系,比传统的平面培养更接近真实的肿瘤沉积物。
把免疫防御者变成旁观者
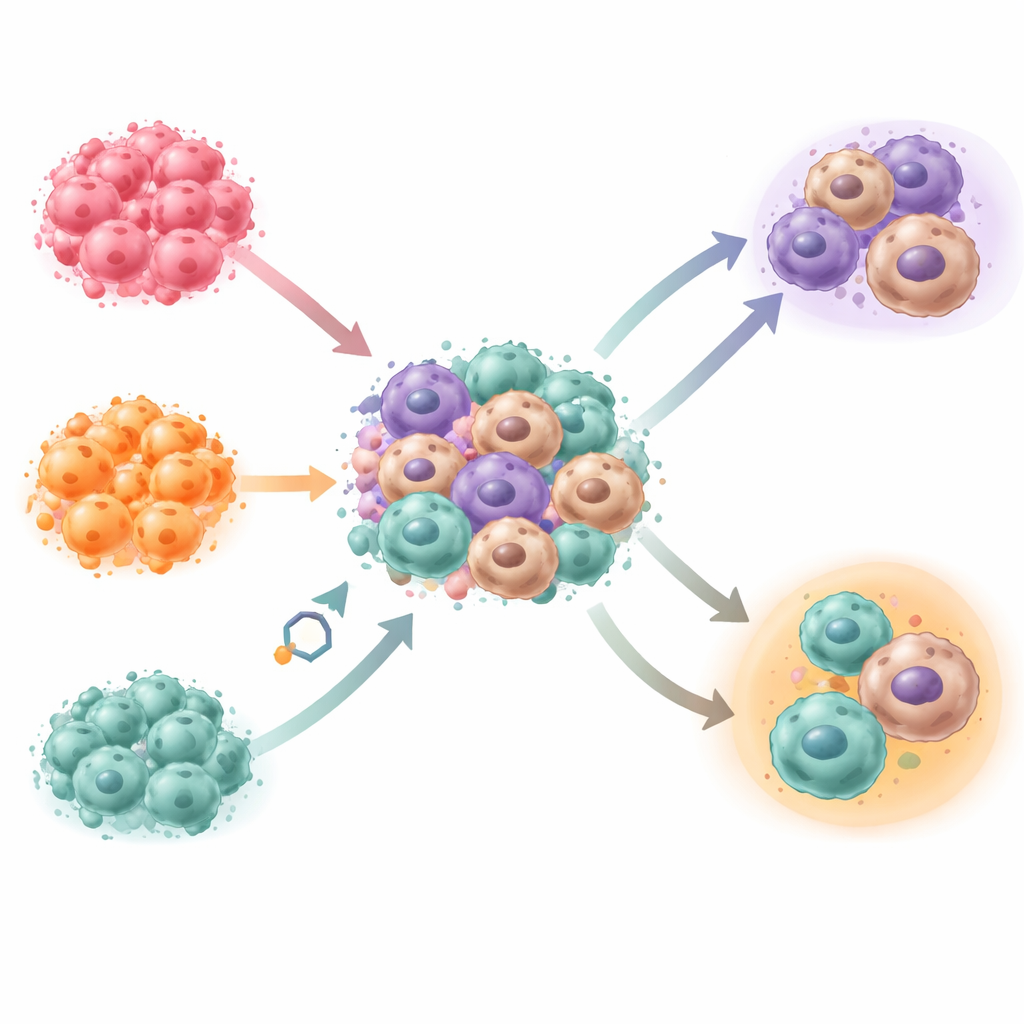
在这个微型肿瘤环境中,单核细胞自然分化为巨噬细胞——而无需实验室通常添加的人工促生长信号。通过基因活性谱分析并与来自患者肿瘤样本的单细胞数据比对,团队表明模型中的巨噬细胞与真实卵巢癌转移灶中的巨噬细胞高度相似。不同的癌细胞系产生了不同组合的巨噬细胞类型以及不同的微型肿瘤结构,表明癌细胞内部的遗传和分子差异强烈塑造了周围的免疫格局。
癌细胞如何躲避免被吞噬
巨噬细胞可以吞噬并销毁癌细胞,但肿瘤常在其表面发出“别吃我”的信号。团队在三种在 3D 模型中培养的卵巢癌细胞系上检测了两种此类信号——CD47 和 CD24。表达这些信号较高的癌细胞较不容易被巨噬细胞吞噬。在五细胞共培养中,一种细胞系容易被吞噬,另一种大多能逃避,而第三种表现出混合行为。实时成像显示,巨噬细胞的移动方式及其相对于癌细胞簇的位置随癌细胞系而异,反映出与患者组织中观察到的模式一致的行为。
测试重新唤醒免疫攻击的方法
由于这些表面信号可以用抗体药物阻断,研究人员用针对 CD47 或 CD24 的实验性抗体处理了模型。在用某一特定癌细胞系构建的五细胞共培养中,阻断任一信号都增加了巨噬细胞与癌细胞的接触、促进了吞噬并减少了癌细胞数量,同时对模型中其他细胞影响甚微。在另一种具有强抗性的癌细胞系中,阻断这些信号几乎无效,但抑制另一条通讯通路(TGFβ 通路)则在依赖巨噬细胞存在的前提下减少了癌细胞——提示存在替代的、非吞噬性杀伤机制,比如有毒细胞因子的释放。
对患者意味着什么
对普通读者来说,关键信息是:并非所有卵巢癌以同样方式操纵免疫细胞,即便它们在显微镜下外观相似。通过从人源组织构建一个真实的五细胞 3D 模型,这项工作展示了肿瘤细胞如何将巨噬细胞调节为忽视或攻击肿瘤,以及阻断特定“别吃我”信号有时如何能翻转这一开关。该模型高度模拟患者肿瘤,使其成为一种有前景的中等通量测试平台,用以筛选哪些免疫靶向药物最可能对特定肿瘤谱有效。长期来看,这类个体化的体外系统或能帮助将患者与最能唤醒其自身免疫系统对抗卵巢癌的治疗匹配起来。
引用: Malacrida, B., Elorbany, S., Laforêts, F. et al. 3D pentaculture model unveils malignant cell-driven macrophage polarization in high-grade serous ovarian cancer. Nat Commun 17, 2451 (2026). https://doi.org/10.1038/s41467-026-70398-z
关键词: 卵巢癌, 肿瘤微环境, 巨噬细胞, 免疫治疗, 3D 细胞培养